Kiểm tra 45’ môn: Hoá 9 (bài số 1)
Bạn đang xem tài liệu "Kiểm tra 45’ môn: Hoá 9 (bài số 1)", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
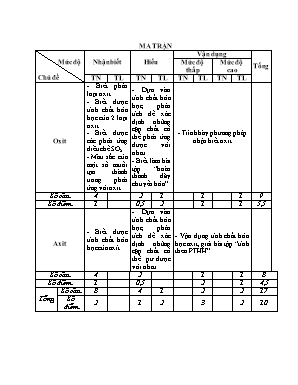
MA TRẬN Mức độ Chủ đề Nhận biết Hiểu Vận dụng Tổng Mức độ thấp Mức độ cao TN TL TN TL TN TL TN TL Oxit - Biết phân loại oxit - Biết được tính chất hóa học của 2 loại oxit - Biết được các phản ứng điều chế SO2 - Màu sắc của một số muối tạo thành trong phản ứng với oxit - Dựa vào tính chất hóa học, phân tích để xác định những cặp chất có thể phản ứng được với nhau - Biết làm bài tập “hoàn thành dãy chuyển hóa” - Trình bày phương pháp nhận biết oxit Số câu 4 2 1 1 1 9 Số điểm 1 0,5 2 1 1 5,5 Axit - Biết được tính chất hóa học của axít - Dựa vào tính chất hóa học, phân tích để xác định những cặp chất có thể pư được với nhau - Vận dụng tính chất hóa học axit, giải bài tập “tính theo PTHH” Số câu 4 2 1 1 8 Số điểm 1 0,5 2 1 4,5 Tổng Số câu 8 4 1 2 2 17 Số điểm 2 1 2 3 2 10 KIỂM TRA 45’ Môn: Hoá 9 (Bài số 1) A.TRẮC NGHIỆM (3đ): Hãy khoanh tròn vào một trong các chữ cái A,B,C,D đứng trước câu trả lời đúng: Câu 1: Phản ứng giữa H2SO4 với NaOH là phản ứng A. trung hoà B. phân huỷ C. thế D. hoá hợp Câu 2: Dãy chất gồm những Oxyt tác dụng được với axit là A. CO2, P2O5, CaO B. FeO, NO2, SO2 C. CO2, P2O5, SO2 . D .CuO, K2O, CaO Câu 3: Những nhóm oxyt tác dụng được với nước là: A. CO2, FeO, BaO B. CaO, CuO, SO2 C. SO2, Fe2O3, BaO D. Na2O, CaO,CO2 Câu 4:Dãy chất những oyt bazơ tác dụng được với axit là A. CaO, K2O, CuO B. CO2, P2O5, CaO C. FeO, NO2, SO2 D. CO2, P2O5, SO2 Câu 5: Chất khi tác dụng với dung dịch HCl tạo ra một dung dịch có màu vàng nâu là A. Cu B. Fe C. Fe2O3 D. ZnO Câu 6: Những nhóm oxyt tác dụng được với nước là: A. CO2, FeO, BaO B. Na2O, CaO,CO2 C. CaO, CuO, SO2 D. SO2, Fe2O3, BaO Câu 7: Phân biệt hai dung dịch HCl và H2SO4 người ta dùng: A. CuO B. Fe(OH)2 C. Zn D. Ba(OH)2 Câu 8: Khí SO2 được điều chế từ cặp phản ứng A. K2SO3 và KOH B. H2SO4 đặc, nguội và Cu C. Na2SO3 và HCl D. Na2SO4 và H2SO4 Câu 9:Chất khi tác dụng với dung dịch H2SO4 tạo ra dung dịch có màu xanh lam là A. Cu(OH)2 B. BaCl2 C. NaOH D. Fe Câu 10:Để làm khô hỗn hợp khí CO2 và SO2 có lẫn hơi nước, người ta dùng: A. CaO B. H2SO4 đặc C. Mg D. HCl Câu 11: Khí SO2 được điều chế trong phòng thí nghiệm bằng phản ứng giữa Na2 SO4 và H2SO3 Na2SO3 và Na2SO4 Na2SO3 và NaOH Na2SO3 và H2SO4 Câu 12: Khí CO làm chất đốt trong công nghiệp có lẫn tạp chất CO2 và SO2, làm thế nào để loại bỏ tạp chất trên: A. Tác dụng với dd H2SO4 B. Tác dụng với dd Ca(OH)2 C. Tác dụng với dd HCl D. Tác dụng với dd NaCl B.TỰ LUẬN (7đ): Câu 1(2 đ).Hãy viết PTHH thực hiện sự chuyển hóa sau: K ---(1)----> K2O ----(2)-----> KOH ----(3)-----> K2SO4 ---(4)-----> BaSO4 Câu 2 (2đ). Hãy trình bày phương pháp hóa học để nhận biết hai chất rắn màu trắng là: NaOH,H2SO4, HCl,NaCl.Viết PTPƯ minh họa . Câu 3 (3 đ).Trung hòa vừa đủ 500ml dung dịch Ba(OH)2 1M với dung dịch H2SO4 15%. Sau khi phản ứng kết thúc thấy tạo ra chất kết tủa màu trắng. Hãy : a) Viết PTHH xảy ra . b) Tính khối lượng dung dịch H2SO4 đã dùng . c) Tính khối lượng chất kết tủa thu được. (Cho Ba = 137, H = 1, O = 16 , S = 32) ĐÁP ÁN I.Trắc nghiệm : (3đ)- Mỗi câu đúng 0,25 đ 1 2 3 4 5 6 7 8 9 10 11 12 A D D A C B D C A B D B II.Tự luận :(7 đ) CÂU ĐÁP ÁN ĐIỂM Câu 1 (2đ) Mỗi PTHH đúng 0,5đ (sai hệ số -0,25đ) (1): 4 K + O2 2K2O (2) : K2O + H2O 2KOH (3): H2SO4 + 2KOH K2SO4 + 2H2O (4) K2SO4 + BaCl2 BaSO4 + 2KCl 0.5.4=2đ Câu2 (2đ) Lấy mỗi ít trong các chất ra bốn ống nghiệm. Sau đó, dùng quỳ tím nhúng vào bốn ống nghiệm. Nếu : - Quỳ tím chuyển màu xanh NaOH - Quỳ tím chuyển màu đỏ HCl,H2SO4. - Không hiện tượng là NaCl Cho dd BaCl2 vào 2 ống chứa dd axit ống nào tạo kết tủa trắng là H2SO4 còn lại không hiện tượng là HCl BaCl2 + H2SO4 BaSO4 + 2HCl 0,5đ 0.5đ 0.5đ 0.5đ Câu3 (3đ) PTHH : Ba(OH)2 + H2SO4 BaSO4 + 2 H2O (1) 0,5mol 0,5 mol 0,5mol b)Ta có : nBa(OH)2 = 1.0,5 = 0,5 mol mH2SO4 = 0,5.98 = 49 g Vậy mdd H2SO4 = =326,7g c) mBaSO4 = 0,5. 233 = 116,5 g 0.5đ 0.5đ 0.5đ 0.5đ 0.5đ 0.5đ
Tài liệu đính kèm:
 KT_1_Tiet_De_1.doc
KT_1_Tiet_De_1.doc





