Đề kiểm tra học kì 2, năm học 2015 - 2016 (tham khảo) môn: Hóa học 8 thời gian: 60 phút
Bạn đang xem tài liệu "Đề kiểm tra học kì 2, năm học 2015 - 2016 (tham khảo) môn: Hóa học 8 thời gian: 60 phút", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
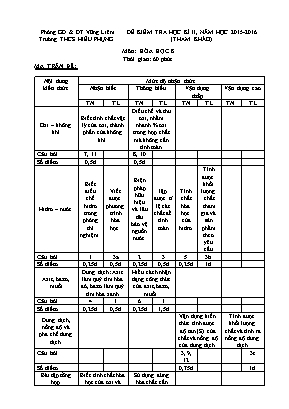
Phòng GD & ĐT Vũng Liêm Trường THCS HIẾU PHỤNG ĐỀ KIỂM TRA HỌC KÌ II, NĂM HỌC 2015-2016 (THAM KHẢO) Môn: HÓA HỌC 8 Thời gian: 60 phút MA TRẬN ĐỀ: Nội dung kiến thức Mức độ nhận thức Nhận biết Thông hiểu Vận dụng thấp Vận dụng cao TN TL TN TL TN TL TN TL Oxi – không khí Biết tính chất vật lý của oxi, thành phần của không khí. Điều chế và thu oxi, nhẩm nhanh % oxi trong hợp chất mà không cần tính toán. Câu hỏi 7, 11 8, 10 Số điểm 0,5đ 0,5đ Hidro – nước Biết điều chế hidro trong phòng thí nghiệm. Viết được phương trình hóa học. Biện pháp hữu hiệu và lâu dài bảo vệ nguồn nước lập được tỉ lệ các chất để tính toán Tính chất hóa học của hidro Tính được khối lượng chất tham gia và sản phẩm theo yêu cầu Câu hỏi 1 3a 2 3 5 3b Số điểm 0,25đ 0,5đ 0,25đ 0,5đ 0,25đ 1đ Axit, bazơ, muối Dung dịch: Axit làm quỳ tím hóa đỏ, bazơ làm quỳ tím hóa xanh Hiểu cách nhận dạng công thức của axit, bazơ, muối. Câu hỏi 4 1 6 1 Số điểm 0,25đ 0,5đ 0,25đ 1,5đ Dung dịch, nồng độ và pha chế dung dịch. Vận dụng kiến thức tính được độ tan (S) của chất và nồng độ của dung dịch. Tính được khối lượng chất và tính ra nồng độ dung dịch Câu hỏi 3, 9, 12 3c Số điểm 0,75đ 1đ Bài tập tổng hợp Biết tính chất hóa học của oxi và nước Sử dụng đúng hóa chất cần thiết để lập phương trình hóa học Câu hỏi 2 2 Số điểm 1đ 1đ Tổng số câu Tổng số điểm Tỉ lệ 4 1,0 (10%) 3 2,0 (20%) 4 1,0 (10%) 3 3,0 (30%) 4 1đ (10%) 1 1,0 (10%) 1 1,0 (10%) ĐỀ I- PHẦN TRẮC NGHIỆM: (3 điểm) Chọn câu trả lời đúng nhất, mỗi câu 0,25 điểm. 1/ Cặp chất nào sau đây dùng để điều chế hidro? A/ Zn và O2 B/ Al và H2SO4 C/ H2O và CaO D/ MgO va HCl 2/ Biện pháp bảo vệ nguồn nước hữu hiệu nhất là? A. Xử lý rác thải. B. Xử phạt người vi phạm. C. Tuyên truyền, giáo dục ý thức bảo vệ môi trường cho mọi người. D. Lọc nước thật kỹ trước khi xử dụng. 3/ Hòa tan 8g NaOH vào nước được 50ml dung dịch có nồng độ là: A. 0,16M B. 16M C. 4M D. 0,4M 4/ Dung dịch Bazơ là những chất làm cho quì tím chuyển sang màu nào trong số các màu cho dưới đây? A. Xanh B. Đỏ C. Tím D. vàng 5/ Cho 48g CuO tác dụng với khí H2 khi đun nóng, thể tích khí H2 (đktc) cần cho phản ứng trên là: A. 11,2 lít B. 13,44 lít C. 13,88 lít D. 13,3 lít 6/ Dãy chất nào chỉ bao gồm toàn muối? A. MgCl2, Na2SO4, KNO3 B. HCl. KOH, CaO C. Al2(SO4)3; MgO; H3PO4 D. NaOH, MgCO3, H2O 7/ Oxi hóa lỏng ở nhiệt độ: A. 1830C B. 1960C C. – 1830C D. – 1960C 8/ Cho pthh: 2KMnO4 K2MnO4 + A + O2 A là chất nào sau đây? A. MnO2 B. Mn2O2 C. Mn2O7 D. MnO 9/ Ở 18 0C, khi hòa tan hết 5,3g Na2CO3 vào 25g nước thì được dung dịch bão hòa. Độ tan của Na2CO3 là: A. 0,212g B. 2,12g C. 21,2g D. 212g 10/ Phần trăm về khối lượng của oxi cao nhất trong oxit nào cho dưới đây ? A. CuO B. ZnO C.PbO D. MgO 11/ Thành phần của không khí gồm: A. 21% O2, 78% N2 và 1% các khí khác (CO2, CO...) B. 78% O2, 21% N2 và 1% các khí khác (CO2, CO...) C. 21% O2, 1% N2 và 78% các khí khác (CO2, CO...) D. 1% O2, 78% N2 và 21% các khí khác (CO2, CO...) 12/ Hòa tan 10g muối ăn vào 40g nước được dung dịch có nồng độ: A. 25% B. 2,50% C. 2,% D. 20% II-PHẦN TỰ LUẬN: (7đ) Câu 1: (2đ) Có 3 lọ không nhãn chứa 3 chất lỏng không màu là KOH. H2SO4 và H2O . Nêu phương pháp hóa học để nhận biết từng chất trên? Câu 2: (2đ) Hãy viết các PTHH thực hiện những chuyển đổi hoá học sau: a/ Na Na2O NaOH b/ P P2O5 H3PO4 Câu 3: (3đ) Trong phòng thí nghiệm, người ta cho kẽm (Zn) tác dụng vừa đủ với một lượng dung dịch axit clohidric (HCl) để điều chế 5,6 lít khí hidro (H2) ở đktc. a. Lập phương trình hóa học của phản ứng. b. Tính khối lượng Zn đã phản ứng? c. Tính nồng độ phần trăm của dung dịch HCl, biết khối lượng dung dịch HCl tham gia phản ứng là 200g. (Zn = 65 ; H = 1 ; Cl = 35,5) ---- hết ---- (KIỂM TRA HỌC KÌ II, NĂM HỌC 2015-2016) ĐÁP ÁN + BIỂU ĐIỂM HÓA 8 I-PHẦN TRẮC NGHIỆM: (3đ) 1 2 3 4 5 6 7 8 9 10 11 12 B C C A B A C A C D A D II- PHẦN TỰ LUẬN: (7đ) Câu 1: Lấy mẫu thử. (0,25đ) KOH H2SO4 H2O Quỳ tím Xanh Đỏ Tím (không phản ứng) (0,5đ) (0,5đ) (0,5đ) (0,25đ) Câu 2: a/ (1) 4Na + O2 2Na2O (0,5đ) (2) Na2O + H2O 2NaOH (0,5đ) b/ (1) 4P + 5O2 2P2O5 (0,5đ) (2) P2O5 + 3H2O 2H3PO4 (0,5đ) * Phản ứng không được cân bằng hoặc thiếu điều kiện, nếu đúng sơ đồ phản ứng thì chỉ được chấm phân nửa số điểm cho phản ứng đó. Câu 3: Số mol hidro (đktc) (0,5đ) a. Phương trình hóa học: Zn + 2HCl ZnCl2 + H2↑ (0,5đ) 1 mol 2 mol 1 mol 0,25 mol 0,5 mol 0,25 mol (0,5đ) b. Khối lượng Zn đã phản ứng là: 0,25.65= 16,25 mol (0,5đ) c. - Khối lượng HCl nguyên chất đã phản ứng: 0,5.36,5 = 18,25 g (0,5đ) - Nồng độ phần trăm của dung dịch HCl là: (0,5đ) * Học sinh có thể giải bằng nhiều cách khác nhau nếu đúng vẫn đạt điểm tối đa.
Tài liệu đính kèm:
 HÓA 8.doc
HÓA 8.doc





