Kiểm tra viết môn: Hóa học 9 tiết 10
Bạn đang xem tài liệu "Kiểm tra viết môn: Hóa học 9 tiết 10", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
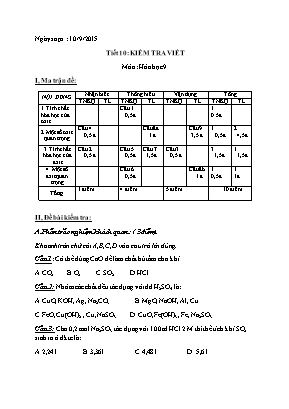
Ngày soạn : 10/9/2015 Tiết 10: KIỂM TRA VIẾT Môn: Hóa học 9 I, Ma trận đề: NỘI DUNG Nhận biết Thông hiểu Vận dụng Tổng TNKQ TL TNKQ TL TNKQ TL TNKQ TL 1.Tính chất hóa học của oxit Câu 1 0,5 đ 1 0.5đ 2.Một số oxit quan trọng Câu 4 0,5 đ Câu8a 1 đ Câu 9 3,5 đ 1 0,5đ 2 4,5đ 3.Tính chất hóa học của axit Câu 2 0,5 đ Câu 5 0,5 đ Câu 7 1,5đ Câu 3 0,5 đ 3 1,5đ 1 1,5đ 4. Một số axit quan trọng Câu 6 0,5 đ Câu8b 1 đ 1 0,5đ 1 1đ Tổng 1 điểm 4 điểm 5 điểm 10 điểm II, Đề bài kiểm tra: A.Phần trắc nghiệm khách quan : ( 3điểm) Khoanh tròn chữ cái A,B,C,D vào câu trả lời đúng. Câu 1: Có thể dùng CaO để làm chất hút ẩm cho khí . A.CO2 B.O2 C. SO2 D.HCl Câu 2: Nhóm các chất đều tác dụng với dd H2SO4 là: A.CuO, KOH, Ag, Na2CO3. B.MgO, NaOH, Al, Cu. C.FeO, Cu(OH)2 , Cu, NaSO3. D. CuO, Fe(OH)3, Fe, Na2SO3. Câu 3: Cho 0,2 mol Na2SO3 tác dụng với 100ml HCl 2 M thì thể tích khí SO2 sinh ra ở đktc là: A.2,24 l B.3,36 l C.4,48 l D. 5,6 l Câu 4: Cho các oxit sau: CaO, SO2, SO3, Na2O, Fe2O3, P2O5,CuO. Những oxit nào thuộc loại oxit bazơ ? A. CaO, Na2O, P2O5, CuO B. CaO, Na2O, Fe2O3, SO2. C. CaO, Na2O, Fe2O3, CuO D. CaO, CuO, Fe2O3, SO3. Câu 5: Để nhận biết được ba dung dịch sau : Na2SO4, H2SO4, NaOH người ta dùng một thuốc thử là: A. Dung dịch BaCl2 B. Quỳ tím C. Dung dịch Ba(OH)2 D. Dung dịch Phenolphtalein Câu 6: Để pha loãng H2SO4 đậm đặc an toàn, cần: A. Cho từ từ H2SO4 đậm đặc vào bình nước. B. Cho từ từ nước vào bình đựng H2SO4 đậm đặc. C. Rót đồng thời H2SO4 đậm đặc và nước vào bình. D. Cách A,B đều dùng được. B. Phần tự luận ( 7 điểm) Câu 7: ( 1,5 đ) Viết PTHH thực hiện dãy chuyển hóa sau, ghi rõ điều kiện phản ứng : S SO2 SO3 H2SO4 CuSO4 (5) Na2SO3 (6 )→ SO2 Câu 8: ( 2 đ) a, Làm thế nào để phân biệt ba chất bột trắng sau: CaO, P2O5, BaSO4. b, Từ 1 tấn lưu huỳnh người ta có thể điều chế được bao nhiêu tấn dung dịch H2SO4 98% nếu hiệu suất phản ứng là 80%. Câu 9: (3,5 điểm) Cho 5,6 lít khí CO2 (đktc) tác dụng vừa đủ với 100 ml dung dịch Ca(OH)2 a. Tính nồng độ mol của dung dịch Ca(OH)2 đã dùng? b. Tính khối lượng chất kết tủa thu được? c. Để trung hòa hết lượng dung dịch Ca(OH)2 trên cần dùng bao nhiêu gam dung dịch HCl nồng độ 20%. III. Đáp án - biểu điểm: A. Phần trắc nghiệm: ( 3 điểm ) - Mỗi câu đúng được 0,5đ : Câu 1 Câu 2 Câu 3 Câu 4 Câu 5 Câu 6 B D A C B A B.Tự luận: ( 7 điểm) Câu Đáp án Điểm 7 Viết đúng mỗi PTHH được 0,25 đ 1) S + O2 SO2 2) 2SO2 + O2 2SO3 3) SO3 + H2O H2SO4 4) H2SO4 + CuO CuSO4 + H2O 5) SO2 + Na2O Na2SO3 6) Na2SO3 + HCl → NaCl + SO2 ↑ + H2O 0,25đ 0,25đ 0,25đ 0,25đ 0,25đ 0,25đ 8 a, - Hòa tan 3 chất bột vào nước + Tan → CaO ( sp Ca(OH)2), P2O5 ( sp H3PO4) + Không tan → BaSO4 - Cho quỳ tím vào hai lọ còn lại: quỳ tím chuyển màu xanh ( CaO), chuyển màu đỏ ( P2O5) - PTHH: CaO + H2O → Ca(OH)2 P2O5 + H2O → H3PO4 0,25đ 0,25đ 0,25đ 0,25đ b, Ta có sơ đồ điều chế S → SO2 → SO3 → H2SO4 32 (g) 98(g) 1 tấn x tấn → x = 3,0625 tấn → m H2SO4 = ( 3,0625 . 100) : 98 = 3,125( tấn) Mà H = 80% → m H2SO4 thực tế là: 3,125 . 80% = 2,5 ( tấn 0,25đ 0,25đ 0,25đ 0,25đ 9 a. CO2 + Ca(OH)2 CaCO3 + H2O (1) Mol : 0,25 0,25 0,25 Đổi 100ml=0,1lit b. Từ pt (1) c. 2HCl + Ca(OH)2 CaCl2 + 2H2O (2) mol: 0,5 0,25 0,5 0,5 0,5 0,5 0,5 0,25 0,25 0,25 0,25 Xét duyệt của tổ chuyên môn Giáo viên Lê Thị Tuyết
Tài liệu đính kèm:
 Tiet_10_kiem_tra_1_tiet_Hoa_9.doc
Tiet_10_kiem_tra_1_tiet_Hoa_9.doc





