Kiểm tra chất lượng học kì II môn: Hóa học 9 trường THCS Nguyễn Bỉnh Khiêm
Bạn đang xem tài liệu "Kiểm tra chất lượng học kì II môn: Hóa học 9 trường THCS Nguyễn Bỉnh Khiêm", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
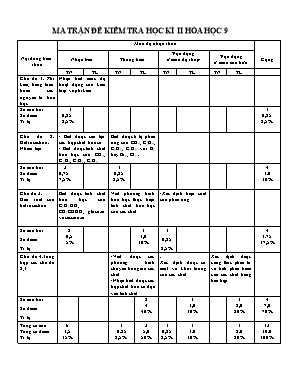
MA TRẬN ĐỀ KIỂM TRA HỌC KÌ II HÓA HỌC 9 Nội dung kiến thức Mức độ nhận thức Cộng Nhận biết Thông hiểu Vận dụng ở mức độ thấp Vận dụng ở mức cao hơn TN TL TN TL TN TL TN TL Chủ đề 1: Phi kim, bảng tuần hoàn các nguyên tố hóa học Nhận biết mức độ hoạt động của kim loại và phi kim Số câu hỏi Số điểm Tỉ lệ 1 0,25 2,5% 1 0,25 2,5% Chủ đề 2: Hidrocacbon. Nhiên liệu - Biết được cấu tạo các hợp chất hữu cơ - Biết được tính chất hóa học của CH4, C2H4, C2H2, C6H6 Biết được tỉ lệ phản ứng của CH4, C2H4, C2H2, C6H6 với O2 hay Br2, Cl2 Số câu hỏi Số điểm Tỉ lệ 3 0,75 7,5% 1 0,25 2,5% 4 1.0 10% Chủ đề 3: Dẫn xuất của hidrocacbon Biết được tính chất hóa học của C2H5OH, CH3COOH, glucozơ và saccarozơ Viết phương trình hóa học thực hiện tính chất hóa học của các chất -Xác định hiệu suất của phản ứng Số câu hỏi Số điểm Tỉ lệ 2 0,5 5% 1 1,0 10% 1 0,25 2,5% 4 1.75 17,5% Chủ đề 4:Tổng hợp: các chủ đề 2,3 -Viết được các phương trình chuyển hóa giữa các chất -Nhận biết được các hợp chất hữu cơ dựa vào tính chất . Xác định được số mol và khối lương của các chất Xác định được công thức phân tử và tính phần trăm của các chất trong hỗn hợp Số câu hỏi Số điểm Tỉ lệ 2 4 40% 1 1,0 10% 1 2,0 20% 4 7,0 70% Tổng số câu Tổng số điểm Tỉ lệ 6 1,5 15% 1 0.25 2,5% 3 5,0 50% 1 0,25 2,5% 1 1.0 10% 1 2.0 20% 13 10.0 100% TRƯỜNG THCS NGUYỄN BỈNH KHIÊM Lớp: 9/ Họ tên: SBD: KIỂM TRA CHẤT LƯỢNG HKII 2015-2016 MÔN: HÓA HỌC 9 THỜI GIAN: 45 phút (Không kể thời gian phát đề) Giám thị: ĐỀ 1 I.Trắc nghiệm: (2,0 điểm) Khoanh tròn vào chữ cái trước câu trả lời đúng. Câu 1: Cách sắp xếp nào sau đây đúng theo chiều tính phi kim tăng dần: A. P, S, Cl, F B. S, P, Cl, F C. Cl, F, S, P D. F, S, P, Cl Câu 2: Dãy các chất nào sau đây đều là những hydrocacbon? A. C2H5OH, CH4, C6H6 B. C4H10, C2H2, CH3COOH C. CH3Cl, C6H6, CH4 D. C4H10, C3H6, C2H2 Câu 3: Nhỏ một giọt dung dịch chất sau lên quì tím, quì tím chuyển thành màu đỏ. Dung dịch đó là A. glucozơ. B. rượu etylic C. saccarozơ D. axit axetic Câu 4: Chất nào sau đây làm mất màu dung dịch brôm? A. CH4 B. C6H6 C. C2H2 D. C2H5OH Câu 5: Công thức cấu tạo của benzen gồm có: A. Ba liên kết đôi B. Ba liên kết đơn C. Ba liên kết đôi xen kẽ ba liên kết đơn D. Ba liên kết đôi xen kẽ hai liên kết đơn Câu 6: Rượu etylic không tác dụng với chất nào sau đây? A. Na B. NaOH C. CH3COOH D. K Câu 7: Phương trình cháy của chất hữu cơ (X) là: 2X + 5O 2 4CO 2 + 2H 2 O. Công thức phân tử của (X) được xác định là: A. CH 4 B. C 2 H 4 C. C 2 H 2 D. C 6 H 6 . Câu 8: Cho 1 (mol) Na tác dụng với 1 (mol) C2H5OH nguyên chất thì có 0,4 (mol) khí H2 sinh ra. Hiệu suất của phản ứng là: A. 80% B. 70% C. 60% D. 50% II. Tự luận (8,0 điểm) Câu 1: (2,0 điểm) Hoàn thành sơ đồ chuyển hóa sau bằng cách viết các phương trình hóa học: C2H4 C2H5OHCH3COOH CH3COONa CH4 Câu 2: ( 2,0 điểm) Trình bày phương pháp để nhận biết các chất lỏng sau: rượu etylic, axit axetic, benzen, dung dịch glucozơ. Viết phương trình phản ứng (nếu có) Câu 3: ( 4,0 điểm) Cho 9,7 gam hỗn hợp X gồm axit axetic và axit A có công thức CmH2m+1COOH tác dụng với dung dịch NaOH 1M thì vừa hết 150 ml. a/ Xác định công thức phân tử của A. Biết tỉ lệ số mol của axit axetic và A trong hỗn hợp là 2: 1 b/ Tính thành phần % khối lượng của mỗi chất trong hỗn hợp X. (C = 12; H = 1; O = 16) TRƯỜNG THCS NGUYỄN BỈNH KHIÊM Lớp: 9/ Họ tên: SBD: KIỂM TRA CHẤT LƯỢNG HKII 2015-2016 MÔN: HÓA HỌC 9 THỜI GIAN: 45 phút (Không kể thời gian phát đề) Giám thị: ĐỀ 2 I.Trắc nghiệm: (2,0 điểm) Khoanh tròn vào chữ cái trước câu trả lời đúng. Câu 1: Cách sắp xếp nào sau đây đúng theo chiều tính kim loại giảm dần: A. Fe, Pb, Ni, Zn B. Zn, Fe, Ni, Pb C. Fe, Ni, Pb, Zn D. Pb, Ni, Fe, Zn Câu 2: Hợp chất nào sau đây không phải là hợp chất hữu cơ? A. CH4 B.C2H5ONa C. NaHCO3 D. C3H9N Câu 3: Cho Na dư vào dung dịch rượu etylic 450, xảy ra bao nhiêu phản ứng? A. 2. B. 1 C. 3 D. Không phản ứng Câu 4: Chất nào sau đây làm mất màu dung dịch brôm? A. C2H6 B. C6H6 C. CH4 D. C2H4 Câu 5: Công thức cấu tạo của benzen gồm có: A. Ba liên kết đôi xen kẽ ba liên kết đơn B. Ba liên kết đơn nằm liền kề nhau C. Ba liên kết đôi D. Ba liên kết đôi xen kẽ hai liên kết đơn Câu 6: Axit axetic không tác dụng với chất nào sau đây? A. Na B. Cu C. C2H5OH D. NaOH Câu 7: Phương trình cháy của chất hữu cơ (X) là: X + 2O 2 CO 2 + 2H 2 O. Công thức phân tử của (X) được xác định là: A. C 2 H 4 B. C 2 H 2 C. CH 4 D. C 6 H 6 . Câu 8: Cho 1 (mol) Na vào rượu C2H5OH nguyên chất ( dư). Thể tích khí H2 (đktc) sinh ra là 6,72 (l). Hiệu suất của phản ứng là: A. 50% B. 60% C. 70% D. 80% II. Tự luận (8,0 điểm) Câu 1: (2,0 điểm) Hoàn thành sơ đồ chuyển hóa sau: GlucozơC2H5OH CH3COOC2H5 CH3COONa CH4 Câu 2: ( 2,0 điểm) Trình bày phương pháp để nhận biết các chất lỏng sau: rượu etylic, axit axetic, etylaxetat, dung dịch glucozơ Câu 3: ( 4,0 điểm) Cho hỗn hợp gồm rượu etylic và rượu X có công thức CnH2n+1OH. Nếu cho 14,2 gam hỗn hợp này tác dụng hết với Na thấy thoát ra 4,48 lít H2 (đktc). Biết tỉ lệ số mol của rượu etylic và rượu X trong hỗn hợp là 1: 3. a/ Xác định công thức phân tử của rượu X b/ Tính thành phần % khối lượng của mỗi rượu trong hỗn hợp. (C = 12; H = 1; O = 16) ĐÁP ÁN VÀ HƯỚNG DẪN CHẤM ĐỀ 1 CÂU NỘI DUNG BIỂU ĐIỂM I. TRẮC NGHIỆM Câu 1 2 3 4 5 6 7 8 Đáp án A D D C C B C A 0,25 x 8= 2 đ II. TỰ LUẬN Câu 1 C2H4 + H2O C2H5OH C2H5OH + O2 CH3COOH + H2O CH3COOH + NaOH CH3COONa + H2O CH3COONa + NaOH CH4 + Na2CO3 Nếu không ghi điều kiện mỗi câu đạt 0,25 điểm 0,5 x 4 = 2 đ Câu 2 + Lấy mỗi chất một ít để làm mẫu thử + Nhúng quỳ tím vào các mẫu thử, nếu quỳ tím hóa đỏ là axit axetic. + Cho dung dịch Ag2O/dd NH3 vào ba mẫu thử còn lại, nếu xuất hiện kết tủa Ag là glucozơ. + Cho Na vào hai mẫu thử còn lại, nếu có khí thoát ra là rượu etylic,; còn lại là benzen. PT: + C6H12O6 + Ag2O C6H12O7 + 2Ag + 2C2H5OH + 2Na 2C2H5ONa + H2 ( Học sinh có thể làm cách khác đúng vẫn đạt điểm tồi đa) 0,25 đ 0,25 đ 0,25 đ 0,25 đ 0,5 đ 0,5 đ Câu 3 a/ + Gọi số mol của CH3COOH là 2x Vậy số mol của CmH2m + 1COOH trong hỗn hợp là x PTHH: + CH3COOH + NaOH CH3COONa + H2O 2x 2x + CmH2m + 1COOH + NaOH CmH2m+1COONa + H2O x x + nNaOH = 2x + x = 0,15 x 1 = 0,15 x = 0,05 mol + m= 0,1 X 60 = 6 (g); m= 9,7 – 6 = 3,7 (g) + Ta có: mA = nA x MA = 0,05 x ( 14m + 46) = 3,7 m = 2 Vậy công thức của axit cần tìm là: C2H5COOH b/ Phần trăm khối lượng của các chất: %m= x 100% = 61,86% %m= 100% - 61,86% = 38,14% Học sinh giải cách khác đúng vẫn đạt điểm tối đa 0,5 đ 0,5 đ 0,5 đ 0,5 đ 0,5 đ 0,5 đ 0,5 đ 0,5 đ Tổng 10,0 đ ĐÁP ÁN VÀ HƯỚNG DẪN CHẤM ĐỀ 2 CÂU NỘI DUNG BIỂU ĐIỂM I. TRẮC NGHIỆM Câu 1 2 3 4 5 6 7 8 Đáp án B C A D A B C B 0,25 x 8= 2 đ II. TỰ LUẬN Câu 1 (1) C6H12O6 2C2H5OH + 2CO2 C2H5OH + CH3COOH CH3COOC2H5 + H2O CH3COOC2H5 + NaOH CH3COONa + C2H5OH CH3COONa + NaOH CH4 + Na2CO3 Nếu không ghi điều kiện mỗi câu đạt 0,25 điểm 0,5 x 4 = 2 đ Câu 2 + Lấy mỗi chất một ít để làm mẫu thử + Nhúng quỳ tím vào các mẫu thử, nếu quỳ tím hóa đỏ là axit axetic. + Cho dung dịch Ag2O/dd NH3 vào ba mẫu thử còn lại, nếu xuất hiện kết tủa Ag là glucozơ. + Cho Na vào hai mẫu thử còn lại, nếu có khí thoát ra là rượu etylic, còn lại là etyl axetat PT: + C6H12O6 + Ag2O C6H12O7 + 2Ag + 2C2H5OH + 2Na 2C2H5ONa + H2 ( Học sinh có thể làm cách khác đúng vẫn đạt điểm tồi đa) 0,25 đ 0,25 đ 0,25 đ 0,25 đ 0,5 đ 0,5 đ Câu 3 a/ + Gọi số mol của C2H5OH là x Vậy số mol của CnH2n + 1OH trong hỗn hợp là 3x PTHH: + 2C2H5OH + 2Na 2C2H5ONa + H2 x 0,5x + 2CnH2n + 1OH + 2Na 2CnH2n+1ONa + H2 3x 1,5x + Ta có: n = 0,5x + 1,5x = = 0,2 x = 0,1 mol + m= 46 x 0,1 = 4,6 (g); m= 14,2 – 4,6 = 9,6 (g) + Ta có: mX = nX. MX = 3 x 0,1 x (14n + 18) = 9,6 n = 1 Vậy công thức của axit cần tìm là: CH3OH b/ Phần trăm khối lượng của các chất: %m= x 100% = 32,39% %m= 100% - 32,39% = 67,61% Học sinh giải cách khác đúng vẫn đạt điểm tối đa 0,5 đ 0,5 đ 0,5 đ 0,5 đ 0,5 đ 0,5 đ 0,5 đ 0,5 đ Tổng 10,0 đ ĐỀ CƯƠNG ÔN THI KÌ 2 MÔN HÓA LỚP 9 Năm học: 2013- 2014 Phần I: Lí thuyết 1. Sơ lược về bảng tuần hoàn các nguyên tố hóa học ( chú ý mức độ hoạt động của kim loại và phi kim) 2. Khái niệm, cấu tạo phân tử hợp chất hữu cơ. 3. Tính chất hóa học, cấu tạo phân tử, điều chế và ứng dụng của metan, etilen, axetilen và benzen. 4. Tính chất hóa học, điều chế và ứng dụng của rượu etylic, axit axetic. 5. Mối liên hệ giữa etilen, rượu etylic và axit axetic. 6. Tính chất hóa học và thành phần cấu tạo của chất béo. 7. Tính chất và ứng dụng của glucozơ và saccarozơ. Phần II: Bài tập vận dụng A/ Nhận biết: Nhận biết các chất sau( nguyên chất hay dạng lỏng) Rượu etylic, axit axetic, ben zen, glucozơ Axit axetic, rượu etylic, etylaxetat Glucozơ, benzen, nước, axit axetic Rượu etylic, axit axetic, benzen bằng phương pháp hóa học Rượu etyli, axit axetic, benzen bằng nước và quỳ tím Metan, etilen, cacbonic, hiđrô Metan, etilen, cacbonic, oxi B/ Chuỗi phản ứng 1- . a. C ® CH4 ® CH3Cl ® CCl4 b. CH3COONa ® CH4 ® CO2 ® CaCO3 c. Al4C3 ® CH4 ® C2H2 2- a. C2H5OH CH3COOH CH3COONa b. C12H22O11 C6H12O6 C2H5OH C2H5ONa 3- a- Ñaù voâi voâi soáng ñaát ñeøn axetylen etylen P.E (5) b- Etilenrượu etylicaxit axetic etylaxetat natriaxetat kẽm axetat 4- GlucozơC2H5OH CH3COOC2H5 CH3COONa CH4 5- C2H4 C2H5OHCH3COOH CH3COONa CH4 C/ Bài toán: 1-Cho 10 gam hỗn hợp gồm rượu etylic và axit axetic tham gia phản ứng vừa đủ với 7,42 gam Na2CO3. Tính thành phần % khối lượng mỗi chất có trong hỗn hợp ban đầu 2- Hỗn hợp X gồm axit axetic và rượu etylic. Cho a gam hồn hợp X tác dụng vừa đủ với dung dịch NaOH 0,1M thì hết 200ml. Mặt khác cho a gam hỗn hợp X tác dụng hết với Na dư thấy thoát ra 0,336l khí H2 ( ĐKTC). a. Viết phương trình hóa học xảy ra. b. Hãy xác định a gam. 3-Cho một lượng rượu etylic phản ứng vừa đủ với kim loại kali sinh ra 8,96 lít khí hidro ở đktc. Tính thể tích rượu etylic đã dùng. Biết khối lượng riêng của rượu là 0,8(g/ml). 4-Cho hỗn hợp gồm rượu etylic và rượu X có công thức CnH2n+1OH. Nếu cho 14,2 gam hỗn hợp này tác dụng hết với Na thấy thoát ra 4,48 lít H2 (đktc). Biết tỉ lệ số mol của rượu etylic và rượu X trong hỗn hợp là 1: 3. a/ Xác định công thức phân tử của rượu X b/ Tính thành phần % khối lượng của mỗi rượu trong hỗn hợp. 5-Cho 9,7 gam hỗn hợp X gồm axit axetic và axit A có công thức CmH2m+1COOH tác dụng với dung dịch NaOH 1M thì vừa hết 150 ml. a/ Xác định công thức phân tử của A. Biết tỉ lệ số mol của axit axetic và A trong hỗn hợp là 2: 1 b/ Tính thành phần % khối lượng của mỗi chất trong hỗn hợp X. 6- Đốt cháy hoàn toàn m(g) hỗn hợp X gồm metan, axetilen và etilen thu được 39,6 gam CO2 và 14,4 gam H2O. Mặt khác cho 2,24 lít hỗn hợp X (đktc) đi từ từ qua nước brom dư thấy có 19,2 gam brom tham gia phản ứng. a. Tính m b. Tính thành phần % theo thể tích mỗi khí trong X. 7- Đốt cháy hoàn toàn 10,08 lít(đktc) hỗn hợp khí A gồm C2H4 và C2H2 rồi cho toàn bộ sản phẩm thu được hấp thụ hết vào bình chứa dung dịch Ca(OH)2 dư. Phản ứng xong thấy khối lượng bình chứa tăng thêm 50,4 gam và có a gam kết tủa. Xác định % theo thể tích của mỗi chất trong hỗn hợp khí A và tính a gam. 8- Đốt cháy hoàn toàn 3,7 gam chất hữu cơ A chúa C, H, O thu được 4,48 lit1khi1 CO2 (đktc) và 4,5 gam H2O. a. Xác định CTPT của A, biết phân tử khối hơi của A đối với H2 là 37 b. Viết CTCT có thể có của A, biết phân tử có nhóm –OH c. Viết phương trình phản ứng của A với Na 9- Tính khối lượng axit axetic chứa trong giấm ăn thu được khi cho lên men 25 lít rượu etylic 8o. Biết khối lượng riêng của rượu etylic là 0,8g/ml và hiệu suất lên men là 90%. 10- Cho 4,5kg glucozơ lên men. Hỏi thu được bao nhiêu lít rượu etylic nguyên chất và bao nhiêu lít CO2 (đktc), biết hiệu suất phản ứng lên men là 80% và khối lượng riêng của rượu là 0,8g/ml.
Tài liệu đính kèm:
 KIEM_TRA_HOC_KI_2.doc
KIEM_TRA_HOC_KI_2.doc





