Đề thi thử THPT Quốc gia lần I môn: Hóa học - Trường THCS-THPT Đông Du
Bạn đang xem 20 trang mẫu của tài liệu "Đề thi thử THPT Quốc gia lần I môn: Hóa học - Trường THCS-THPT Đông Du", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
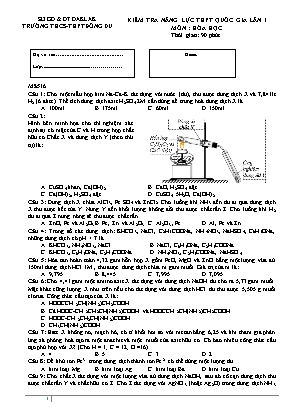
KIỂM TRA NĂNG LỰC THPT QUỐC GIA LẦN I MÔN : HÓA HỌC Thời gian: 90 phút Họ và tên: Lớp:.............................................................. Điểm: SỞ GD & ĐT ĐẮKLẮK TRƯỜNG THCS-THPT ĐÔNG DU Mã 516 Câu 1: Cho một mẫu hợp kim Na-Ca-K tác dụng với nước (dư), thu được dung dịch X và 7,84 lít H2 (ở đktc). Thể tích dung dịch axit H2SO4 2M cần dùng để trung hoà dung dịch X là A. 100ml. B. 175ml. C. 60ml. D. 150ml. Câu 2: Hình bên minh họa cho thí nghiệm xác định sự có mặt của C và H trong hợp chất hữu cơ.Chất X và dung dịch Y (theo thứ tự) là: A. CuSO4 khan, Ca(OH)2. B. CaO, H2SO4 đặc. C. Ca(OH)2, H2SO4 đặc. D. CuSO4.5H2O, Ca(OH)2. Câu 3: Dung dịch X chứa AlCl3, Fe SO4 và ZnCl2. Cho luồng khí NH3 đến dư đi qua dung dịch X thu được kết tủa Y. Nung Y đến khối lượng không đổi thu được chất rắn Z. Cho luồng khí H2 dư đi qua Z nung nóng sẽ thu được chất rắn A. ZnO, Fe và Al2O3 B. Fe, Zn và Al2O3 C. Al2O3 , Fe. D. Al, Fe và Zn Câu 4: Trong số các dung dịch: KHCO3, NaCl, C2H5COONa, NH4NO3, NaHSO4, C6H5ONa, những dung dịch có pH > 7 là A. KHCO3, NH4NO3, NaCl. B. NaCl, C6H5ONa, C2H5COONa. C. KHCO3, C6H5ONa, C2H5COONa. D. NH4NO3, C2H5COONa, NaHSO4. Câu 5: Hòa tan hoàn toàn 4,32 gam hỗn hợp X gồm FeO, MgO và ZnO bằng một lượng vừa đủ 150ml dung dịch HCl 1M , thu được dung dịch chứa m gam muối. Giá trị của m là: A. 9,795. B. 8,445. C. 7,995. D. 7,095. Câu 6: Cho 4,41 gam một amino axit X tác dụng với dung dịch NaOH dư cho ra 5,73 gam muối. Mặt khác cũng lượng X như trên nếu cho tác dụng với dung dịch HCl dư thu được 5,505 g muối clorua. Công thức cấu tạo của X là: A. HOOCCH2CH(NH2)CH2COOH. B. Cả HOOC-CH2CH2CH(NH2)COOH và HOOCCH2CH(NH2)CH2COOH C. HOOC-CH2CH2CH(NH2)COOH. D. CH3CH(NH2)COOH. Câu 7: Este X không no, mạch hở, có tỉ khối hơi so với metan bằng 6,25 và khi tham gia phản ứng xà phòng hoá tạo ra một anđehit và một muối của axit hữu cơ. Có bao nhiêu công thức cấu tạo phù hợp với X? (Cho H = 1; C = 12; O =16) A. 4. B. 5. C. 3. D. 2. Câu 8: Để khử ion Fe3+ trong dung dịch thành ion Fe2+ có thể dùng một lượng dư A. kim loại Mg. B. kim loại Ag. C. kim loại Ba. D. kim loại Cu. Câu 9: Cho chất X tác dụng với một lượng vừa đủ dung dịch NaOH, sau đó cô cạn dung dịch thu được chất rắn Y và chất hữu cơ Z. Cho Z tác dụng với AgNO3 (hoặc Ag2O) trong dung dịch NH3 thu được chất hữu cơ T. Cho chất T tác dụng với dung dịch NaOH thu được chất M. M có nhiều hơn Y một nguyên tử cacbon. Chất X có thể là: A. CH3COOC(CH)3=CH2. B. HCOOCH3. C. CH3COOCH=CH2. D. HCOOCH=CH2. Câu 10: Trong số các loại tơ sau: tơ tằm, tơ visco, tơ nilon-6,6, tơ axetat, tơ capron, tơ enang, những loại tơ nào thuộc loại tơ nhân tạo? A. Tơ visco và tơ axetat. B. Tơ visco và tơ nilon-6,6. C. Tơ nilon-6,6 và tơ capron. D. Tơ tằm và tơ enang. Câu 11: Đun 6 gam axit axetic với 6,9 gam etanol (có H2SO4 đặc làm xúc tác) đến khi phản ứng đạt tới trạng thái cân bằng, thu được m gam este (biết hiệu suất của phản ứng este hoá là 75%). Giá trị của m gam là (Cho H = 1; C = 12; O = 16) A. 8,8. B. 6,6. C. 9,9 D. 13,2. Câu 12: Polime dùng để chế tạo thuỷ tinh hữu cơ (plexiglas) được điều chế bằng phản ứng trùng hợp A. CH2=C(CH3)COOCH3. B. CH2 =CHCOOCH3. C. C6H5CH=CH2. D. CH3COOCH=CH2. Câu 13: Đốt cháy hoàn toàn hỗn hợp M gồm một ankan X và một ankin Y, thu được số mol CO2 bằng số mol H2O. Thành phần phần trăm về số mol của X và Y trong hỗn hợp M lần lượt là A. 20%; 80%. B. 50%; 50%. C. 35%; 65%. D. 75%; 25%. Câu 14: Cho 0,1 mol α-amino axit dạng H2NRCOOH (X) phản ứng hết với HCl tạo 12,55g muối. X là A. Phenylalanin B. Valin C. Glixin D. Alanin Câu 15: Cho sơ đồ chuyển hoá: Glucozơ ® X ® Y ® CH3COOH. Hai chất X, Y lần lượt là A. CH3CH(OH)COOH và CH3CHO. B. CH3CH2OH và CH2=CH2. C. CH3CHO và CH3CH2OH. D. CH3CH2OH và CH3CHO. Câu 16: Cho các nguyên tố M (Z = 11), X (Z = 17), Y (Z = 9) và R (Z = 19). Bán kình của các nguyên tố tăng dần theo thứ tự A. Y < X < M < R. B. M < X < R < Y. C. M < X < Y < R. D. Y < M < X < R. Câu 17: Cho 4,48 lít khí CO (ở đktc) từ từ đi qua ống sứ nung nóng đựng 8 gam một oxit sắt đến khi phản ứng xảy ra hoàn toàn. Khí thu được sau phản ứng có tỉ khối so với hiđro bằng 20. Công thức của oxit sắt và phần trăm thể tích của khí CO2 trong hỗn hợp khí sau phản ứng là: A. Fe2O3; 65%. B. Fe3O4; 75%. C. FeO; 75%. D. Fe2O3; 75%. Câu 18: Thứ tự một số cặp oxi hoá - khử trong dãy điện hoá như sau: Fe2+/Fe; Cu2+/Cu; Fe3+/Fe2+ , Ag+/Ag Cặp chất không phản ứng với nhau là A. Fe và dung dịch CuCl2. B. dung dịch Fe(NO3)3 và dung dịch AgNO3. C. Fe và dung dịch FeCl3. D. Cu và dung dịch AgNO3. Câu 19: Cho sơ đồ chuyển hoá: FeFeCl3Fe(OH)3 (mỗi mũi tên ứng với một phản ứng). Hai chất X, Y lần lượt là A. HCl, NaOH. B. Cl2, NaOH. C. NaCl, Cu(OH)2. D. HCl, Al(OH)3. Câu 20: Cho 5,6 gam một anđehit phản ứng hoàn toàn với lượng dư AgNO3 (hoặc Ag2O) trong dung dịch NH3 thu được m gam Ag. Nếu lấy m gam Ag này cho tác dụng vừa đủ với một lượng HNO3 đặc thì sau phản ứng thu được 4,48 lít khí (là sản phẩm khử duy nhất, ở đktc). Công thức cấu tạo thu gọn của anđehit là: A. CH2=CH-CHO. B. CH3CHO. C. OHC-CHO. D. HCHO. Câu 21: Cho 150ml dung dịch matozơ chưa rõ nồng độ tác dụng với một lượng dư AgNO3 (hoặc Ag2O) trong dung dịch NH3 thu được 12,96 gam bạc kết tủa. Nồng độ mol (hoặc mol/l) của dung dịch matozơ đã dùng là: A. 0,80M. B. 0,40M. C. 0,20M. D. 0,10M. Câu 22: Cho X, Y là hai chất thuộc dãy đồng đẳng của axit acrylic và MX < MY; Z là ancol có cùng số nguyên tử cacbon với X; T là este hai chức tạo bở X, Y và Z. Đốt cháy hoàn toàn 11,16 gam hỗn hợp E gồm X, Y, Z, T cần vừa đủ 13,216 lít khí O2 (đktc), thu được khí CO2 và 9,36 gam H2O. Mặt khác, 11,16 gam E tác dụng tối đa với dung dịch chứa 0,04 mol Br2. Khối lượng muối thu được khi cho lượng E trên tác dụng hết ới dung dịch KOH dư là: A. 4,68 gam. B. 5,04 gam. C. 5,80 gam. D. 5,44 gam. Câu 23: Sục CO2 vào dung dịch hỗn hợp gồm Ca(OH)2 và KOH ta quan sát hiện tượng theo đồ thị hình bên (số liệu tính theo đơn vị mol). Giá trị của x là: A. 0,13. B. 0,11. C. 0,12. D. 0,10. Câu 24: Cho các ion kim loại: Zn2+, Sn2+, Ni2+, Fe2+, Pb2+. Thứ tự tính oxi hoá giảm dần là A. Zn2+ > Sn2+ > Ni2+ > Fe2+ > Pb2+. B. Sn2+ > Ni2+ > Zn2+ > Pb2+ > Fe2+. C. Pb2+ > Sn2+ > Ni2+ > Fe2+ > Zn2+. D. Pb2+ > Sn2+ > Fe2+ > Ni2+ > Zn2+. Câu 25: Chỉ dùng Cu(OH)2 có thể phân biệt được tất cả các dung dịch riêng biệt sau: A. saccarozơ, glixerol, anđehit axetic, rượu (ancol) etylic. B. lòng trắng trứng, glucozơ, fructozơ, glixerol. C. glucozơ, mantozơ, glixerol, anđehit axetic. D. glucozơ, lòng trắng trứng, glixerol, rượu (ancol) etylic. Câu 26: Cho các cặp kim loại nguyên chất tiếp xúc trực tiếp với nhau: Fe và Pb; Fe và Zn; Fe và Sn; Fe và Ni. Khi nhúng các cặp kim loại trên vào dung dịch axit, số cặp kim loại trong đó Fe bị phá huỷ trước là A. 4. B. 1. C. 3. D. 2. Câu 27: Cho hỗn hợp X gồm Mg và Fe vào dung dịch axit H2SO4 đặc, nóng đến khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y và một phần Fe không tan. Chất tan có trong dung dịch Y là A. MgSO4. B. MgSO4, Fe2(SO4)3 và FeSO4. C. MgSO4 và Fe2(SO4)3. D. MgSO4 và FeSO4. Câu 28: Các hợp chất trong dãy chất nào dưới đây đều có tính lưỡng tính? A. Cr(OH)3, Pb(OH)2, Mg(OH)2. B. Cr(OH)3, Zn(OH)2, Mg(OH)2. C. Cr(OH)3, Zn(OH)2, Pb(OH)2. D. Cr(OH)3, Fe(OH)2, Mg(OH)2. Câu 29: Một dung dịch chứa x mol Mg2+, y mol Na+, 0,02 mol Cl– và 0,025 mol SO42–. Tổng khối lượng các muối tan có trong dung dịch là 4,28 gam. Giá trị của x và y lần lượt là: A. 0,02 và 0,03. B. 0,02 và 0,05. C. 0,015 và 0,04. D. 0,03 và 0,01. Câu 30: Để khử ion Cu2+ trong dung dịch CuSO4 có thể dùng kim loại A. Li. B. Ba. C. Sr. D. Zn. Câu 31: Một bình kín chứa hỗn hợp X gồm 0,195 mol H2; 0,15 mol axetilen; 0,12 mol vinyl axetilen và một ít bột Ni. Nung nóng bình một thời gian, thu được hỗn hợp khí Y có tỉ khối so với H2 là 19,5. Khí Y phản ứng vừa đủ với 0,21 mol AgNO3 trong NH3 thu được m gam kết tủa và 3,024 lít hỗn hợp khí Z ở đktc. Khí Z phản ứng tối đa với 0,165 mol Br2 trong dung dịch. Giá trị của m là: A. 55,2. B. 52,5. C. 27,6. D. 82,8. Câu 32: Hòa tan 11,6 gam hỗn hợp A gồm Fe và Cu vào 87,5 gam dung dịch HNO3 50,4%, sau khi kim loại tan hết thu được dung dịch X và V lít hỗn hợp khí B (gồm hai chất khí có tỉ lệ mol 3 : 2). Cho 500 ml dung dịch KOH 1M vào đ X thu được kết tủa Y và dung dịch Z. Lọc lấy Y rồi nung trong không khí đến khối lượng không đổi thu được 16,0 gam chất rắn. Cô cạn dung dịch Z thu được chất rắn T. Nung T đến khối lượng không đổi thu được 41,05 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Nồng độ % của Fe(NO3)3 trong X là: A. 20,02%. B. 40,69%. C. 13,56%. D. 12,3%. Câu 33: Cho các phát biểu sau: (1) Andehit vừa có tính oxi hóa vừa có tính khử. (2) Phenol tham gia phản ứng thế brom khó hơn benzene. (3) Amin bậc 2 có lực bazơ mạnh hơn amin bậc 1. (5) Phenol có tính axit nên dung dịch phenol trong nước làm quỳ tím hóa đỏ. (5) Chỉ dung dịch KMnO4 có thể phân biệt được toluene, benzene và stiren. (6) Trong công nghiệp, axeton và phenol được sản xuất từ cumen. (7) Trong y học, glucozơ được dùng làm thuốc tăng lực. (8) Để khử mùi tanh của các người ta thường dùng dung dịch giấm ăn. Số phát biểu đúng là: A. 4. B. 5. C. 6. D. 3. Câu 34: Hidrat hóa hỗn hợp gồm etilen và propilen có tỉ lệ mol 1 : 3 khi có mặt axit H2SO4 loãng thu được hỗn hợp ancol X. Lấy m gam hỗn hợp ancol X tác dụng hết với Na thấy bay ra 448 ml khí ở đktc. Oxi hóa m gam hỗn hợp ancol X bằng oxi không khí ở nhiệt độ cao có Cu xúc tác được hỗn hợp sản phẩn Y. Cho Y tác dụng với AgNO3 trong NH3 dư thu được 2,808 gam bạc kim loại. Phần trăm số mol propan-1-ol trong hỗn hợp là: A. 25%. B. 75%. C. 7,5%. D. 12,5%. Câu 35: Cho từ từ, đồng thời khuấy đều 300 ml dung dịch hỗn hợp gồm NaHCO3 0,1M và K2CÔ3 0,2M vào 100 ml dung dịch hỗn hợp gồm HCl 0,2M và NaHSO4 0,6M thu được V lít khí CO2 ở đktc và dung dịch X. Thêm vào dung dịch X 100 ml dung dịch hỗn hợp gồm KOH 0,6M và BaCl2 1,5M thu được m gam kết tủa. Giá trị của m là: A. 22,254. B. 17,73. C. 8,274. D. 31,71. Câu 36: Có phản ứng hoá học xảy ra như sau: H2S + 4Cl2 + 4H2O -> H2SO4 + 8 HCl Câu nào diễn tả đúng tính chất các chất phản ứng? A. H2S là chất khử, H2O là chất oxi hoá B. Cl2 là chất oxi hoá. H2O là chất khử C. H2S là chất oxi hoá, Cl2 là chất khử D. Cl2 là chất oxi hoá. H2S là chất khử. Câu 37: Khi cho 41,4 gam hỗn hợp X gồm Fe2O3, Cr2O3 và Al2O3 tác dụng với dung dịch NaOH đặc (dư), sau phản ứng thu được chất rắn có khối lượng 16 gam. Để khử hoàn toàn 41,4 gam X bằng phản ứng nhiệt nhôm, phải dùng 10,8 gam Al. Thành phần phần trăm theo khối lượng của Cr2O3 trong hỗn hợp X là (Cho: hiệu suất của các phản ứng là 100%; O = 16; Al = 27; Cr = 52; Fe = 56) A. 66,67%. B. 20,33%. C. 50,67%. D. 36,71%. Câu 38: Cho phương trình hoá học của phản ứng tổng hợp amoniac N2 (k) + 3H2 (k) 2NH3 (k) Khi tăng nồng độ của nitơ lên 2 lần, nồng độ của hiđro không đổi thì tốc độ phản ứng thuận A. giảm đi 2 lần. B. tăng lên 6 lần. C. tăng lên 2 lần. D. tăng lên 8 lần. Câu 39: Peptit A có phân tử khối nhỏ hơn 300. Trong A có 43,64% C; 6,18% H; 34,91% O và 15,27% N. Thủy phân hoàn toàn 2,75 gam A trong dung dịch axit vô cơ thu được 3,11 gam hỗn hợp các amino axit trong đó có amino axit Z là hợp chất phổ biến nhất trong protein của các loại hạt ngũ cốc, trong y học được sử dụng trong việc hỗ trợ chức năng thần kinh, muối mononatri của Z dùng làm bột ngọt (mì chính)Phát biểu nào sau đây không đúng về A? A. Tổng số nguyên tử H và N bằng 2 lần số nguyên tử C. B. Tác dụng với NaOH theo tỉ lệ mol 1 : 3. C. Có ít nhất 1 gốc Gly. D. Có 6 công thức cấu tạo thỏa mãn. Câu 40: Đốt cháy hoàn toàn một rượu (ancol) X thu được CO2 và H2O có tỉ lệ số mol tương ứng là 3 : 4. Thể tích khí CO2 thu được khi đốt cháy X bằng 0,75 lần thể tích oxi cần dùng để đốt (ở cùng điều kiện). Công thức phân tử của X là: A. C3H8O2. B. C3H4O. C. C3H8O3 D. C3H8O. Câu 41: Trong tự nhiên, nguyên tố brom có 2 đồng vị là Br và Br. Nếu nguyên tử khối trung bình là brom là 79,91 thì phần trăm của 2 đồng vị này lần lượt là A. 54,5% và 45,5% B. 35% và 65% C. 45,5% và 54,5% D. 61,8% và 38,2% Câu 42: Dãy gồm các ion cùng tồn tại trong một dung dịch là A. Ca2+,Cl-,Na+,CO32- B. Na+ ,K+,OH-,HCO3- C. Al3+,PO43-,Cl-, Ba2+ D. K+,Ba2+,OH-,Cl- Câu 43: Cho các chất có công thức cấu tạo như sau: HOCH2-CH2OH (X); HOCH2-CH2-CH2OH (Y); HOCH2-CHOH-CH2OH (Z); CH3-CH2-O-CH2-CH3 (R); CH3-CHOH-CH2OH (T). Những chất tác dụng được với Cu(OH)2 tạo thành dung dịch màu xanh lam là A. X, Y, R, T. B. X, Z, T. C. Z, R, T. D. X, Y, Z, T. Câu 44: Hòa tan hoàn toàn 19,2 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 trong 250 ml dung dịch H2SO4 3,6M (đặc, nóng, dư) thu được dung dịch Y và V lít khí SO2 ở đktc (sản phẩm khử duy nhất). Cho 450 ml dung dịch NaOH 2M vào dung dịch Y thu được 21,4 gam kết tủa. Giá trị của V là: A. 5,60. B. 4,48. C. 6,72. D. 3,36. Câu 45: Cho x gam hỗn hợp X gồm 2 chất hữu cơ có công thức phân tử C2H8O3N2 và C4H12O4N2 đều no mạch hở tác dụng với dung dịch NaOH vừa đủ thu được 5,6 lít hỗn hợp khí Y gồm 2 chất hữu cơ đều làm xanh quỳ tím ẩm có tỉ khối so với H2 bằng 19,7 và dung dịch Z có chứa m gam hỗn hợp 3 muối. Giá trị của m là: A. 27,45. B. 19,55. C. 29,25. D. 25,65. Câu 46: Polivinyl axetat (hoặc poli(vinyl axetat)) là polime được điều chế bằng phản ứng trùng hợp A. CH2=CH-COO-C2H5. B. C2H5COO-CH=CH2. C. CH2=CH-COO-CH3. D. CH3COO-CH=CH2. Câu 47: Dự án luyện nhôm Đắk Nông là dự án luyện nhôm đầu tiên của Việt Nam và do một doanh nghiệp tư nhân trong nước trực tiếp đầu tư nên có vai trò rất quan trọng không chỉ với sự phát triển kinh tế, xã hội của tỉnh Đắk Nông, mà còn với cả nước nói chung. Hãy cho biết nguyên liệu chính dùng để sản xuất nhôm là nguyên liệu nào sau đây A. quặng boxit. B. quặng manhetit. C. quặng pirit. D. quặng đôlômit. Câu 48: Khi thực hiện phản ứng tách nước đối với rượu (ancol) X, chỉ thu được một anken duy nhất. Oxi hoá hoàn toàn một lượng chất X thu được 5,6 lít CO2 (ở đktc) và 5,4 gam nước. Có bao nhiêu công thức cấu tạo phù hợp với X? (Cho H = 1; C = 12; O = 16) A. 3. B. 2. C. 4. D. 5. Câu 49: Khi điện phân NaCl nóng chảy (điện cực trơ), tại catôt xảy ra: A. sự khử ion Cl-. B. sự khử ion Na+ C. sự oxi hoá ion Na+. D. sự oxi hoá ion Cl-. Câu 50: Hòa tan m gam Mg trong 500 ml dung dịch chưa hỗn hợp gồm H2SO4 0,4M và Cu(NO3)2 đến phản ứng hoàn toàn thu được 1,12 lít hỗn hợp khí X ở đktc có tỉ khối của X so với H2 là 6,2 gồm N2 và H2, dung dịch Y và 2 gam hỗn hợp kim loại. Giá trị m là: A. 6,68. B. 5,48. C. 5,08. D. 4,68. ----------- HẾT ---------- Cho biết khối lượng nguyên tử (theo u) của các nguyên tố: H = 1; Li = 7; Be =9; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; P = 31; S = 32; Cl = 35,5; K = 39; Ca = 40; Cr=52; Fe = 56; Cu = 64; Zn = 65; As = 75; Br = 80; Rb = 85,5; Ag = 108; I=127; Ba = 137. Mã 022 Câu 1: Trong số các loại tơ sau: tơ tằm, tơ visco, tơ nilon-6,6, tơ axetat, tơ capron, tơ enang, những loại tơ nào thuộc loại tơ nhân tạo? A. Tơ visco và tơ nilon-6,6. B. Tơ nilon-6,6 và tơ capron. C. Tơ tằm và tơ enang. D. Tơ visco và tơ axetat. Câu 2: Trong số các dung dịch: KHCO3, NaCl, C2H5COONa, NH4NO3, NaHSO4, C6H5ONa, những dung dịch có pH > 7 là A. NaCl, C6H5ONa, C2H5COONa. B. KHCO3, C6H5ONa, C2H5COONa. C. NH4NO3, C2H5COONa, NaHSO4. D. KHCO3, NH4NO3, NaCl. Câu 3: Cho 4,48 lít khí CO (ở đktc) từ từ đi qua ống sứ nung nóng đựng 8 gam một oxit sắt đến khi phản ứng xảy ra hoàn toàn. Khí thu được sau phản ứng có tỉ khối so với hiđro bằng 20. Công thức của oxit sắt và phần trăm thể tích của khí CO2 trong hỗn hợp khí sau phản ứng là: A. FeO; 75%. B. Fe3O4; 75%. C. Fe2O3; 65%. D. Fe2O3; 75%. Câu 4: Cho 4,41 gam một amino axit X tác dụng với dung dịch NaOH dư cho ra 5,73 gam muối. Mặt khác cũng lượng X như trên nếu cho tác dụng với dung dịch HCl dư thu được 5,505 g muối clorua. Công thức cấu tạo của X là: A. HOOCCH2CH(NH2)CH2COOH. B. HOOC-CH2CH2CH(NH2)COOH. C. CH3CH(NH2)COOH. D. Cả HOOC-CH2CH2CH(NH2)COOH và HOOCCH2CH(NH2)CH2COOH Câu 5: Cho sơ đồ chuyển hoá: Glucozơ ® X ® Y ® CH3COOH. Hai chất X, Y lần lượt là A. CH3CH(OH)COOH và CH3CHO. B. CH3CH2OH và CH3CHO. C. CH3CH2OH và CH2=CH2. D. CH3CHO và CH3CH2OH. Câu 6: Hình bên minh họa cho thí nghiệm xác định sự có mặt của C và H trong hợp chất hữu cơ.Chất X và dung dịch Y (theo thứ tự) là: A. CuSO4 khan, Ca(OH)2. B. CuSO4.5H2O, Ca(OH)2. C. Ca(OH)2, H2SO4 đặc. D. CaO, H2SO4 đặc. Câu 7: Cho sơ đồ chuyển hoá: FeFeCl3Fe(OH)3 (mỗi mũi tên ứng với một phản ứng). Hai chất X, Y lần lượt là A. NaCl, Cu(OH)2. B. HCl, Al(OH)3. C. HCl, NaOH. D. Cl2, NaOH. Câu 8: Hòa tan hoàn toàn 4,32 gam hỗn hợp X gồm FeO, MgO và ZnO bằng một lượng vừa đủ 150ml dung dịch HCl 1M , thu được dung dịch chứa m gam muối. Giá trị của m là: A. 7,995. B. 8,445. C. 7,095. D. 9,795. Câu 9: Dung dịch X chứa AlCl3, Fe SO4 và ZnCl2. Cho luồng khí NH3 đến dư đi qua dung dịch X thu được kết tủa Y. Nung Y đến khối lượng không đổi thu được chất rắn Z. Cho luồng khí H2 dư đi qua Z nung nóng sẽ thu được chất rắn A. Fe, Zn và Al2O3 B. Al, Fe và Zn C. Al2O3 , Fe. D. ZnO, Fe và Al2O3 Câu 10: Cho chất X tác dụng với một lượng vừa đủ dung dịch NaOH, sau đó cô cạn dung dịch thu được chất rắn Y và chất hữu cơ Z. Cho Z tác dụng với AgNO3 (hoặc Ag2O) trong dung dịch NH3 thu được chất hữu cơ T. Cho chất T tác dụng với dung dịch NaOH thu được chất M. M có nhiều hơn Y một nguyên tử cacbon. Chất X có thể là: A. CH3COOCH=CH2. B. HCOOCH3. C. HCOOCH=CH2. D. CH3COOC(CH)3=CH2. Câu 11: Dãy gồm các ion cùng tồn tại trong một dung dịch là A. Ca2+,Cl-,Na+,CO32- B. K+,Ba2+,OH-,Cl- C. Al3+,PO43-,Cl-, Ba2+ D. Na+ ,K+,OH-,HCO3- Câu 12: Trong tự nhiên, nguyên tố brom có 2 đồng vị là Br và Br. Nếu nguyên tử khối trung bình là brom là 79,91 thì phần trăm của 2 đồng vị này lần lượt là A. 45,5% và 54,5% B. 35% và 65% C. 61,8% và 38,2% D. 54,5% và 45,5% Câu 13: Đốt cháy hoàn toàn hỗn hợp M gồm một ankan X và một ankin Y, thu được số mol CO2 bằng số mol H2O. Thành phần phần trăm về số mol của X và Y trong hỗn hợp M lần lượt là A. 35%; 65%. B. 75%; 25%. C. 50%; 50%. D. 20%; 80%. Câu 14: Đun 6 gam axit axetic với 6,9 gam etanol (có H2SO4 đặc làm xúc tác) đến khi phản ứng đạt tới trạng thái cân bằng, thu được m gam este (biết hiệu suất của phản ứng este hoá là 75%). Giá trị của m gam là (Cho H = 1; C = 12; O = 16) A. 8,8. B. 6,6. C. 13,2. D. 9,9 Câu 15: Cho các cặp kim loại nguyên chất tiếp xúc trực tiếp với nhau: Fe và Pb; Fe và Zn; Fe và Sn; Fe và Ni. Khi nhúng các cặp kim loại trên vào dung dịch axit, số cặp kim loại trong đó Fe bị phá huỷ trước là A. 4. B. 1. C. 3. D. 2. Câu 16: Dự án luyện nhôm Đắk Nông là dự án luyện nhôm đầu tiên của Việt Nam và do một doanh nghiệp tư nhân trong nước trực tiếp đầu tư nên có vai trò rất quan trọng không chỉ với sự phát triển kinh tế, xã hội của tỉnh Đắk Nông, mà còn với cả nước nói chung. Hãy cho biết nguyên liệu chính dùng để sản xuất nhôm là nguyên liệu nào sau đây A. quặng boxit. B. quặng đôlômit. C. quặng manhetit. D. quặng pirit. Câu 17: Cho X, Y là hai chất thuộc dãy đồng đẳng của axit acrylic và MX < MY; Z là ancol có cùng số nguyên tử cacbon với X; T là este hai chức tạo bở X, Y và Z. Đốt cháy hoàn toàn 11,16 gam hỗn hợp E gồm X, Y, Z, T cần vừa đủ 13,216 lít khí O2 (đktc), thu được khí CO2 và 9,36 gam H2O. Mặt khác, 11,16 gam E tác dụng tối đa với dung dịch chứa 0,04 mol Br2. Khối lượng muối thu được khi cho lượng E trên tác dụng hết ới dung dịch KOH dư là: A. 5,04 gam. B. 5,44 gam. C. 5,80 gam. D. 4,68 gam. Câu 18: Cho một mẫu hợp kim Na-Ca-K tác dụng với nước (dư), thu được dung dịch X và 7,84 lít H2 (ở đktc). Thể tích dung dịch axit H2SO4 2M cần dùng để trung hoà dung dịch X là A. 175ml. B. 100ml. C. 60ml. D. 150ml. Câu 19: Cho hỗn hợp X gồm Mg và Fe vào dung dịch axit H2SO4 đặc, nóng đến khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y và một phần Fe không tan. Chất tan có trong dung dịch Y là A. MgSO4 và Fe2(SO4)3. B. MgSO4 và FeSO4. C. MgSO4, Fe2(SO4)3 và FeSO4. D. MgSO4. Câu 20: Cho các nguyên tố M (Z = 11), X (Z = 17), Y (Z = 9) và R (Z = 19). Bán kình của các nguyên tố tăng dần theo thứ tự A. Y < M < X < R. B. Y < X < M < R. C. M < X < R < Y. D. M < X < Y < R. Câu 21: Để khử ion Cu2+ trong dung dịch CuSO4 có thể dùng kim loại A. Zn. B. Sr. C. Ba. D. Li. Câu 22: Hòa tan 11,6 gam hỗn hợp A gồm Fe và Cu vào 87,5 gam dung dịch HNO3 50,4%, sau khi kim loại tan hết thu được dung dịch X và V lít hỗn hợp khí B (gồm hai chất khí có tỉ lệ mol 3 : 2). Cho 500 ml dung dịch KOH 1M vào đ X thu được kết tủa Y và dung dịch Z. Lọc lấy Y rồi nung trong không khí đến khối lượng không đổi thu được 16,0 gam chất rắn. Cô cạn dung dịch Z thu được chất rắn T. Nung T đến khối lượng không đổi thu được 41,05 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Nồng độ % của Fe(NO3)3 trong X là: A. 20,02%. B. 13,56%. C. 12,3%. D. 40,69%. Câu 23: Chỉ dùng Cu(OH)2 có thể phân biệt được tất cả các dung dịch riêng biệt sau: A. glucozơ, lòng trắng trứng, glixerol, rượu (ancol) etylic. B. lòng trắng trứng, glucozơ, fructozơ, glixerol. C. saccarozơ, glixerol, anđehit axetic, rượu (ancol) etylic. D. glucozơ, mantozơ, glixerol, anđehit axetic. Câu 24: Các hợp chất trong dãy chất nào dưới đây đều có tính lưỡng tính? A. Cr(OH)3, Zn(OH)2, Pb(OH)2. B. Cr(OH)3, Fe(OH)2, Mg(OH)2. C. Cr(OH)3, Pb(OH)2, Mg(OH)2. D. Cr(OH)3, Zn(OH)2, Mg(OH)2. Câu 25: Một bình kín chứa hỗn hợp X gồm 0,195 mol H2; 0,15 mol axetilen; 0,12 mol vinyl axetilen và một ít bột Ni. Nung nóng bình một thời gian, thu được hỗn hợp khí Y có tỉ khối so với H2 là 19,5. Khí Y phản ứng vừa đủ với 0,21 mol AgNO3 trong NH3 thu được m gam kết tủa và 3,024 lít hỗn hợp khí Z ở đktc. Khí Z phản ứng tối đa với 0,165 mol Br2 trong dung dịch. Giá trị của m là: A. 82,8. B. 52,5. C. 55,2. D. 27,6. Câu 26: Cho 5,6 gam một anđehit phản ứng hoàn toàn với lượng dư AgNO3 (hoặc Ag2O) trong dung dịch NH3 thu được m gam Ag. Nếu lấy m gam Ag này cho tác dụng vừa đủ với một lượng HNO3 đặc thì sau phản ứng thu được 4,48 lít khí (là sản phẩm khử duy nhất, ở đktc). Công thức cấu tạo thu gọn của anđehit là: A. CH2=CH-CHO. B. HCHO. C. CH3CHO. D. OHC-CHO. Câu 27: Một dung dịch chứa x mol Mg2+, y mol Na+, 0,02 mol Cl– và 0,025 mol SO42–. Tổng khối lượng các muối tan có trong dung dịch là 4,28 gam. Giá trị của x và y lần lượt là: A. 0,02 và 0,03. B. 0,02 và 0,05. C. 0,03 và 0,01. D. 0,015 và 0,04. Câu 28: Este X không no, mạch hở, có tỉ khối hơi so với metan bằng 6,25 và khi tham gia phản ứng xà phòng hoá tạo ra một anđehit và một muối của axit hữu cơ. Có bao nhiêu công thức cấu tạo phù hợp với X? (Cho H = 1; C = 12; O =16) A. 3. B. 2. C. 4. D. 5. Câu 29: Sục CO2 vào dung dịch hỗn hợp gồm Ca(OH)2 và KOH ta quan sát hiện tượng theo đồ thị hình bên (số liệu tính theo đơn vị mol). Giá trị của x là: A. 0,12. B. 0,10. C. 0,11. D. 0,13. Câu 30: Cho 0,1 mol α-amino axit dạng H2NRCOOH (X) phản ứng hết với HCl tạo 12,55g muối. X là A. Alanin B. Phenylalanin C. Glixin D. Valin Câu 31: Khi cho 41,4 gam hỗn hợp X gồm Fe2O3, Cr2O3 và Al2O3 tác dụng với dung dịch NaOH đặc (dư), sau phản ứng thu được chất rắn có khối lượng 16 gam. Để khử hoàn toàn 41,4 gam X bằng phản ứng nhiệt nhôm, phải dùng 10,8 gam Al. Thành phần phần trăm theo khối lượng của Cr2O3 trong hỗn hợp X là (Cho: hiệu suất của các phản ứng là 100%; O = 16; Al = 27; Cr = 52; Fe = 56) A. 66,67%. B. 36,71%. C. 50,67%. D. 20,33%. Câu 32: Polivinyl axetat (hoặc poli(vinyl axetat)) là polime được điều chế bằng phản ứng trùng hợp A. C2H5COO-CH=CH2. B. CH3COO-CH=CH2. C. CH2=CH-COO-C2H5. D. CH2=CH-COO-CH3. Câu 33: Cho các chất có công thức cấu tạo như sau: HOCH2-CH2OH (X); HOCH2-CH2-CH2OH (Y); HOCH2-CHOH-CH2OH (Z); CH3-CH2-O-CH2-CH3 (R); CH3-CHOH-CH2OH (T). Những chất tác dụng được với Cu(OH)2 tạo thành dung dịch màu xanh lam là A. X, Y, Z, T. B. Z, R, T. C. X, Y, R, T. D. X, Z, T. Câu 34: Cho các ion kim loại: Zn2+, Sn2+, Ni2+, Fe2+, Pb2+. Thứ tự tính oxi hoá giảm dần là A. Pb2+ > Sn2+ > Ni2+ > Fe2+ > Zn2+. B. Zn2+ > Sn2+ > Ni2+ > Fe2+ > Pb2+. C. Pb2+ > Sn2+ > Fe2+ > Ni2+ > Zn2+. D. Sn2+ > Ni2+ > Zn2+ > Pb2+ > Fe2+. Câu 35: Cho 150ml dung dịch matozơ chưa rõ nồng độ tác dụng với một lượng dư AgNO3 (hoặc Ag2O) trong dung dịch NH3 thu được 12,96 gam bạc kết tủa. Nồng độ mol (hoặc mol/l) của dung dịch matozơ đã dùng là: A. 0,40M. B. 0,20M. C. 0,80M. D. 0,10M. Câu 36: Peptit A có phân tử khối nhỏ hơn 300. Trong A có 43,64% C; 6,18% H; 34,91% O và 15,27% N. Thủy phân hoàn toàn 2,75 gam A trong dung dịch axit vô cơ thu được 3,11 gam hỗn hợp các amino axit trong đó có amino axit Z là hợp chất phổ biến nhất trong protein của các loại hạt ngũ cốc, trong y học được sử dụng trong việc hỗ trợ chức năng thần kinh, muối mononatri của Z dùng làm bột ngọt (mì chính)Phát biểu nào sau đây không đúng về A? A. Có 6 công thức cấu tạo thỏa mãn. B. Tổng số nguyên tử H và N bằng 2 lần số nguyên tử C. C. Tác dụng với NaOH theo tỉ lệ mol 1 : 3. D. Có ít nhất 1 gốc Gly. Câu 37: Hòa tan m gam Mg trong 500 ml dung dịch chưa hỗn hợp gồm H2SO4 0,4M và Cu(NO3)2 đến phản ứng hoàn toàn thu được 1,12 lít hỗn hợp khí X ở đktc có tỉ khối của X so với H2 là 6,2 gồm N2 và H2, dung dịch Y và 2 gam hỗn hợp kim loại. Giá trị m là: A. 6,68. B. 5,08. C. 4,68. D. 5,48. Câu 38: Hòa tan hoàn toàn 19,2 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 trong 250 ml dung dịch H2SO4 3,6M (đặc, nóng, dư) thu được dung dịch Y và V lít khí SO2 ở đktc (sản phẩm khử duy nhất). Cho 450 ml dung dịch NaOH 2M vào dung dịch Y thu được 21,4 gam kết tủa. Giá trị của V là: A. 3,36. B. 5,60. C. 6,72. D. 4,48. Câu 39: Thứ tự một số cặp oxi hoá - khử trong dãy điện hoá như sau: Fe2+/Fe; Cu2+/Cu; Fe3+/Fe2+ , Ag+/Ag Cặp chất không phản ứng với nhau là A. Fe và dung dịch FeCl3. B. Cu và dung dịch AgNO3. C. Fe và dung dịch CuCl2. D. dung dịch Fe(NO3)3 và dung dịch AgNO3. Câu 40: Polime dùng để chế tạo thuỷ tinh hữu cơ (plexiglas) được điều chế bằng phản ứng trùng hợp A. CH2=C(CH3)COOCH3. B. C6H5CH=CH2. C. CH2 =CHCOOCH3. D. CH3COOCH=CH2. Câu 41: Khi thực hiện phản ứng tách nước đối với rượu (ancol) X, chỉ thu được một anken duy nhất. Oxi hoá hoàn toàn một lượng chất X thu được 5,6 lít CO2 (ở đktc) và 5,4 gam nước. Có bao nhiêu công thức cấu tạo phù hợp với X? (Cho H = 1; C = 12; O = 16) A. 4. B. 2. C. 3. D. 5. Câu 42: Có phản ứng hoá học xảy ra như sau: H2S + 4Cl2 + 4H2O -> H2SO4 + 8 HCl Câu nào diễn tả đúng tính chất các chất phản ứng? A. H2S là chất oxi hoá, Cl2 là chất khử B. H2S là chất khử, H2O là chất oxi hoá C. Cl2 là chất oxi hoá. H2O là chất khử D. Cl2 là chất oxi hoá. H2S là chất khử. Câu 43: Cho phương trình hoá học của phản ứng tổng hợp amoniac N2 (k) + 3H2 (k) 2NH3 (k) Khi tăng nồng độ của nitơ lên 2 lần, nồng độ của hiđro không đổi thì tốc độ phản ứng thuận A. tăng lên 6 lần. B. giảm đi 2 lần. C. tăng lên 2 lần. D. tăng lên 8 lần. Câu 44: Cho từ từ, đồng thời khuấy đều 300 ml dung dịch hỗn hợp gồm NaHCO3 0,1M và K2CÔ3 0,2M vào 100 ml dung dịch hỗn hợp gồm HCl 0,2M và NaHSO4 0,6M thu được V lít khí CO2 ở đktc và dung dịch X. Thêm vào dung dịch X 100 ml dung dịch hỗn hợp gồm KOH 0,6M và BaCl2 1,5M thu được m gam kết tủa. Giá trị của m là: A. 31,71. B. 17,73. C. 8,274. D. 22,254. Câu 45: Cho x gam hỗn hợp X gồm 2 chất hữu cơ có công thức phân tử C2H8O3N2 và C4H12O4N2 đều no mạch hở tác dụng với dung dịch NaOH vừa đủ thu được 5,6 lít hỗn hợp khí Y gồm 2 chất hữu cơ đều làm xanh quỳ tím ẩm có tỉ khối so với H2 bằng 19,7 và dung dịch Z có chứa m gam hỗn hợp 3 muối. Giá trị của m là: A. 19,55. B. 27,45. C. 29,25. D. 25,65. Câu 46: Hidrat hóa hỗn hợp gồm etilen và propilen có tỉ lệ mol 1 : 3 khi có mặt axit H2SO4 loãng thu được hỗn hợp ancol X. Lấy m gam hỗn hợp ancol X tác dụng hết với Na thấy bay ra 448 ml khí ở đktc. Oxi hóa m gam hỗn hợp ancol X bằng oxi không khí ở nhiệt độ cao có Cu xúc tác được hỗn hợp sản phẩn Y. Cho Y tác dụng với AgNO3 trong NH3 dư thu được 2,808 gam bạc kim loại. Phần trăm số mol propan-1-ol trong hỗn hợp là: A. 25%. B. 12,5%. C. 7,5%. D. 75%. Câu 47: Đốt cháy hoàn toàn một rượu (ancol) X thu được CO2 và H2O có tỉ lệ số mol tương ứng là 3 : 4. Thể tích khí CO2 thu được khi đốt cháy X bằng 0,75 lần thể tích oxi cần dùng để đốt (ở cùng điều kiện). Công thức phân tử của X là: A. C3H4O. B. C3H8O. C. C3H8O3 D. C3H8O2. Câu 48: Để khử ion Fe3+ trong dung dịch thành ion Fe2+ có thể dùng một lượng dư A. kim loại Cu. B. kim loại Mg. C. kim loại Ba. D. kim loại Ag. Câu 49: Cho các phát biểu sau: (1) Andehit vừa có tính oxi hóa vừa có tính khử. (2) Phenol tham gia phản ứng thế brom khó hơn benzene. (3) Amin bậc 2 có lực bazơ mạnh hơn amin bậc 1. (5) Phenol có tính axit nên dung dịch phenol trong nước làm quỳ tím hóa đỏ. (5) Chỉ dung dịch KMnO4 có thể phân biệt được toluene, benzene và stiren. (6) Trong công nghiệp, axeton và phenol được sản xuất từ cumen. (7) Trong y học, glucozơ được dùng làm thuốc tăng lực. (8) Để khử mùi tanh của các người ta thường dùng dung dịch giấm ăn. Số phát biểu đúng là: A. 6. B. 4. C. 5. D. 3. Câu 50: Khi điện phân NaCl nóng chảy (điện cực trơ), tại catôt xảy ra: A. sự khử ion Cl-. B. sự khử ion Na+ C. sự oxi hoá ion Cl-. D. sự oxi hoá ion Na+. ----------- HẾT ---------- Cho biết khối lượng nguyên tử (theo u) của các nguyên tố: H = 1; Li = 7; Be =9; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; P = 31; S = 32; Cl = 35,5; K = 39; Ca = 40; Cr=52; Fe = 56; Cu = 64; Zn = 65; As = 75; Br = 80; Rb = 85,5; Ag = 108; I=127; Ba = 137. Mã 815 Câu 1: Hình bên minh họa cho thí nghiệm xác định sự có mặt của C và H trong hợp chất hữu cơ.Chất X và dung dịch Y (theo thứ tự) là: A. CuSO4.5H2O, Ca(OH)2. B. CaO, H2SO4 đặc. C. CuSO4 khan, Ca(OH)2. D. C
Tài liệu đính kèm:
 DE_THI_THU_THPT_QUOC_GIA_2016_LAN_1.docx
DE_THI_THU_THPT_QUOC_GIA_2016_LAN_1.docx





