Đề thi tham khảo học kì II năm học 2015 - 2016 môn hóa học 9 thời gian làm bài : 60 phút (không kể thời gian phát đề)
Bạn đang xem tài liệu "Đề thi tham khảo học kì II năm học 2015 - 2016 môn hóa học 9 thời gian làm bài : 60 phút (không kể thời gian phát đề)", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
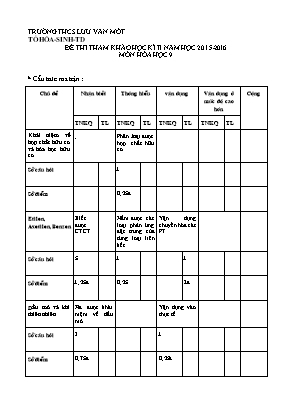
TRƯỜNG THCS LƯU VĂN MĨT TỔ HĨA-SINH-TD ĐỀ THI THAM KHẢO HỌC KÌ II NĂM HỌC 2015-2016 MƠN HĨA HỌC 9 * Cấu trúc ma trận : Chủ đề Nhận biết Thông hiểu vận dụng Vận dụng ở mức độ cao hơn Cộng TNKQ TL TNKQ TL TNKQ TL TNKQ TL Khái niệm về hợp chất hữu cơ và hĩa học hữu cơ . Phân loại được hợp chất hữu cơ Số câu hỏi 1 Số điểm 0,25đ Etilen, Axetilen,Benzen Biết được CTCT Nắm được các loại phản ứng đặc trưng của từng loại liên kết Vận dụng chuyển hĩa các PT Số câu hỏi 5 1 1 Số điểm 1,25đ 0,25 2đ Dầu mỏ và khí thiên nhiên Nêu được khái niệm về dầu mỏ Vận dụng vào thực tế Số câu hỏi 3 1 Số điểm 0,75đ 0,25đ Rượu etylic Tính chất vật lí Số câu hỏi 1 Số điểm 0,25đ 5. Kiến thức tổng hợp Dựa vào tính chất đặc trưng để nhận biết từng lọ riêng biệt Tính khối lượng của chất dựa vào phản ứng trên Tính khối lượng kết tủa dựa vào số mol và khối lượng Số câu hỏi 1 1 1 Số điểm 2đ 2đ 1,0 Tổng số câu (trắc nghiệm) TS điểm (trắc nghiệm) 9 2,25đ 2 0,5đ 1 0,25đ 12 câu 3đ Tổng số câu (tự luận) TS điểm (tự luận) 1 2đ 2 4đ c 1đ 3 câu 7đ Đề 1 TRƯỜNG THCS LƯU VĂN MĨT TỔ HĨA-SINH-TD ĐỀ THI THAM KHẢO HỌC KÌ II NĂM HỌC 2015-2016 MƠN HĨA HỌC 9 Thời gian làm bài :60 phút (khơng kể thời gian phát đề) A.PHẦN TRẮC NGHIỆM:(3điểm) Học sinh chọn câu đúng nhất ,mỗi câu 0,25đ Câu1 : Trong các dãy hợp chất sau đây, dãy nào gồm tồn loại hiđrocacbon ? A. CH4,C2H4,C2H5Cl B. C3H6,C4H10,C2H4 C.C2H4,CH4,C3H7 D.CH4,C2H4,CH3Cl Câu 2: Cơng thức nào là của Etilen? A. CH4 B. C2H2 C. C2H4 D.C6H6 Câu 3: Các chất cĩ liên kết đơi dễ tham gia phản ứng: A. Phản ứng thế B. Phản ứng phân hủy C. Phản ứng trao đổi D.Phản ứng cộng Câu 4 : Cặp chất nào sao đây làm mất màu dung dịch Brom? A.C2H4,C2H2 B.CH4,C2H2 C. C6H6, C2H5Cl D. C2H4, CH4 Câu 5 : Chất khí nào kích thích quả mau chín? A. Khí cacbonic B.Metan C.Etilen D.Benzen Câu 6 : Cơng thức cấu tạo của benzen cĩ đặc điểm: A.Gồm vịng 6 cạnh B. Cĩ 3 liên kết đơn C.Vịng 6 cạnh đều D. Vịng 6 cạnh đều ,cĩ 3 liên kết đơi xen kẽ với 3 liên kết đơn. Câu 7 : Điều chế axetilen bằng cách: A.Điện phân nước B. Cho CaC2 tác dụng với nước C. Cho Ca tác dụng với nước D. Cho Mg tác dụng với HCl Câu 8 :Phát biểu nào sau đây là đúng ? A. Dầu mỏ là đơn chất B. Dầu mỏ là hợp chất C.Dầu mỏ là hỗn hợp phức tạp của nhiều loại hidrocacbon D.Dầu mỏ là 1 chất phức tạp Câu 9 : Mục đích của phương pháp crackinh dầu nặng là: A .Điều chế etilen B. Điều chế metan C. Tăng chất lượng xăng D. Tăng lượng xăng thu được Câu 10 : Để sử dụng nhiên liệu cĩ hiệu quả cần cung cấp lượng oxi: A. Vừa đủ B. Dư C. Thiếu D. Đủ và phải dư Câu 11 : Rượu etylic sơi ở nhiệt độ : A.78.3oC B.88.3 oC C.87.3 oC D. 100 oC. Câu 12 : Cần bao nhiêu lít dung dịch Brom 0,1 M để tác dụng hết với 0,1 mol khí etilen? A. 0,1 lít B. 1 lít C. 2 lít D. 1,5lít B. TỰ LUẬN : ( 7 điểm ) Câu 1 : ( 2 đ) Hồn thành chuổi phản ứng hĩa học sau đây ghi rõ điều kiện (nếu cĩ) CaC2. → C2H2 → C2H4 → PE ↓ C 2H2Br4 (Chuỗi PU cần đánh số thứ tự) Câu 2 : ( 2đ ) Cĩ 3 lọ đựng 3 chất khí là: CH4, C2H4 và CO2 .Hãy trình bày cách nhận biết các chất khí đĩ? Viết các phương trình hĩa học (nếu cĩ). Câu 3 : (3đ ) Đốt cháy hồn tồn 5,6 lít khí Metan (ở đktc). Tính: Phải dùng bao nhiêu lít khí oxi (ở đktc) ? Phải dùng bao nhiêu lít khí khơng khí ? ( Biết rằng oxi chiếm 20 % thể tích khơng khí). Dẫn khí CO2 đi qua dung dịch Ca(OH)2 thì thu được bao nhiêu gam kết tủa? ( Cho biết : Ca = 40 ; O = 16 ; C = 16 ) . - HẾT- ĐÁP ÁN VÀ BIỂU ĐIỂM A.PHẦN TRẮC NGHIỆM : ( 3 đ) HS chọn đúng mỗi câu đạt 0,25 đ CÂU 1 2 3 4 5 6 7 8 9 10 11 12 CHỌN B C D A C D B C D A A B B. TỰ LUẬN : (7đ) Câu 1 : ( 2 đ ) Hồn thành đúng mỗi phương trình đúng đạt 0,5 đ , cân bằng sai cịn 0,25đ. (1). CaC2 + H2O → C2H2 + Ca(OH)2 Ni,t0 (2). C2H2 + H2 → C2H4 (3) nCH2 = CH2 xt,p,t0à ( - CH2- CH2 -)n (4) C2H2 + 2 Br2 à C2H2Br4 Câu 2 : ( 2 đ ) Đánh số thứ tự vào mỗi lọ.(0,125đ) Lấy 1 ít chất khí của mỗi lọ làm mẫu thử (0,125đ) Dùng dung dịch Brom để nhận biết C2H4 à làm mất màu vàng da cam của Brom . ( 0.25đ ) PT : C2H4 + Br2 à C2H4Br2 (0,5đ) Dùng dung dịch nước vơi trong Ca(OH)2 nhận biết CO2 à cĩ xuất hiện chất kất tủa trắng . ( 0.25 đ ) PT : Ca(OH)2 + CO2 à CaCO3â + H2O ( 0.5đ) - Cịn lại là CH4. ( 0.25đ) Câu 3 : ( 2 đ ) Số mol của CH4 : n = 5,6/22,4 = 0.25 (mol) PT : CH4 + 2O2 → CO2 + 2H2O (0,5đ) TPT 1mol 2mol 1 mol 2mol TĐB 0,25mol 0,5mol 0,25mol 0,5mol (0,25đ) a. Thể tích khí oxi cần dùng: VOxi = 0,5x 22,4 = 11,2 lít (0,5đ) b. Thể tích khơng khí: VKK = 11.2x 100/20 = 56 lít (0,5đ) c. PT : CO2 + Ca(OH)2 → CaCO3 ↓ + H2O (0,25đ) số mol CO2 = số mol CaCO3 = 0,25 mol (0,25đ) Khối lượng của chất kết tủa là: m = n x M = 0,25 x 100 = 25 gam (0,5đ) (Học sinh cĩ thể làm bài theo cách khá, nếu đúng vẫn đạt điểm tương đương) - Hết -
Tài liệu đính kèm:
 Đề 1.doc
Đề 1.doc





