Đề thi học kì I năm học 2015 – 2016 môn : Hóa học 8 (đề 1) thời gian: 45 phút (không kể thời gian phát đề)
Bạn đang xem tài liệu "Đề thi học kì I năm học 2015 – 2016 môn : Hóa học 8 (đề 1) thời gian: 45 phút (không kể thời gian phát đề)", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
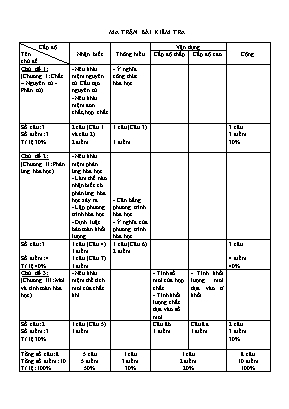
MA TRẬN BÀI KIỂM TRA Cấp độ Tên chủ đề Nhận biết Thông hiểu Vận dụng Cộng Cấp độ thấp Cấp độ cao Chủ đề 1: (Chương I: Chất – Nguyên tử - Phân tử) - Nêu khái niệm nguyên tử. Cấu tạo nguyên tử. - Nêu khái niệm đơn chất, hợp chất - Ý nghĩa công thức hóa học Số câu: 3 Số điểm: 3 Tỉ lệ 30% 2 câu (Câu 1 và câu 2) 2 điểm 1 câu (Câu 3) 1 điểm 3 câu 3 điểm 30% Chủ đề 2: (Chương II: Phản ứng hóa học) - Nêu khái niệm phản ứng hóa học. - Làm thế nào nhận biết có phản ứng hóa học xảy ra. - Lập phương trình hóa học. - Định luật bảo toàn khối lượng - Cân bằng phương trình hóa học - Ý nghĩa của phương trình hóa học. Số câu: 3 Số điểm: 4 Tỉ lệ 40% 1 câu (Câu 4) 1 điểm 1 câu (Câu 7) 1 điểm 1 câu (Câu 6) 2 điểm 3 câu 4 điểm 40% Chủ đề 3: (Chương III: Mol và tính toán hóa học) - Nêu khái niệm thể tích mol của chất khí. - Tính số mol của hợp chất - Tính khối lượng chất dựa vào số mol - Tính khối lượng mol dựa vào tỉ khối Số câu: 2 Số điểm: 3 Tỉ lệ 30% 1 câu (Câu 5) 1 điểm Câu 8b 1 điểm Câu 8a 1 điểm 2 câu 3 điểm 30% Tổng số câu: 8 Tổng số điểm: 10 Tỉ lệ: 100% 5 câu 5 điểm 50% 1 câu 3 điểm 30% 1 câu 2 điểm 20% 8 câu 10 điểm 100% PHÒNG GD&ĐT CHÂU THÀNH TRƯỜNG THCS THÁI BÌNH ĐỀ THI HỌC KÌ I NĂM HỌC 2015 – 2016 MÔN : HÓA HỌC 8 (ĐỀ 1) Thời gian: 45 phút (Không kể thời gian phát đề) I.Lí thuyết: (5 điểm) Câu 1: (1 điểm ) Nêu khái niệm nguyên tử là gì? Nguyên tử có cấu tạo như thế nào? Câu 2: (1 điểm ) Nêu khái niệm đơn chất là gì? Hợp chất là gì? Cho ví dụ minh họa? Câu 3: (1 điểm) Công thức hóa học CuSO4 cho ta biết ý nghĩa gì? (Biết Cu = 64 ; S = 32 ; O = 16) Câu 4: (1 điểm ) Phản ứng hóa học là gì? Làm thế nào nhận biết có phản ứng hóa học xảy ra? Câu 5: (1 điểm ) Nêu khái niệm thể tích mol của chất khí? Cho biết thể tích mol của các chất khí ở đktc? II.Bài tập: (5 điểm) Câu 6: (2 điểm ) Cho sơ đồ của các phản ứng sau: a. Na + O2 - - -- > Na2O b. KClO3 - - - - > KCl + O2 Hãy viết thành phương trình hóa học và cho biết tỉ lệ số nguyên tử, số phân tử của các chất trong mỗi phương trình hóa học lập được Câu 7: (1 điểm ) Để chế tạo mỗi quả pháo bông nhằm phục vụ cho các chiến sĩ biên phòng giữ gìn biên giới hải đảo ở Quần đảo Trường sa đón xuân về, người ta cho vào hết 600 gam kim loại Magie (Mg), khi pháo cháy trong khí oxi (O2) sinh ra 1000 gam Magie oxit (MgO) Viết công thức về khối lượng của phản ứng? Tính khối lượng khí oxi (O2) tham gia phản ứng? Câu 8: (2 điểm ) Hợp chất A có tỉ khối so với khí oxi là 2. Tính khối lượng mol của hợp chất? Hãy cho biết 5,6 lít khí A (ở đktc) có khối lượng là bao nhiêu gam? Thái Bình, ngày 19 tháng 11 năm 2015 Tổ trưởng GVBM Lê Ngọc Châu Võ Thị Thu Sương ĐÁP ÁN ĐỀ THI MÔN HÓA HỌC 8 HK I NĂM HỌC 2015 – 2016 ĐÁP ÁN BIỂU ĐIỂM I.Lí thuyết: Câu 1: - Nguyên tử là hạt vô cùng nhỏ và trung hòa về điện. - Nguyên tử gồm hạt nhân mang điện tích dương và vỏ tạo bởi một hay nhiều electron mang điện tích âm Câu 2: - Đơn chất là những chất tạo nên từ một nguyên tố hóa học Ví dụ: Cu; H2 - Hợp chất là những chất tạo nên từ hai nguyên tố hóa học trở lên Ví dụ: H2O; H2SO4 Câu 3: - Công thức hóa học CuSO4 cho ta biết: - Nguyên tố Cu; S; O tạo nên chất - Trong hợp chất có 1Cu; 1S; 4O - Phân tử khối: 64 + 32 + 16.4 = 160(đvC) Câu 4: - Phản ứng hóa học là quá trình biến đổi chất này thành chất khác - Nhận biết phản ứng xảy ra dựa vào dấu hiệu có chất mới tạo thành Câu 5: Thể tích mol của chất khí là thể tích chiếm bởi N phân tử chất đó. - Ở đktc, thể tích mol của các chất khí đều bằng 22,4 lít II.Bài tập: Câu 6: a. 4Na + O2 2Na2O Có tỉ lệ: Số nguyên tử Na: Số phân tử O2: Số phân tử Na2O = 4 : 1 : 2 b. 2KClO3 2KCl + 3O2 Có tỉ lệ: Số phân tử KClO3: Số phân tử KCl: Số phân tử O2 = 2 : 2 : 3 Câu 7: a) Áp dụng theo ĐLBTKL, ta có công thức về khối lượng của phản ứng b) Khối lượng khí oxi tham gia phản ứng: = 1000 - 600 = 400 (gam) Câu 8: a) Khối lượng mol của hợp chất A là: = 2.32 = 64 (gam) b) Số mol của hợp chất A là: Khối lượng 5,6 lít khí A (ở đktc) là: = 0,25.64 = 16 (gam) (5 điểm) 0,5 điểm 0,5 điểm 0,25 điểm 0,25 điểm 0,25 điểm 0,25 điểm 0,25 điểm 0,25 điểm 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm (5 điểm) 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm 1 điểm 0,5 điểm 0,5 điểm Thái Bình, ngày 19 tháng 11 năm 2015 Tổ trưởng GVBM Lê Ngọc Châu Võ Thị Thu Sương
Tài liệu đính kèm:
 De_thi_Hoa_hoc_8_HKI_1516.doc
De_thi_Hoa_hoc_8_HKI_1516.doc





