Đề kiểm tra học kì II năm học 2014 – 2015 môn: Hóa học 8 Trường Thcs Hùng Vương
Bạn đang xem tài liệu "Đề kiểm tra học kì II năm học 2014 – 2015 môn: Hóa học 8 Trường Thcs Hùng Vương", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
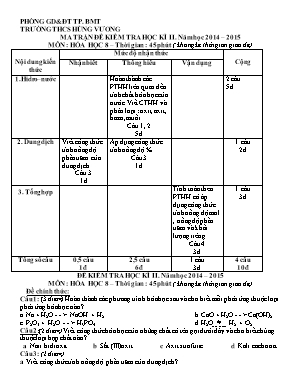
PHÒNG GD&ĐT TP. BMT TRƯỜNG THCS HÙNG VƯƠNG MA TRẬN ĐỀ KIỂM TRA HỌC KÌ II. Năm học 2014 – 2015 MÔN : HÓA HỌC 8 – Thời gian : 45 phút ( không kể thời gian giao đề) Nội dung kiến thức Mức độ nhận thức Cộng Nhận biết Thông hiểu Vận dụng 1.Hidro–nước Hoàn thành các PTHH liên quan đến tính chất hóa học của nước.Viết CTHH và phân loại : oxit, axit, bazơ, muối. Câu 1, 2 5đ 2 câu 5đ 2. Dung dịch Viết công thức tính nồng độ phần trăm của dung dịch. Câu 3 1đ Áp dụng công thức tính nồng độ % Câu 3 1đ 1 câu 2đ 3. Tổng hợp Tính toán theo PTHH có áp dụng công thức tính nồng độ mol , nồng độ phần trăm và khối lượng riêng. Câu 4 3đ 1 câu 3đ Tổng số câu 0,5 câu 1đ 2,5 câu 6đ 1 câu 3đ 4 câu 10đ ĐỀ KIỂM TRA HỌC KÌ II. Năm học 2014 – 2015 MÔN : HÓA HỌC 8 – Thời gian : 45 phút ( không kể thời gian giao đề) Đề chính thức: Câu 1: (3 điểm) Hoàn thành các phương trình hóa học sau và cho biết mỗi phản ứng thuộc loại phản ứng hóa học nào? a. Na + H2O - - > NaOH + H2 b. CaO + H2O - - > Ca(OH)2 c. P2O5 + H2O - - > H3PO4 d. H2O đp H2 + O2 Câu 2:(2 điểm) Viết công thức hóa học của những chất có tên gọi dưới đây và cho biết chúng thuộc loại hợp chất nào? a. Nari hiđroxit b. Sắt (III)oxit c. Axit sunfuric d. Kali cacbonat Câu 3: (2 điểm) a. Viết công thức tính nồng độ phần trăm của dung dịch ? b. Áp dụng: Hòa tan 10g CuSO4 vào nước thu được 200 gam dung dịch CuSO4. Tính nồng độ phần trăm của dung dịch thu được ? Câu 4: (3 điểm) Cho 3,6 gam Mg tác dụng hết với dung dịch axit clohidric HCl 1M Viết PTHH và tính thể tích khí thoát ra (ở đktc)? Tính thể tích dung dịch HCl cần dùng cho phản ứng? Tính khối lượng dung dịch HCl 1M tham gia phản ứng, biết ( Ddd HCl = 1,2 g/ml)? Tính nồng độ phần trăm dung dịch muối sau phản ứng? (Biết : Mg = 24; Cl = 35,5 ; H = 1)./. ĐÁP ÁN ĐỀ KIỂM TRA HỌC KÌ II. Năm học 2014 – 2015 MÔN : HÓA HỌC 8 – Thời gian : 45 phút ( không kể thời gian giao đề) Đề chính thức: Câu 1(3đ) :Mỗi PTHH đúng được 0,5 điểm Xác định đúng loại phản ứng của mỗi pư được : 0,25đ Câu 2(2đ): Viết đúng mỗi công thức được 0,25 điểm Phân loại đúng mỗi công thức được 0,25 điểm a. NaOH : bazơ b.Fe2O3: oxit c.H2SO4: axit d. K2CO3 : muối Câu 3(2đ): Viết công thức tính nồng độ phần trăm đúng được 0,5 đ Nêu đầy đủ các đại lượng và đơn vị trong công thức 0,5 đ b. C% ddCuSO4 = mct / mdd x100% = 10/200 x 100% = 5% 1đ Câu 4(3đ): (1,5đ)PT: Mg + 2HCl FeCl2 + H2 0,5đ 0,15 0,3 0,15 0,15 nMg = 3,6 / 24 = 0,15 mol 0,5đ VH2 (đktc) = 0,15 . 22,4 = 3,36 (lít) 0,5đ (0,5đ)Vdd = n/ CM = 0,3 / 1 = 0,3 lít = 300ml 0,25đ c.(1đ) mdd = Vdd . D = 300. 1,2 = 336 g 0,25đ mFeCl2 = 015 . 127 = 19,05 g 0,25đ Theo ĐLBTKL, ta có: mdd sau = 3,6 + 336 - (0,15 . 2) = 339,3 g 0,25đ C%dd FeCl2 = 19,05 / 339,3 x 100% = 5,6% 0,25đ./. PHÒNG GD&ĐT TP. BMT TRƯỜNG THCS HÙNG VƯƠNG ĐỀ KIỂM TRA HỌC KÌ II. Năm học 2014 – 2015 MÔN : HÓA HỌC 8 – Thời gian : 45 phút ( không kể thời gian giao đề) Đề chính thức: Câu 1: (3 điểm) Hoàn thành các phương trình hóa học sau và cho biết mỗi phản ứng thuộc loại phản ứng hóa học nào? a. Na + H2O - - > NaOH + H2 b. CaO + H2O - - > Ca(OH)2 c. P2O5 + H2O - - > H3PO4 d. H2O đp H2 + O2 Câu 2:(2 điểm) Viết công thức hóa học của những chất có tên gọi dưới đây và cho biết chúng thuộc loại hợp chất nào? a. Nari hiđroxit b. Sắt (III)oxit c. Axit sunfuric d. Kali cacbonat Câu 3: (2 điểm) a. Viết công thức tính nồng độ phần trăm của dung dịch ? b. Áp dụng: Hòa tan 10g CuSO4 vào nước thu được 200 gam dung dịch CuSO4. Tính nồng độ phần trăm của dung dịch thu được ? Câu 4: (3 điểm) Cho 3,6 gam Mg tác dụng hết với dung dịch axit clohidric HCl 1M Viết PTHH và tính thể tích khí thoát ra (ở đktc)? Tính thể tích dung dịch HCl cần dùng cho phản ứng? Tính khối lượng dung dịch HCl 1M tham gia phản ứng, biết ( Ddd HCl = 1,2 g/ml)? Tính nồng độ phần trăm dung dịch muối sau phản ứng? (Biết : Mg = 24; Cl = 35,5 ; H = 1)./. PHÒNG GD&ĐT TP. BMT TRƯỜNG THCS HÙNG VƯƠNG ĐỀ KIỂM TRA HỌC KÌ II. Năm học 2014 – 2015 MÔN : HÓA HỌC 8 – Thời gian : 45 phút ( không kể thời gian giao đề) Đề chính thức: Câu 1: (3 điểm) Hoàn thành các phương trình hóa học sau và cho biết mỗi phản ứng thuộc loại phản ứng hóa học nào? a. Na + H2O - - > NaOH + H2 b. CaO + H2O - - > Ca(OH)2 c. P2O5 + H2O - - > H3PO4 d. H2O đp H2 + O2 Câu 2:(2 điểm) Viết công thức hóa học của những chất có tên gọi dưới đây và cho biết chúng thuộc loại hợp chất nào? a. Nari hiđroxit b. Sắt (III)oxit c. Axit sunfuric d. Kali cacbonat Câu 3: (2 điểm) a. Viết công thức tính nồng độ phần trăm của dung dịch ? b. Áp dụng: Hòa tan 10g CuSO4 vào nước thu được 200 gam dung dịch CuSO4. Tính nồng độ phần trăm của dung dịch thu được ? Câu 4: (3 điểm) Cho 3,6 gam Mg tác dụng hết với dung dịch axit clohidric HCl 1M Viết PTHH và tính thể tích khí thoát ra (ở đktc)? Tính thể tích dung dịch HCl cần dùng cho phản ứng? Tính khối lượng dung dịch HCl 1M tham gia phản ứng, biết ( Ddd HCl = 1,2 g/ml)? Tính nồng độ phần trăm dung dịch muối sau phản ứng? (Biết : Mg = 24; Cl = 35,5 ; H = 1)./.
Tài liệu đính kèm:
 De_thi_Hoc_Ky_2_Hoa_8.doc
De_thi_Hoc_Ky_2_Hoa_8.doc





