Đề kiểm tra học kì II môn: Hóa học 8 trường THCS Bình Hòa Phước
Bạn đang xem tài liệu "Đề kiểm tra học kì II môn: Hóa học 8 trường THCS Bình Hòa Phước", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
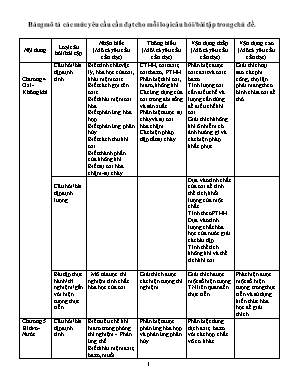
Bảng mô tả các mức yêu cầu cần đạt cho mỗi loại câu hỏi/bài tập trong chủ đề. Nội dung Loại câu hỏi/bài tập Nhận biết (Mô tả yêu cầu cần đạt) Thông hiểu (Mô\ tả yêu cầu cần đạt) Vận dụng thấp (Mô tả yêu cầu cần đạt) Vận dụng cao (Mô tả yêu cầu cần đạt) Chương 4 Oxi- Không khí Câu hỏi/bài tập định tính Biết tính chất vật lý, hóa học của oxi, khái niệm oxit. Biết cách gọi tên oxit. Biết khái niệm oxi hóa. Biết phản ứng hóa hợp. Biết phản ứng phân hủy. Biết cách thu khí oxi. Biết thành phần của không khí Biết sự oxi hóa chậm- sự cháy CTHH, oxit axit, oxit bazơ, PTHH Phân biệt khí oxi, hiđro, không khí. Các ứng dụng của oxi trong đời sống và sản xuất. Phân biệt được sự cháy và sự oxi hóa chậm. Các biện pháp dập tắt sự cháy. Phân biệt được oxit axit và oxit bazơ. Tính lượng oxi cần điều chế và lượng cần dùng để điều chế khí oxi. Giải thích không khí ô nhiễm có ảnh hưởng gì và các biện pháp khắc phục. Giải thích tại sao các phi công, thợ lặn phải mang theo bình chứa oxi để thở. Câu hỏi/bài tập định lượng Dựa vào tính chất của oxi để tính thể tích, khối lượng của một chất. Tính theo PTHH. Dựa vào tính lượng chất hóa học của nước giải các bài tập. Tính thể tích không khí và thể tích khí oxi. Bài tập thực hành/thí nghiệm/gắn với hiện tượng thực tiễn. Mô tả được thí nghiệm tính chất hóa học của oxi. Giải thích được các hiện tượng thí nghiệm. Giải thích được một số hiện tượng TN liên quan đến thực tiễn. Phát hiện được một số hiện tượng trong thực tiễn và sử dụng kiến thức hóa học để giải thích. Chương 5 Hiđro- Nước Câu hỏi/bài tập định tính Biết điều chế khí hiđro trong phòng thí nghiệm - Phản ứng thế. Biết khái niệm axit, bazơ, muối. Cách gọi tên axit, bazơ. Phân biệt được phản ứng hóa hợp và phản ứng phân hủy. Phân biệt dung dịch axit, bazơ với các hợp chất vô cơ khác. Câu hỏi/bài tập định lượng Dựa vào tính lượng chất hóa học của nước giải các bài tập Bài tập thực hành/thí nghiệm/gắn với hiện tượng thực tiễn. Mô tả được thí nghiệm điều chế khí oxi. Giải thích được các hiện tượng thí nghiệm. Giải thích được một số hiện tượng TN liên quan đến thực tiễn. Phát hiện được một số hiện tượng trong thực tiễn và sử dụng kiến thức hóa học để giải thích. Chương 6 Dung dịch Câu hỏi/bài tập định tính Biết khái niệm dung dịch, độ tan. Câu hỏi/bài tập định lượng Tính độ tan của một chất. Bài tập thực hành/thí nghiệm/gắn với hiện tượng thực tiễn. Mô tả được thí nghiệm xác định thành phần không khí. Giải thích được các hiện tượng thí nghiệm. Giải thích được một số hiện tượng TN liên quan đến thực tiễn. Phát hiện được một số hiện tượng trong thực tiễn và sử dụng kiến thức hóa học để giải thích. PHÒNG GD-ĐT LONG HỒ TRƯỜNG THCS BÌNH HÒA PHƯỚC MA TRẬN ĐỀ KIỂM TRA HỌC KÌ II NĂM HỌC 2015 - 2016 MÔN: HÓA HỌC 8 CHỦ ĐỀ Mức độ nhận thức Nhận biết Thông hiểu Vận dụng Vận dụng ở mức cao hơn TN TL TN TL TN TL TN TL 1. Oxi-Không khí Hiểu được dung dịch axit, bazơ, muối. Hiểu thế nào là phản ứng hóa hợp, điều chế khí oxi, sự oxi hóa. Số câu hỏi 4 1 Sô điểm 1 2 2. Hiđro . Nước Biết tính chất hóa học của hiđro, nước, điều chế khí hiđro. Hiểu chất nào là oxitaxit, oxitbazơ. Hiểu được phản ứng thế, quì tím để nhận biết dung dịch axit, bazơ. Hiểu cách tính số mol dựa vào PTHH. Dựa vào PTHH tính khối lượng của một chất. Số câu hỏi 2 6 2 Sô điểm 3 1,5 2 3. Dung dịch Hiểu được thế nào dung dịch, dung dịch bảo hòa, chưa bảo hòa. Số câu hỏi 2 Số điểm 0,5 Tổng 3 30% 3 30% 2 20% 2 20% ĐỀ TỰ LUẬN PHÒNG GD-ĐT LONG HỒ ĐỀ KIỂM TRA HỌC KỲ II NĂM HỌC 2015- 2016 TRƯỜNG THCS BÌNH HÒA PHƯỚC MÔN: HÓA HỌC 8 Thời gian làm bài : 60 phút (không kể thời gian phát đề) (phần tự luận: 45 phút, phần trắc nghiệm:15 phút) ĐÊ CHÍNH THỨC I. TỰ LUẬN: (7 ĐIỂM) Câu 1: (2 điểm) (Hiểu) Có 3 lọ đã bị mất nhãn đựng riêng biệt có dung dịch không màu sau: Natriclorua (NaCl), Natrihiđroxit (NaOH), Axitsunfuric (H2SO4). Bằng phương pháp hóa học hãy nhận biết dung dịch trong mỗi lọ? Câu 1 : (2 điểm): Hoàn thành sơ đồ phản ứng sau: (Biết) a/ CaO + H2O → b/ Na + H2O → c/ Zn + HCl → d/ H2 + CuO → Câu 3 :(3 điểm) Cho a gam kim loại sắt phản ứng vừa đủ với 200 gam dung dịch HCl 14,6% a/ Viết phương trình hóa học xãy ra.( Hiểu) b/ Tính a. (Vận dụng thấp) c/ Tính thể thể khí hiđro thu được ở điều kiện tiểu chuẩn. (Vận dụng thấp) (Cho biết Na = 23; O = 16; Fe = 56; Cl = 35,5 ; H = 1) ĐỀ TRẮC NGHIỆM PHÒNG GD-ĐT LONG HỒ ĐỀ KIỂM TRA HỌC KỲ II NĂM HỌC 2015- 2016 TRƯỜNG THCS BÌNH HÒA PHƯỚC MÔN: HÓA HỌC 8 Thời gian làm bài :60 phút (không kể thời gian phát đề) (phần tự luận: 45 phút, phần trắc nghiệm:15 phút) ĐÊ CHÍNH THỨC II. TRẮC NGHIỆM: (3 ĐIỂM). Học sinh chọn câu trả lời đúng nhất và khoanh tròn. Mỗi câu 0,25 điểm. 1/ Cho phản ứng: C + O2 → CO2. Phản ứng trên là: (Hiểu) A. Phản ứng hóa hợp B. Phản ứng phân hủy C. Phản ứng thế D. Không xác định được 2/ Quá trình nào sau đây không làm giảm lượng oxi trong khí? (Hiểu) A. Sự gỉ của các đồ vật bằng sắt B. Sự cháy của than, củi, bếp ga C. Sự quang hợp của cây xanh D. Sự hô hấp của động vật 3 / Dãy chỉ gồm các oxit axit là: (Biết) A. CO, CO2, MnO2, Al2O3, P2O5 B. CO2, SO2, P2O5 , SO3, N2O5 C. FeO, Mn2O5, SiO2, CaO, Fe2O3 D. Na2O, BaO, H2O, H2O2, ZnO 4/ Oxit của kim loại nào dưới đây là oxit bazơ? (Biết) A. CO2 B. P2O5 C. SO2 D. CaO 5/ Oxit của phi kim nào dưới đây là oxit axit? (Biết) A. CO2 B. CaO C. CuO D. Fe2O3 6/ Các phản ứng cho dưới đây phản ứng nào là phản ứng thế? (Hiểu) A. CO2 + NaOH → NaHCO3 B. Fe + 2HCl → FeCl2 + H2 C. CaO + H2O → Ca(OH)2 D. 2Fe + Cl2 → 2FeCl3 7/ Cho 13g Zn tác dụng vừa đủ với axit HCl. Thể tích khí H2 (đktc) thu được là: (Hiểu) A. 11,2 lít B. 2,24 lít B. 3,35 lít D. 4,48 lít 8/ Nguyên liệu để sản xuất khí oxi trong phòng thí nghiệm là: (Biết) A. KClO3 B. H2O C. Không khí D.CaO 9/ Trong các chất cho dưới đây, chất nào làm quì tím hóa đỏ: (Hiểu) A. Nước B. Bazơ C. Axit D. Muối 10/ Dung dịch Bazơ là những chất làm quì tím chuyển sang màu: (Hiểu) A. Xanh B. Đỏ C. Tím D. Vàng 11/ Dung dịch là hỗn hợp đồng nhất của: (Hiểu) A. Chất rắn và chất lỏng B. Chất tan và dung môi C. Hai chất lỏng D. Chất khí và chất lỏng 12/ Hòa tan 10g muối ăn (NaCl) vào 40 g nước được dung dịch nước muối có nồng độ phần trăm là: (Hiểu) A. 40% B. 10% C. 25% D. 20% PHÒNG GD- ĐT LONG HỒ HƯỚNG DẪN CHẤM MÔN: HÓA HỌC 8 TRƯỜNG THCS BÌNH HÒA PHƯỚC NĂM HỌC 2015- 2016 I. TỰ LUẬN (7Đ) Câu 1:(2đ)) Dùng mẫu quì tím bỏ vào 3 mẫu thử (0,5đ): Mẫu nào làm quì tím hóa đỏ là H2SO4 (0,5đ), mẫu nào làm quì tím hóa xanh là NaOH (0,5đ), mẫu nào không làm qui tím đổi màu là NaCl. (0,5đ) Câu 2: (2đ) a/ CaO + H2O → Ca(OH)2 (0,5đ) b/ 2Na + 2H2O → 2NaOH + H2 (0,5đ) c/ Zn + 2HCl → ZnCl2 + H2 (0,5đ) d/ H2 + CuO H2O + Cu (0,5đ) Câu 3: (3đ) a/ Fe + 2HCl FeCl2 + H2 1đ 1mol 2mol 1mol 1mol 0,1mol ? mol ?mol ?mo b/ Khối lượng của HCl: mHCl = 200 x14,6/100 = 29,2g 0,25đ Sô mol HCl là: nHCl =29,2/36,5 = 0,8mol 0,25đ Theo PTHH ta có: nFe = 1/2 nHCl = 0,8/2 = 0,4 mol 0,25đ Vậy a = mFe = 0,4 x 56= 22,4g 0,25đ c/ Theo PTHH: nH2 = nFe= 0,4 mol 0,5đ VH2 =0,4 x 22,4= 8,96l 0,5đ II.TRẮC NGHIỆM KHÁCH QUAN: (3 Đ) Mỗi câu đúng được: 0,25 đ 1 2 3 4 5 6 7 8 9 10 11 12 A C B D A B D A C A B D
Tài liệu đính kèm:
 DE_THI_HOC_KI_II.doc
DE_THI_HOC_KI_II.doc





