2 Đề kiểm tra cuối học kì I Hóa học 8 - Năm học 2022-2023 - Trường PTDTBT THCS Cốc Ly 1 (Có đáp án + Ma trận)
Bạn đang xem tài liệu "2 Đề kiểm tra cuối học kì I Hóa học 8 - Năm học 2022-2023 - Trường PTDTBT THCS Cốc Ly 1 (Có đáp án + Ma trận)", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
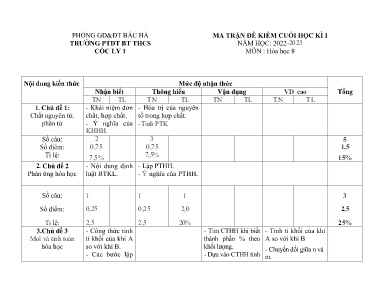
PHÒNG GD&ĐT BẮC HÀ MA TRẬN ĐỀ KIỂM CUỐI HỌC KÌ I TRƯỜNG PTDT BT THCS NĂM HỌC: 2022-2023 CỐC LY 1 MÔN : Hóa học 8 Nội dung kiến thức Mức độ nhận thức Nhận biết Thông hiểu Vận dụng VD cao Tổng TN TL TN TL TN TL TN TL 1. Chủ đề 1: - Khái niệm đơn - Hóa trị của nguyên Chất nguyên tử, chất, hợp chất. tố trong hợp chất. phân tử - Ý nghĩa của -Tính PTK KHHH. Số câu: 2 3 5 Số điểm: 0,75 0,75 1,5 Tỉ lệ: 7,5% 7,5% 15% 2. Chủ đề 2 - Nội dung định - Lập PTHH. Phản ứng hóa học luật BTKL. - Ý nghĩa của PTHH. Số câu: 1 1 1 3 Số điểm: 0,25 0,25 2,0 2,5 Tỉ lệ: 2,5 2,5 20% 25% 3.Chủ đề 3 - Công thức tính - Tìm CTHH khi biết - Tính tỉ khối của khí Mol và tính toán tỉ khối của khí A thành phần % theo A so với khí B hóa học so với khí B. khối lượng. - Chuyển đổi giữa n và - Các bước lập - Dựa vào CTHH tính m. CTHH khí biết % về khối lượng các thành hần % n.tố. theo khối lượng các nguyên tố Số câu: 1,5 1 0,5 3 Số điểm: 3,0 2,0 1,0 5,0 Tỉ lệ: 30% 20% 10% 50% Tổng số câu 4,5 5 1 0,5 11 Tổng số điểm 4,0 3,0 2,0 1,0 10,0 Tỉ lệ 40% 30% 20% 10% 100% PHÒNG GD&ĐT BẮC HÀ ĐỀ KIỂM TRA CUỐI HỌC KÌ I TRƯỜNG PTDT BT THCS NĂM HỌC: 2022-2023 CỐC LY 1 MÔN : Hóa học 8 Thời gian : 45 phút ( Không tính thời gian giao đề) Đề thi gồm 2 trang 11 câu. ĐỀ SỐ 1 I. Trắc nghiệm khách quan: (2,0 điểm) Khoanh tròn vào chữ cái A, B, C hoặc D đứng trước câu trả lời mà em cho là đúng. Câu 1: 8 Cl có nghĩa là gì? A. 8 chất clo. B. 8 nguyên tố Clo. C. 8 phân tử clo. D. 8 nguyên tử clo Câu 2: Hóa trị của Fe trong hợp chất Fe2(SO4)3 A. IV. B. III. C. II. D. I. Câu 3: Dãy chất nào dưới đây là đơn chất A. O2, SO2, Fe. B. H2, Cu, ZnO. C. Cl2, S, Ca. D. Ca, Cl2, Na. Câu 4: Phân tử khối của hợp chất FeO là A. 80 đvC. B. 160đvC. C. 81 đvC. D. 72 đvC Câu 5: Đốt cháy 20g Kali (K) trong không khí thì thu được 35g kali Oxit (K2O). Khối lượng Oxi tham gia phản ứng là: A.15g. B.20 g. C. 10g. D. 35 g. t0 Câu 6: Cho PTHH: 4Al + 3O2 2Al2O3. Tỉ lệ số nguyên tử, số phân tử của các chất lần lượt trong phương trình hóa học trên là A. 3:2:4. B. 4:3:2. C. 2:3:4. D. 3:4:2. Câu 7: Năm phân tử hiđro viết là: A. 5H B. 5H2 C. H2 D. 5 h2 II. Trắc nghiệm tự luận: (8,0 điểm) Câu 8 (2,0 điểm) Cân bằng các sơ đồ phản ứng sau: a. C2H4 + O2 -----> CO2 + H2O b. Al + Cl2 -----> AlCl3 c. K + O2 ----> K2O. d. Fe + HCl ----> FeCl2 + H2 Câu 9: (2,0 điểm) Tỉ khối của chất khí Tỉ khối của chất khí là một dạng bài tập cơ bản nhất trong chương trình hóa học 8. Công thức tính tỉ khối chất khí khá đơn giản và dễ nhớ, dễ vận dụng vào tính toán bài tập thực tế. a. Viết công thức tính tỉ khối chất khí của khí A và khí B ? b. Khí SO3 nặng hay nhẹ hơn khí O2 bao nhiêu lần ? Câu 10: (2,0 điểm) Trình bày các bước lập CTHH khi biết thành phần % theo khối lượng các nguyên tố trong hợp chất ? Câu 11: (2,0 điểm) Tìm CTHH của khí A được tạo bởi 2 nguyên tố hóa học là Cacbon và Oxi. Biết rằng %C=27,3%; % O=72,7% và MA=44(g/mol) BGH Duyệt TTCM Duyệt GV ra đề Hoàng Việt Chuyền PHÒNG GD&ĐT BẮC HÀ ĐỀ KIỂM TRA CUỐI HỌC KÌ I TRƯỜNG PTDT BT THCS NĂM HỌC: 2022-2023 CỐC LY 1 MÔN : Hóa học 8 Thời gian : 45 phút ( Không tính thời gian giao đề) Đề thi gồm 2 trang 11 câu. ĐỀ SỐ 2 I. Trắc nghiệm khách quan: (2,0 điểm) Khoanh tròn vào chữ cái A, B, C hoặc D đứng trước câu trả lời mà em cho là đúng. Câu 1: 5 Cl có nghĩa là gì? A. 5 nguyên tử clo B. 5 nguyên tố Clo. C. 5 phân tử clo. D. 5 chất clo. Câu 2: Hóa trị của S trong hợp chất SO3 A. IV. B. III. C. II. D.V I. Câu 3: Dãy chất nào dưới đây là hợp chất A. O2, SO2, Fe. B. H2O, CuCl2, ZnO. C. Cl2, S, Ca. D. CaO, HCl, NaOH. Câu 4: Phân tử khối của hợp chất CaO là A. 80 đvC. B. 160đvC. C. 81 đvC. D. 56 đvC Câu 5: Đốt cháy 25g Magie (Mg) trong không khí thì thu được 35g Magie Oxit (MgO). Khối lượng Oxi tham gia phản ứng là: A. 5g. B. 25 g. C. 10g. D. 15 g. Câu 6: Cho PTHH: 2H2 + O2 2H2O. Tỉ lệ số nguyên tử, số phân tử của các chất lần lượt trong phương trình hóa học trên là A. 3:2:4. B. 4:3:2. C. 2:1:2. D. 3:4:2. Câu 7: Năm phân tử Oxi viết là: A. 5O B. 5O2 C. O2 D. 5 o2 II. Trắc nghiệm tự luận (8,0 điểm) Câu 8 (2,0 điểm) Cân bằng các sơ đồ phản ứng sau: a. CH4 + O2 -----> CO2 + H2O b. Al + O2 -----> Al2O3 c. Na + O2 ----> Na2O. d. H2 + Fe2O3 ----> Fe + H2O Câu 9: (2,0 điểm) Tỉ khối của chất khí Tỉ khối của chất khí là một dạng bài tập cơ bản nhất trong chương trình hóa học 8. Công thức tính tỉ khối chất khí khá đơn giản và dễ nhớ, dễ vận dụng vào tính toán bài tập thực tế. a. Viết công thức tính tỉ khối chất khí của khí A và khí B ? b. Khí CH4 nặng hay nhẹ hơn khí H2 bao nhiêu lần ? Câu 10:(2,0 điểm).Trình bày các bước lập CTHH khi biết thành phần % theo khối lượng các nguyên tố trong hợp chất ? Câu 11:(2,0 điểm).Tìm CTHH của khí A được tạo bởi 2 nguyên tố hóa học là Cacbon và Oxi ? Biết rằng %C=27,3%; % O=72,7% và MA=44(g/mol) BGH Duyệt TTCM Duyệt GV ra đề Hoàng Việt Chuyền PHÒNG GD&ĐT BẮC HÀ HƯỚNG DẪN CHẤM CUỐI HỌC KÌ I TRƯỜNG PTDT BT THCS NĂM HỌC: 2022-2023 CỐC LY 1 MÔN : Hóa học 8 ĐỀ SỐ 1 I. Trắc nghiệm khách quan: (2 điểm) Mỗi đáp án đúng 0,25 điểm Câu 1 2 3 4 5 6 7 Đ/a D B C,D D A B B II. Trắc nghiệm tự luận (8 điểm) Câu Đáp án Điểm a. C2H4 + 3O2 2CO2 + 2H2O 0,5 b. 2Al + 3Cl2 2AlCl3 0,5 8 c. 4K + O2 2 K2O. 0,5 (2,0 d. Fe + 2HCl FeCl2 + H2 0,5 điểm) * Chú ý: Học sinh đặt số thứ tự các hệ số chưa đúng cho 0,25 điểm. Nếu một hệ số nào đó sai hoặc thiếu thì không tính điểm. a. CT tính tỉ khối khí A so với khí B: 0 t 0,25 9 (2,0 M : k/l mol của khí A 0,25 điểm) A MB: k/l mol của khí B 0,25 dA/B: tỉ khối của khí A so với khí B 0,25 b. MSO3 = 32 +3.16 = 80 (g) 80 0,25 dSO3/O2 = 2,5 lần 32 0,5 0,25 - Vậy khí SO3 nặng hơn khí O2 là 2,5 lần 10 + Bước 1: Tính khối lượng của mỗi nguyên tố có trong 1 0,75 (2,0 mol hợp chất điểm) + Bước 2: Tính số mol nguyên tử mỗi nguyên tố trong 1 0,75 mol hợp chất Suy ra số nguyên tử của mỗi nguyên tố trong 1 phân tử hợp chất + Bước 3: Viết công thức hóa học của hợp chất 0,5 -Khối lượng của mỗi nguyên tố có trong 1 mol khí A là: 27,3.44 0,5 m 12(g) 11 C 100 (2,0 72,7.44 m 32(g) 0,5 điểm) O 100 -Số mol của mỗi nguyên tố có trong 1 mol khí A là: m 12 n C 1(mol) 0,25 C MC 12 m 32 n O 2(mol) O 0,25 MO 16 -Vậy, trong 1 mol phân tử khí A có 1 nguyên tử C và 2 nguyên tử O. 0,25 0,25 - CTHH của khí A là CO2. Tổng 10 PHÒNG GD&ĐT BẮC HÀ HƯỚNG DẪN CHẤM CUỐI HỌC KÌ I TRƯỜNG PTDT BT THCS NĂM HỌC: 2022-2023 CỐC LY 1 MÔN : Hóa học 8 ĐỀ SỐ 2 I. Trắc nghiệm khách quan: (2 điểm) Mỗi đáp án đúng 0,25 điểm Câu 1 2 3 4 5 6 7 Đ/a A D B,D D C C B II. Trắc nghiệm tự luận (8 điểm) Câu Đáp án Điểm a. CH4 + 2O2 CO2 + 2H2O 0,5 b. 4Al + 3O2 2Al2O3. 0,5 8 c. 4Na + O2 2 Na2O. 0,5 (2,0 t0 d. 3H2 + Fe2O3 2 Fe + 3H2O 0,5 điểm) * Chú ý: Học sinh đặt số thứ tự các hệ số chưa đúng cho 0,25 điểm. Nếu một hệ số nào đó sai hoặc thiếu thì không tính điểm. a. CT tính tỉ khối khí A so vơi khí B: t0 0,25 9 (2,0 MA: k/l mol của khí A 0,25 điểm) MB: k/l mol của khí B 0,25 dA/B: tỉ khối của khí A so với khí B 0,25 b. MCH4 = 12 +4.1 = 16 (g/mol) 0,25 dCH4/H2 =16/2 = 8 lần 0,5 - Vậy khí CH4 nặng hơn khí H2 là 8 lần 0,25 10 + Bước 1: Tính khối lượng của mỗi nguyên tố có trong 1 0,75 (2,0 mol hợp chất điểm) + Bước 2: Tính số mol nguyên tử mỗi nguyên tố trong 1 0,75 mol hợp chất Suy ra số nguyên tử của mỗi nguyên tố trong 1 phân tử hợp chất + Bước 3: Viết công thức hóa học của hợp chất 0,5 11 -Khối lượng của mỗi nguyên tố có trong 1 mol khí A là: (2,0 điểm) 0,5 27,3.44 m 12(g) C 100 72,7.44 m 32(g) 0,5 -SốO mol100 của mỗi nguyên tố có trong 1 mol khí A là: m 12 n C 1(mol) 0,25 C MC 12 m 32 0,25 n O 2(mol) O 0,25 -Vậy,M trongO 16 1 mol phân tử khí A có 1 nguyên tử C và 2 nguyên tử O. 0,25 - CTHH của khí A là CO2. Tổng 10
Tài liệu đính kèm:
 2_de_kiem_tra_cuoi_hoc_ki_i_hoa_hoc_8_nam_hoc_2022_2023_truo.pdf
2_de_kiem_tra_cuoi_hoc_ki_i_hoa_hoc_8_nam_hoc_2022_2023_truo.pdf






