Tổng hợp Hidrocacbon
Bạn đang xem tài liệu "Tổng hợp Hidrocacbon", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
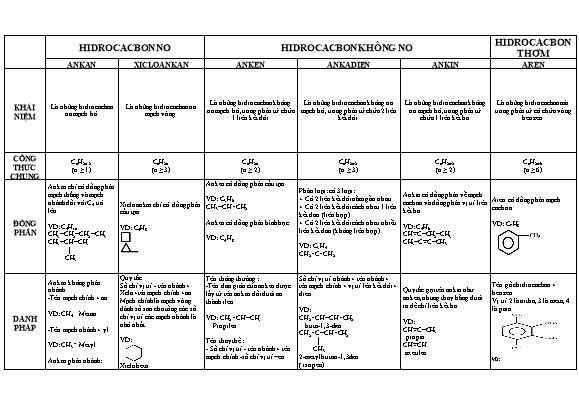
HIDROCACBON NO HIDROCACBON KHÔNG NO HIDROCACBON THƠM ANKAN XICLOANKAN ANKEN ANKADIEN ANKIN AREN KHÁI NIỆM Là những hidrocacbon no mạch hở. Là những hidrocacbon no mạch vòng. Là những hidrocacbon không no mạch hở, trong phân tử chứa 1 liên kết đôi. Là những hidrocacbon không no mạch hở, trong phân tử chứa 2 liên kết đôi. Là những hidrocacbon không no mạch hở, trong phân tử chứa 1 liên kết ba. Là những hidrocacbon mà trong phân tử có chứa vòng benzen. CÔNG THỨC CHUNG CnH2n+2 (n ≥ 1) CnH2n (n ≥ 3) CnH2n (n ≥ 2) CnH2n-2 (n ≥ 3) CnH2n-2 (n ≥ 2) CnH2n-6 (n ≥ 6) ĐỒNG PHÂN Ankan chỉ có đồng phân mạch thẳng và mạch nhánh đối với C4 trở lên. VD: C4H10 CH3−CH2−CH2−CH3 CH3−CH−CH3 | CH 3 Xicloankan chỉ có đồng phân cấu tạo. VD: C4H8 Anken có đồng phân cấu tạo. VD: C3H6 CH3−CH=CH2 Anken có đồng phân hình học. VD: C4H8 Phân loại: có 3 loại: + Có 2 liên kết đôi nằm gần nhau. + Có 2 liên kết đôi cách nhau 1 liên kết đơn (liên hợp). + Có 2 liên kết đôi cách nhau nhiều liên kết đơn (không liên hợp). VD: C3H4 CH2=C =CH2 Ankin có đồng phân về mạch cacbon và đồng phân vị trí liên kết ba. VD: C4 H6 CH≡C−CH2−CH3 CH3−C≡C−CH3 Aren có đồng phân mạch cacbon. VD: C 7H 8 DANH PHÁP Ankan không phân nhánh -Tên mạch chính + an. VD: CH 4 Metan. -Tên mạch nhánh + yl. VD: CH3 – Metyl. Ankan phân nhánh: - Số chỉ vị trí − Tên nhánh + tên mạch nhánh + an. VD: CH3−CH−CH3 │ CH3 2-metylpropan Quy tắc Số chỉ vị trí - tên nhánh + Xclo+tên mạch chính +an Mạch chính là mạch vòng . đánh số sao cho tổng các số chỉ vị trí các mạch nhánh là nhỏ nhất. VD: Xiclohexn Tên thông thường : -Tên đơn giản của anken được lấy từ tên ankan đổi đuôi an thành ilen. VD: CH2=CH−CH3 Propilen Tên thay thế : - Số chỉ vị trí - tên nhánh + tên mạch chính -số chỉ vị trí –en. VD: CH2 =CH2 eten Số chỉ vị trí nhánh + tên nhánh + tên mạch chính + vị trí lên kết đôi + đien. VD: CH2=CH−CH=CH2 buta-1,3-đien CH2=C−CH=CH2 │ CH3 2-metylbutan-1,3đien ( isopen) Quy tắc gọi tên ankin như anken, nhưng thay bằng đuôi in để chỉ liên kết ba. VD: CH≡C−CH3 propin CH≡CH axetilen Tên gốc hidrocacbon + benzen. Vị trí 2 là ortho, 3 là meta, 4 là para. VD: 1,2-đimetylbenzen o-đimetylbenzen TÍNH CHẤT HÓA HỌC 1.Phản ứng thế CH4+Cl2→ CH3Cl+HCl 2. Phản ứng tách a. Tách H2 CH3−CH3→ CH2=CH2+H2 b. Phản ứng Cracking c. Phản ứng cháy. PTTQ: CnH2n+2+O2 →nCO2+(n+1)H2O 1.Phản ứng thế 2.Phản ứng cộng 3.Phản ứng oxi hóa CnH2n+ O2 →nCO2+nH2O 1.Phản ứng cộng H2 CH2=CH2+H2→CH3−CH3 2. Phản ứng cộng với halogen a. Cộng Clo CH2=CH2+Cl2→CH2Cl−CH2Cl b. Cộng Br2 CH2=CH2+Br2→CH2Br−CH2Br 3. Phản ứng cộng với axit và cộng nước a . Cộng axit CH2=CH2+HCl→CH3CH2Cl b. Cộng nước CH2=CH2+H2O →CH3−CH2OH 4. Phản ứng trùng hợp nCH2=CH2 → (CH2−CH2 )n (polietilen) 5. Phản ứng oxi hóa CnH2n+2 +O 2→nCO2+n H2O * Anken làm mất màu KMnO4 1. Phản ứng cộng CH2=CH−CH=CH2 +H2→ CH3−CH2−CH2−CH3 CH2−CH−CH−CH2 +Br2→ CH2Br−CHBr−CH−CH3 2. Phản ứng trùng hợp nCH=CH−CH=CH2→ (CH2−CH=CH−CH2 )n 3. Phản ứng oxi hóa *Phản ứng làm mất màu KMnO 4 *Phản ứng cháy CnH2n -2+O2 → nCO2+(n-)H2O 1. Phản ứng cộng a.Cộng H2 CHCH +H2→CH2=CH2 CH2=CH2 +H2→C2H6 b. Cộng Brom CHCH+Br2 →CHBr=CHBr CHBr=CHBr+Br2→CHBr2−CHBr2 c. Cộng axit CHCH+HCl →CH2 =CHCl CH2=CHCl+HCl →CH3−CHCl2 d. Cộng nước CHCH+H2O →CH2=CH−OH e .Phản ứng điem hóa và trime hóa 2CH≡CH→CH2=CH−C≡CH 3CH≡CH→C6H6 2. Phản ứng thế bằng ion kim loại CH≡CH+2AgNO3+NH3 →CAg≡CAg+NH4NO3 *Chú ý: phản ứng chỉ xảy ra với ankin có H linh động. 3. Phản ứng oxi hóa CnH2n-2+O2 →nCO2+(n-1)H2O 1 . Phản ứng thế a. Phản ứng với halogen +Br2→+HBr b.Phản ứng nitro hóa +HO-NO2 → +H2O +HNO3 →+H2O Quy tắc thế vòng benzen ● Khi trên vòng benzen có nhóm đẩy e (OH-, NH2- , CH3-,...) ưu tiên cộng vào vị trí ortho và para. ● Khi trên vòng benzen có nhóm hút e ( NO2-,COOH- ,...) ưu tiên cộng vào vị trí meta . 2. Phản ứng cộng C 6H6 + 3H2 →C6H12 3. Phản ứng oxi hóa ● Benzen không tác dụng với KMnO4 . Các ankylbenzen tác dụng với KMnO4 ở nhiệt độ cao. C6H5CH C6H5− C−OK || O C6H5 −C−OH ║ O ● C6H6 +O2 →6CO2 +3H2O ĐIỀU CHẾ a. Trong công nghiệp Metan và các đồng đẳng được tách từ dầu mỏ. b. Trong phòng thí nghiệm Al3C4+12H2O→3CH4+4Al(OH)3 Xicloankan được tách từ ankan. CH3[CH2]4CH3 →+H2 Trong phòng thí nghiệm . Đun nóng ancol với axit sunfuric đặc. CH3CH2OH CH2=CH2 + H2O Trong công nghiệp −Tách hidro từ ankan tương ứng hoặc bằng phản ứng cacking. Tách hidro ankan tương ứng CH3CH2CH2CH3 → CH2=CH−CH=CH2+2H2 CH3−CH−CH2−CH3 | → CH3 CH2=C−CH=CH2+2H2 | CH3 Trong công nghiệp : nhiệt phân metan ở 1500 C 2CH4 CH≡CH+3H 2 CaO+3C →CaC2 →Ca(OH)2+C2H2 Benzen , toluen ... thường được tách bằng chưng cất dầu mỏ CH3[CH2]4CH3 → C6H6 Etylbenzen được điều chế từ benzen và etilen. C6H6+CH2=CH2 → C6H5CH2CH3
Tài liệu đính kèm:
 tong_hop_hiddrocacbon.docx
tong_hop_hiddrocacbon.docx





