Lí thuyết và bài tập Hóa học Lớp 9 - Bài 45: Acetic acid
Bạn đang xem 20 trang mẫu của tài liệu "Lí thuyết và bài tập Hóa học Lớp 9 - Bài 45: Acetic acid", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
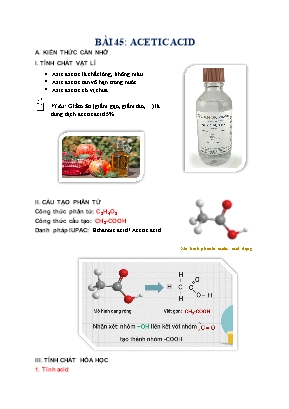
BÀI 45: ACETIC ACID A. KIẾN THỨC CẦN NHỚ I. TÍNH CHẤT VẬT LÍ Axit axetic là chất lỏng, không màu. Axit axetic tan vô hạn trong nước. Axit axetic có vị chua. Ví dụ: Giấm ăn (giấm gạo, giấm táo,) là dung dịch acetic acid 5%. II. CẤU TẠO PHÂN TỬ Công thức phân tử: C2H4O2 Công thức cấu tạo: CH3-COOH Danh pháp IUPAC: Ethanoic acid / Acetic acid Mô hình phân tử acetic acid dạng rỗng III. TÍNH CHẤT HÓA HỌC 1. Tính acid Acetic acid là một acid hữu cơ, có đầy đủ tính chất của một acid. a) Tác dụng với quì tím Acetic acid làm quì tím hóa hồng. Acetic acid làm giấy pH đổi sang màu da cam b) Tác dụng với kim loại PTHH: 2CH3COOH + Mg → (CH3COO)2Mg + H2 c) Tác dụng với base PTHH: CH3COOH + NaOH → CH3COONa + H2O d) Tác dụng với basic oxide PTHH: 2CH3COOH + CuO → (CH3COO)2Cu + H2O e) Tác dụng với muối PTHH: Acetic acid tác dụng Mg Acetic acid tác dụng Cu(OH)2 Acetic acid tác dụng Na2CO3 2CH3COOH + Na2CO3 → 2CH3COONa + H2O + CO2 H2SO4 đặc, to Acetic acid tác dụng Mg 2. Tác dụng với ethanol PTHH: CH3COOH + C2H5OH ⇌ CH3COOC2H5 + H2O Đun nóng hỗn hợp acetic acid và ethanol thu được chất lỏng không màu có mùi thơm không tan trong nước, nổi lên trên mặt nước. IV. ỨNG DỤNG V. ĐIỀU CHẾ B. BÀI TẬP I. PHẦN TRẮC NGHIỆM Câu 1. Công thức phân tử của acetic acid là A. CH4O. B. C2H4O2. Mô hình acetic acid dạng đặc C. C2H6O. Acetic acid tác dụng Na2CO3 D. C3H8O. Câu 2. Công thức cấu tạo của acetic acid là A. CH3OH. B. CH3COOH. C. C2H5OH. D. C2H5OCH3. Câu 3. Hợp chất CH3COOH có tên gọi theo danh pháp IUPAC là A. ethanol. B. ethanoic acid. C. methane. D. ethene. Câu 4. Nhiệt độ sôi của acetic acid (CH3COOH) tuyệt đối là A. 1120C. B. 1180C. C. 112,50C D. 116,50C. Câu 5. Đối với các bà nội trợ, công việc khó khăn nhất mỗi ngày chính là giữ cho tổ ấm của mình luôn sáng bóng và sạch sẽ. Một trong những trợ thủ đắc lực trong việc làm sạch ngôi nhà của bạn, đó chính là giấm. Giấm có thể loại bỏ đi các vết bẩn cứng đầu một cách nhanh chóng. Bạn dùng một khăn sạch nhúng vào dung dịch giấm, sau đó chà mạnh lên bộ đồng. Hay bạn hòa trộn hỗn hợp giấm và nước ấm để lau đồ gỗ. Đảm bảo sẽ đánh bay các vết bẩn và giúp đồ đồng và đồ gỗ sáng bóng hơn. Ngâm quần áo bị dính vết bẩn trong thau đã pha loãng dung dịch nước, giấm và để qua đêm. Sau đó, bạn giặt lại bình thường. Các vết bẩn sẽ được vệ sinh sạch sẽ. Trong hình bên là sự kết hợp giấm với với một chất bột màu trắng. Trộn giấm với chất này bạn sẽ có một hỗn hợp tuyệt vời để đánh rửa nhà vệ sinh khỏi những vết ố vàng trên các vật dụng trong nhà tắm như vòi nước, giá inox hay bồn cầu, bồn rửa. Chất bột trắng đó là A. muối ăn B. đường C. baking soda D. bột mì Câu 6. Nhóm –COOH trong phân tử acetic acid (CH3COOH) có tính chất hóa học đặc trưng là A. tác dụng được với kim loại giải phóng khí hydrogen. B. tác dụng được với sodium, potasium giải phóng khí hydrogen. C.tác dụng được với magnesium, sodium giải phóng khí hydrogen. D. tác dụng được với potasium, zinc giải phóng khí hydrogen. Câu 7. Cho bộ dụng cụ và hóa chất như trong hình 1. Hiện tượng xảy ra khi cho các chất phản ứng với nhau là A. dung dịch trong suốt không màu. B. sủi bọt khí và xuất hiện kết tủa trắng. Hình 1. C. sủi bọt khí không màu. D. dung dịch vẩn đục. Câu 8. Một bạn học sinh tiến hành thí nghiệm giữa hai hóa chất X và Y. Hiện tượng quan sát được như trong hình 2. Các chất X, Y bạn học sinh đã sử dụng là A. CH3OH và NaOH. Hình 2. B. CH3COOH và Na2CO3. C. CH3COOH và Cu. D. CH3COOH và Cu(OH)2. Câu 9. Acetic acid tác dụng với kim loại zinc (Zn) vì A. trong phân tử có nhóm -COOH B. trong phân tử có nguyên tử hydrogen và oxygen. C. trong phân tử có nguyên tử carbon, hydrogen và oxygen. D. trong phân tử có nhóm -OH. Câu 10. Phân tử acetic acid có cấu tạo gồm A. nhóm ethyl (C2 H5) liên kết với nhóm – COOH. B. nhóm methyl (CH3) liên kết với nhóm – COOH. C. nhóm hydrocarbon liên kết với nhóm – OH. D. nhóm methyl (CH3) liên kết với nguyên tử oxygen. Câu 11. Tính chất vật lý đúng của acetic acid (CH3COOH) là A. chất lỏng không màu, nhẹ hơn nước, có vị chua, tan vô hạn trong nước B. chất lỏng màu hồng, nhẹ hơn nước, tan vô hạn trong nước C. chất lỏng màu xanh, nhẹ hơn nước, có vị chua, tan vô hạn trong nước D. chất lỏng không màu, nặng hơn nước, tan vô hạn trong nước Câu 12. Hợp chất hữu cơ X là một chất lỏng trong suốt không màu. X phản ứng với giấy quì tím cho hiện tượng như trong hình 3. Chất lỏng X trong cốc thí nghiệm là A. C6H6. B. CH3COOH. Hình 3. C. CH3COOC2H5. D. C2H5OH. Câu 13. Hợp chất Y là chất lỏng không màu, có nhóm –COOH trong phân tử, vừa tác dụng với magnesium vừa tác dụng với sodium hydroxide. Y là A. NaOH. B. CH3COOH. C. Ca(OH)2. D. C2H5OH. Câu 14. Cho một mẫu sodium vào ống nghiệm đựng acetic acid. Hiện tượng quan sát được là A. có bọt khí màu nâu thoát ra. B. mẫu sodium tan dần không có bọt khí thoát ra. C. mẫu sodium nằm dưới bề mặt chất lỏng và không tan. D. có bọt khí không màu thoát ra và sodium tan dần. Câu 15. Acetic acid (CH3COOH) tác dụng được với tất cả các chất trong dãy là A. NaOH; K; C2H5OH; O2. B. Na; K; CH3COOH; O2. C. C2H4; Na; CH3COOH; O2. D. Ca(OH)2; K; CH3COOH; O2. Câu 16. Giấm là gia vị khá quen thuộc trong căn bếp của người dân Việt Nam. Những kinh nghiệm và nghiên cứu lâu đời đã chỉ ra giấm có những tác dụng tuyệt vời đối với sức khỏe và đời sống. 1. Làm salad: Một vài giọt giấm trắng có thể làm dậy lên hương vị đặc trưng của một số loại salad truyền thống. Giấm giúp tăng khả năng hấp thụ calcium trong rau xà lách. 2. Làm nước xốt: Giấm trắng làm tăng thêm hương vị cho món nước sốt. Ngoài ra, axit trong giấm cũng có chức năng như một chất làm mềm cho thịt, hải sản và rau quả, vì vậy có thể cho vào quá trình ướp gia vị trước khi chế biến món ăn. 3. Dùng cho món nướng: Giấm trắng có thể được sử dụng cùng với baking soda như một tác nhân lên men cho các món ăn nướng. Giấm có tính axit sẽ phản ứng với baking soda có tính kiềm và giải phóng khí carbon dioxide giúp món nướng có hương vị ngon hơn. 3. Làm phô mai: Một số loại phô mai có thể được chế biến từ sữa và giấm trắng. Khi được thêm vào sữa, giấm có tính axit làm thay đổi protein sữa, cho phép sữa đông lại và váng sữa tách ra. Kết quả là chế biến ra một loại phô mai nhẹ, mềm và thơm ngon. 4. Là phương án giảm cân và làm đẹp hiệu quả: Những acid amin có trong giấm giúp đẩy nhanh quá trình trao đổi chất, hạn chế sự hình thành, tích tụ của mỡ thừa. Vì vậy muốn giảm cân nhanh chóng có thể uống một lượng lớn giấm hàng ngày. Qua nội dung trên, các phát biểu đúng là A. 1, 2, 4. B. 1, 3, 4 C. 1, 2, 3. D. 2, 3, 4. Câu 17. Acetic acid (CH3COOH) tác dụng tất cả các chất trong dãy là A. Na, O2. B. CH3COOH, C2H4. C. H2O, Na. D. O2, CH4. Câu 18. Chất không tác dụng được với acetic acid (CH3COOH) là A. O2. B. C2H5OH. C. H2O. D. Mg. Câu 19. Trong công nghiệp để sản xuất acetic acid, người ta sản xuất từ buthane theo phương trình phản ứng là A. C2H5OH+ O2 men giấm CH3COOH + H2O. B. 2C4H10 + 5O2 xt, to 4CH3COOH + 2H2O. C. C4H10 + Cl2 as C4H9Cl + HCl. D. 2CH3CHO + O2 xt, to 2CH3COOH. Câu 20. Chất không tác dụng được với acetic acid (CH3COOH) là A. Na. B. CaO. C. CaCO3. D. CuCl2. Câu 21. Hòa tan hoàn toàn một mẫu đá vôi vào dung dịch acetic acid thu được khí CO2 thoát ra. Sản phẩm thu được chứa muối calcium acetate. Tổng hệ số cân bằng tối giản trong phương trình hóa học của phản ứng xảy ra là A. 6. B. 5. C. 8. D. 7. Lên men giấm bỗng từ alcohol Câu 22. Giấm bỗng (hay dấm bỗng, bỗng rượu) là loại gia vị truyền thống của người miền Bắc, được sử dụng tương tự như giấm gạo. Sử dụng giấm bỗng an toàn hơn rất nhiều so với các loại giấm công nghiệp, cách làm giấm nuôi bằng rượu cũng không khó. Phương trình hóa học của phản ứng lên men giấm bỗng từ ethanol là A. C2H5OH+ O2 men giấm CH3COOH + H2O B. 2C4H10 + 5O2 xt, to 4CH3COOH + 2H2O C. C2H4 + H2 xt, to C2H6. D. 2C2H5OH + 2Na → 2C2H5ONa + H2. Câu 23. Ngâm giấm hoa quả là phương pháp bảo quản tự nhiên, giúp giữ được độ tươi, màu sắc cũng như hàm lượng dinh dưỡng có trong hoa quả. Thường các loại rau quả sẽ được ngâm trong giấm cùng với muối đường và một số gia vị và đóng trong trong lọ thủy tinh hoặc hũ nhựa để bảo quản. Trong môi trường acetic acid loãng sẽ giúp làm tăng hương vị sản phẩm, ức chế nha bào của nhiều loại vi khuẩn giúp sản phẩm ngâm giấm hoa quả được bảo quản lâu hơn, tốt hơn. Theo thời gian thì nước giấm sẽ thấm vào bên trong nguyên liệu ngày càng nhiều, tạo được cấu trúc giòn dai cho nguyên liệu. Vì thế để càng lâu thì hương vị của món ngâm giấm hoa quả lại càng thơm ngon, hấp dẫn. Giấm ăn dùng để ngâm hoa quả là dung dịch acetic acid có nồng độ A. trên 5%. B. dưới 2%. C. từ 2% - 5%. Trái cây ngâm giấm D. từ 3% - 6%. Câu 24. Phản ứng giữa acetic acid với dung dịch base thuộc loại A. phản ứng oxi hóa - khử. B. phản ứng hóa hợp. C. phản ứng phân hủy. D. phản ứng trung hòa. Câu 25. Trong công nghiệp một lượng lớn acetic acid được điều chế bằng cách A. oxi hóa methane có xúc tác và nhiệt độ thích hợp. B. oxi hóa ethylene có xúc tác và nhiệt độ thích hợp. C. oxi hóa ethane có xúc tác và nhiệt độ thích hợp. D. oxi hóa buthane có xúc tác và nhiệt độ thích hợp. Câu 26. Axit axetic tác dụng với zinc (Zn) giải phóng khí là A. hydrogen (H2). B. hydrogen chloride (HCl). C. hydrogen sulfide (H2S). D. ammonia (NH3). Câu 27. Phương trình phản ứng sản xuất acetic acid trong công nghiệp là Xúc tác, t0 C4H10 + O2 CH3COOH + H2O Tổng hệ số trong phương trình hóa học trên là A. 11. B. 12. C. 13. D. 14. Câu 28. Để phân biệt dung dịch CH3COOH và C2H5OH ta dùng kim loại là A. Na. B. Zn. C. K. D. Cu. Câu 29. Dung dịch tác dụng được với CaO, CaCO3 nhưng không tác dụng được với dung dịch AgNO3 là A. NaOH. B. HCl. C. CH3COOH. D. C2H5OH. Câu 30. Cặp chất khi trộn lẫn vào nhau có phản ứng xảy ra và sinh ra khí CO2 là A. CH3COOH và ZnO. B. CH3COOH và Zn(OH)2. C. CH3COOH và ZnCO3. D. CH3COONa và K2SO4. Câu 31. Cho thêm Cu(OH)2 vào hai ống nghiệm đựng CH3COOH (ống 1) và C2H5OH (ống 2). Hiện tượng chứng tỏ ống 1 là acid CH3COOH và ống 2 là alcohol C2H5OH là A. ống 1: dung dịch có màu xanh; ống 2: không hiện tượng. B. ống 1: dung dịch chuyển màu vàng nâu; ống 2: có kết tủa trắng. C. ống 1: kết tủa tan dần; ống 2: sủi bọt khí. D. ống 1: dung dịch có màu xanh; ống 2: kết tủa tan dần. Câu 32. Cho dung dịch chứa 10 gam CH3COOH tác dụng với dung dịch chứa 10 gam KOH. Sau khi phản ứng hoàn toàn dung dịch chứa các chất tan là A. CH3COOK và KOH. B. CH3COOK và CH3COOH. C. CH3COOK. D. CH3COOK, CH3COOH và KOH. Câu 33. Hòa tan hoàn toàn 6,5 gam Zn vào dung dịch CH3COOH. Thể tích khí H2 thoát ra (đkc) là A. 0,61975 lít. B. 1,2395 lít. C. 2,479 lít. D. 3,7185 lít. Câu 34. Trung hòa 400 ml dung dịch acetic acid 0,5M bằng dung dịch NaOH 0,5M. Thể tích dung dịch NaOH cần dùng là A. 100 ml. B. 200 ml. C. 300 ml. D. 400 ml. Câu 35. Cho acetic acid tác dụng với ethyl alcohol có mặt H2SO4 đặc làm xúc tác và đun nóng. Sau phản ứng thu được 44 gam ethyl acetate. Khối lượng CH3COOH và C2H5OH đã phản ứng là A. 60 gam và 46 gam. B. 30 gam và 23 gam. C. 15 gam và 11,5 gam. D. 45 gam và 34,5 gam. Câu 36. Biết tỉ khối hơi của X so với khí H2 là 30. Công thức phân tử của X là A. C2H4O2. B. C4H8O2. C. CH4O. D. CH2O. Câu 37. Đốt cháy hoàn toàn 6 gam acetic acid (CH3COOH) thu được CO2 và nước. Thể tích khí carbonic thu được ở đkc là A. 4,958 lít. B. 24,79 lít. C. 9,916 lít. D. 11,1555 lít. Câu 38. Cho 18 gam acetic acid (CH3COOH) nguyên chất tác dụng với sodium dư. Thể tích khí H2 thoát ra (đkc) là A. 3,09875 lít. B. 3,7185 lít. C. 9,29625 lít. D. 12,395 lít. Câu 39. Thể tích khí oxygen (đkc) cần dùng để đốt cháy hoàn toàn 9 gam acetic acid (CH3COOH) nguyên chất là A. 14,874 lít. B. 7,437 lít. C. 22,311 lít. D. 23,164 lít. Câu 40. Thể tích không khí (đkc) (chứa 20% thể tích oxygen) cần dùng để đốt cháy hoàn toàn 22,5 gam acetic acid (CH3COOH) nguyên chất là A. 92,9625 lít. B. 9,29625 lít. C. 3,1785 lít. D. 31,785 lít. II. PHẦN TỰ LUẬN Câu 1. Giấm được ví như một loại “thuốc tiên” có công dụng vô tận. Nó không chỉ là một gia vị tuyệt vời mà còn được sử dụng như một chất tẩy rửa tự nhiên an toàn và hiệu quả. Thành phần hóa học chính trong giấm là acetic acid. Acid này có thể tác dụng được với các nhiều chất như calcium, zinc, magnesium oxide, potasium hydroxide, potasium carbonate. Em hãy viết các phương trình hóa học các phản ứng minh họa tính chất của acetic acid. Câu 2. Hoàn thành các phương trình hóa học (Mỗi chỗ trống là 1 chất) a) .. + Na → CH3COONa + .. b) CH3COOH + . → (CH3COO)2Ca + H2O c) . + .. → CH3COOC2H5 + H2O d) CH3COOH + CuO → + . e) C2H5OH + . → CH3COOH + f) + O2 → CH3COOH + H2O Câu 3. Viết phương trình hóa học hoàn thành sơ đồ phản ứng a) CH4 → C2H2 → C2H4 → C2H5OH → CH3COOH → CH3COONa b) C6H12O6 → C2H5OH → C2H4 → C2H5OH → CH3COOC2H5 c) C2H2 → CH3CHO → CH3COOH → CO2 Câu 4. Giấm táo là loại thực phẩm quen thuộc và phổ biến với nhiều gia đình người Việt. Giấm táo còn được biết đến với nhiều tên gọi khác nhau như giấm rượu táo hay ACV. Đây là một loại giấm được làm từ rượu táo hoặc táo tươi. Loại giấm này không chỉ chứa nhiều vitamin hữu ích cho sức khỏe mà còn có hương vị hấp dẫn. Giấm táo được điều chế bằng cách ngâm táo với đường vào để quá trình lên men diễn ra tự nhiên. Em hãy viết các phương trình hóa học các phản ứng chính diễn ra khi làm giấm táo. Câu 5. Cho dung dịch chứa 10 gam hỗn hợp X gồm C2H5OH và CH3COOH tác dụng với Zn dư, thu được 1,2395 lít khí H2 (đkc). Tính thành phần phần trăm theo khối lượng của mỗi chất trong hỗn hợp X. Câu 6. Cho 16,6 gam hỗn hợp Y gồm HCOOH, CH3COOH tác dụng hết với Mg, thu được 3,7185 lít H2 (đkc). Tính thành phần phần trăm về số mol mỗi chất trong Y. Câu 7. Cho 60 gam acetic acid tác dụng với ethanol dư có mặt H2SO4 đặc làm xúc tác và đun nóng. Sau phản ứng thu được 66 gam ethyl acetate. a) Tính khối lượng C2H5OH đã phản ứng. b) Tính hiệu suất của phản ứng. Câu 8. Cho dung dịch CH3COOH 0,5M tác dụng với Na2CO3 vừa đủ thu được 4,958 lít khí CO2 (đkc). a) Tính thể tích của dung dịch CH3COOH đã phản ứng. b) Trung hòa lượng acid trên bằng dung dịch NaOH thì thấy hết 200 ml dung dịch NaOH. Tính nồng độ NaOH đã dùng. Câu 9. Hòa tan hoàn toàn 4,02 gam hỗn hợp X gồm CuO và ZnO (có tỉ lệ mol 3:2) vào dung dịch giấm ăn (chứa CH3COOH 5%) thu được dung dịch Y. a) Tính thành phần phần trăm khối lượng mỗi oxide trong hỗn hợp X. b) Tính khối lượng dung dịch CH3COOH cần dùng. Câu 10. Hòa tan 20 gam CaCO3 vào một lượng vừa đủ dung dịch CH3COOH 0,1M thu được khí carbonic. a) Tính thể tích khí CO2 thoát ra ở đkc. b) Tính thể tích dung dịch acid đã dùng. -----HẾT---- C. ĐÁP ÁN I. PHẦN TRẮC NGHIỆM 1 2 3 4 5 6 7 8 9 10 B B B B C B B B A B 11 12 13 14 15 16 17 18 19 20 A B B B A A C B D 21 22 23 24 25 26 27 28 29 30 A A C D D A C B C C 31 32 33 34 35 36 37 38 39 40 A A C D B A A B B A Hướng dẫn giải trắc nghiệm Câu 1. Công thức phân tử của acetic acid là → Chọn B. C2H4O2. Câu 2. Công thức cấu tạo của acetic acid là → Chọn B. CH3COOH. Câu 3. Hợp chất CH3COOH có tên gọi theo danh pháp IUPAC là → Chọn B. ethanoic acid. Câu 4. Nhiệt độ sôi của acetic acid (CH3COOH) tuyệt đối là → Chọn B. 1180C. Câu 5. Chất bột trắng đó là → Chọn C. baking soda Câu 6. Nhóm –COOH trong phân tử acetic acid (CH3COOH) có tính chất hóa học đặc trưng là → Chọn B. tác dụng được với sodium, potasium giải phóng khí hydrogen. Câu 7. Cho bộ dụng cụ và hóa chất như trong hình 1. Hiện tượng xảy ra khi cho các chất phản ứng với nhau là → Chọn B. sủi bọt khí và xuất hiện kết tủa trắng. Phương trình hóa học giải thích hiện tượng CH3COOH + Na2CO3 → CH3COONa + CO2↑ + H2O Câu 8. Một bạn học sinh tiến hành thí nghiệm giữa hai hóa chất X và Y. Hiện tượng quan sát được như trong hình 2. Các chất X, Y bạn học sinh đã sử dụng là → Chọn B. CH3COOH và Na2CO3. Câu 9. Acetic acid tác dụng với kim loại zinc (Zn) vì → Chọn A. trong phân tử có nhóm -COOH Câu 10. Phân tử acetic acid có cấu tạo gồm → Chọn B. nhóm methyl (CH3) liên kết với nhóm – COOH. Câu 11. Tính chất vật lý đúng của acetic acid (CH3COOH) là → Chọn A. chất lỏng không màu, nhẹ hơn nước, có vị chua, tan vô hạn trong nước Câu 12. Hợp chất hữu cơ X là một chất lỏng trong suốt không màu. X phản ứng với giấy quì tím cho hiện tượng như trong hình 3. Chất lỏng X trong cốc thí nghiệm là → Chọn B. CH3COOH. Lời giải CH3COOH làm quỳ tím hóa hồng Câu 13. Hợp chất Y là chất lỏng không màu, có nhóm –COOH trong phân tử, vừa tác dụng với magnesium vừa tác dụng với sodium hydroxide. Y là → Chọn B. CH3COOH. Lời giải CH3COOH + Mg → (CH3COO)2Mg + H2↑ CH3COOH + NaOH → CH3COONa + H2O Câu 14. Cho một mẫu sodium vào ống nghiệm đựng acetic acid. Hiện tượng quan sát được là → Chọn B. mẫu sodium tan dần không có bọt khí thoát ra. Lời giải CH3COOH + Na → CH3COONa + H2↑ Câu 15. Acetic acid (CH3COOH) tác dụng được với tất cả các chất trong dãy là → Chọn A. NaOH; K; C2H5OH; O2. Lời giải NaOH + CH3COOH → CH3COONa + H2O CH3COOH + K → CH3COOK + H2↑ CH3COOH + C2H5OH → CH3COOC2H5 + H2O CH3COOH + O2 → CO2↑ + H2O Câu 16. Qua nội dung trên, các phát biểu đúng là → Chọn C. 1, 2, 3. Phát biểu 4. Sai vì muốn giảm cân nhanh chóng có thể uống một lượng lớn giấm hàng ngày. Như vậy sẽ không tốt cho sức khỏe. Câu 17. Acetic acid (CH3COOH) tác dụng tất cả các chất trong dãy là → Chọn A. Na, O2. Câu 18. Chất không tác dụng được với acetic acid (CH3COOH) là → Chọn C. H2O. Câu 19. Trong công nghiệp để sản xuất acetic acid, người ta sản xuất từ buthane theo phương trình phản ứng là → Chọn B. Lời giải 2C4H10 + 5O2 xt, to 4CH3COOH + 2H2O. Câu 20. Chất không tác dụng được với acetic acid (CH3COOH) là → Chọn D. CuCl2. Câu 21. Chọn A. 6. Lời giải CaCO3 + 2CH3COOH → (CH3COO)2Ca + CO2↑+ H2O Câu 22. Phương trình hóa học của phản ứng lên men giấm bỗng từ ethanol là → Chọn A. C2H5OH+ O2 men giấm CH3COOH + H2O Câu 23. Giấm ăn dùng để ngâm hoa quả là dung dịch acetic acid có nồng độ → Chọn C. từ 2% - 5%. Câu 24. Phản ứng giữa acetic acid với dung dịch base thuộc loại → Chọn D. phản ứng trung hòa. Câu 25. Trong công nghiệp một lượng lớn acetic acid được điều chế bằng cách → Chọn D. oxi hóa buthane có xúc tác và nhiệt độ thích hợp. Lời giải 2C4H10 + 5O2 xt, to 4CH3COOH + 2H2O Câu 26. Axit axetic tác dụng với zinc (Zn) giải phóng khí là → Chọn A. hydrogen (H2). Lời giải 2CH3COOH + Zn → (CH3COO)2Zn + H2 Câu 27. Chọn C. 13. Lời giải 2C4H10 + 5O2 xt, to 4CH3COOH + 2H2O Câu 28. Để phân biệt dung dịch CH3COOH và C2H5OH ta dùng kim loại là → Chọn B. Zn. Lời giải CH3COOH tác dụng với Zn có hiện tượng sủi bọt khí H2 C2H5OH không có hiện tượng Câu 29. Dung dịch tác dụng được với CaO, CaCO3 nhưng không tác dụng được với dung dịch AgNO3 là → Chọn C. CH3COOH. Câu 30. Cặp chất khi trộn lẫn vào nhau có phản ứng xảy ra và sinh ra khí CO2 là → Chọn C. CH3COOH và ZnCO3. Lời giải 2CH3COOH + ZnCO3 → (CH3COO)2Zn + CO2 + H20 Câu 31. Cho thêm Cu(OH)2 vào hai ống nghiệm đựng CH3COOH (ống 1) và C2H5OH (ống 2). Hiện tượng chứng tỏ ống 1 là acid CH3COOH và ống 2 là alcohol C2H5OH là → Chọn A. Ống 1: dung dịch có màu xanh; Ống 2: không hiện tượng. Câu 32. Chọn A. CH3COOK và KOH. Lời giải nCH3COOH=1060=16 (mol) nKOH= 1056=0, 179 (mol) CH3COOH + KOH → CH3COOK + H2O Ta thấy: nKOH>nCH3COOH→KOH dư, dung dịch sau phản ứng có CH3COOK và KOH Câu 33. Chọn C. 2,479 lít. Lời giải nZn=6,565=0,1 (mol) 2CH3COOH + Zn → (CH3COO)2Zn + H2 0,2← 0,1 →0,1 VH2=0,1. 24, 79=2,479 (l) Câu 34. Chọn D. 400 ml. Lời giải nCH3COOH=0,4.0,5=0,2 (mol) CH3COOH + NaOH → CH3COONa + H2O 0,2 →0,2 VNaOH=0,20,5=0,4 l=400(ml) Câu 35. Chọn B. 30 gam và 23 gam. Lời giải CH3COOH + C2H5OH → CH3COOC2H5 + H2O 0,5← 0,5← 0,5 nethyl acetate=4488=0,5 (mol) mCH3COOH=0,5. 60=30(g) mC2H5OH=0,5. 46=23(g) Câu 36. Chọn A. C2H4O2. Lời giải dXH2=30 →mX=30. 2=60 Câu 37. Chọn A. 4,958 lít. Lời giải nCH3COOH=660=0,1 (mol) CH3COOH + 2O2 → 2CO2 + 2H2O 0,1 →0,2 VCO2=0,2. 24, 79=4,958 (l) Câu 38. Chọn B. 3,7185 lít. Lời giải nCH3COOH=1860=0,3 (mol) CH3COOH + Na → CH3COONa + 12H2 0,3 →0,15 VO2=0,15. 24, 79=3, 7185 (l) Câu 39. Chọn B. 7,437 lít. Lời giải nCH3COOH=960=0,15 (mol) CH3COOH + 2O2 → 2CO2 + 2H2O 0,15 →0,3 VO2=0,3. 24, 79=7, 437 (l) Câu 40. Chọn A. 92,9625 lít. Lời giải nCH3COOH=22,560=0,375 (mol) CH3COOH + 2O2 → 2CO2 + 2H2O 0,375 →0,75 VKK=0,75. 24, 79.10020=92, 9625 (l) II. PHẦN TỰ LUẬN Câu 1. Lời giải Acid này có thể tác dụng được với các nhiều chất như calcium, zinc, magnesium oxide, potasium hydroxide, potasium carbonate. Các phương trình hóa học các phản ứng minh họa tính chất của acetic acid. 2CH3COOH + Ca → (CH3COO)2Ca + H2 2CH3COOH + Zn → (CH3COO)2Zn + H2 2CH3COOH + MgO → (CH3COO)2Mg + H2O CH3COOH + KOH → CH3COOK + H2O 2CH3COOH + K2CO3 → 2CH3COOK + H2O + CO2 Câu 2. Hoàn thành các phương trình hóa học (Mỗi chỗ trống là 1 chất) a) CH3COOH + Na → CH3COONa + 12 H2 b) 2CH3COOH + Ca(OH)2 → (CH3COO)2Ca + 2H2O c) CH3COOH + C2H5OH → CH3COOC2H5 + H2O d) CH3COOH + CuO → (CH3COO)2Cu + H2O e) C2H5OH + O2 → CH3COOH + H2O g) 2C4H10 + 5O2 xt, to 4CH3COOH + 2H2O Câu 3. Viết phương trình hóa học hoàn thành sơ đồ phản ứng a) CH4 → C2H2 → C2H4 → C2H5OH → CH3COOH → CH3COONa 2CH4 1500OC, làm lạnh nhanh C2H2 + 3H2 C2H2 + H2 Ni, to C2H4 CH2=CH2 + H2O → CH3 – CH2OH C2H5OH + O2lên men CH3COOH + H2O CH3COOH + Na → CH3COONa + 12H2 b) C6H12O6 → C2H5OH → C2H4 → C2H5OH → CH3COOC2H5 C6H12O6 lên men C2H5OH + CO2 C2H5OH H2SO4 CH2=CH2 + H2O CH2=CH2 + H2O → CH3 – CH2OH C2H5OH + CH3COOH → CH3COOC2H5 + H2O c) C2H2 → CH3CHO → CH3COOH → CO2 C2H2 + H2O → CH3CHO CH3CHO + 12O2 → CH3COOH CH3COOH + 2O2 → 2CO2 + 2H2O Câu 4. Lời giải C6H12O6 lên men 2C2H5OH + 2CO2 C2H5OH + O2 → CH3COOH + H2O Câu 5. Lời giải Do C2H5OH không phản ứng với Zn nH2=1, 239524,79=0,05 (mol) 2CH3COOH + Zn → (CH3COO)2Zn + H2 0,1 ← 0,05 %mCH3COOH=0,1. 6010.100=60%→%mC2H5OH=100-60=40% Câu 6. Lời giải Gọi số mol của HCOOH và CH3COOH lần lượt là x và y 2HCOOH + Mg → (HCOO)2Mg + H2 x →0,5x 2CH3COOH+ Mg → (CH3COO)2Mg + H2 y →0,5y nH2=3,718524,79=0.15 (mol) 46x+60y=16,60,5x+0,5y=0,15→x=0,1y=0,2 %molHCOOH=0,10,1+0,2.100=33,33% %molCH3COOH=100-33,33=66,67% Câu 7. Lời giải nCH3COOH=6060=1 (mol) CH3COOH + C2H5OH ⇌ CH3COOC2H5 + H2O 1 →1 →1 mC2H5OH=1.46=46 g mester lý thuyết=1. 88=88(g) H=mthực tếmlý thuyết.100%=6688.100=75% Câu 8. Lời giải nCO2=4,95824,79=0,2 (mol) 2CH3COOH + Na2CO3 → 2CH3COONa + CO2 + H2O 0,4← 0,2 VCH3COOH=0,40,5=0,8 lít=800 (ml) Ta có phương trình CH3COOH + NaOH → CH3COONa + H2O 0,4 →0,4 CMNaOH=0,40,2=2M Câu 9. Lời giải 2CH3COOH + CuO → (CH3COO)2Cu + H2O 0,06 ← 0,03 mol 2CH3COOH + ZnO → (CH3COO)2Zn + H2O 0,04 ← 0,02 mol Gọi số mol CuO và ZnO là x, y mol 80x+81y=4,02xy=32⇒ x=0,03y=0,02 a) %mCuO=0,03.804,02. 100%=59,7% %mZnO=100%-59,7%=40,3% b) nCH3COOH=0,06+0,04=0,1 mol ⇒ mCH3COOH= 0,1. 60=6 gam Câu 10. Lời giải nCaCO3=20100=0,2 (mol) CaCO3 + 2CH3COOH → (CH3COO)2Ca + CO2 + H2O 0,2 → 0,4 → 0,2 VCO2=0,2. 24,79=4,958 (lít) VCH3COOH=0,40,1=4 (lít)
Tài liệu đính kèm:
 li_thuyet_va_bai_tap_hoa_hoc_lop_9_bai_45_acetic_acid.docx
li_thuyet_va_bai_tap_hoa_hoc_lop_9_bai_45_acetic_acid.docx





