Kiểm tra một tiết (bài số 1) môn: Hóa học - Lớp 9
Bạn đang xem tài liệu "Kiểm tra một tiết (bài số 1) môn: Hóa học - Lớp 9", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
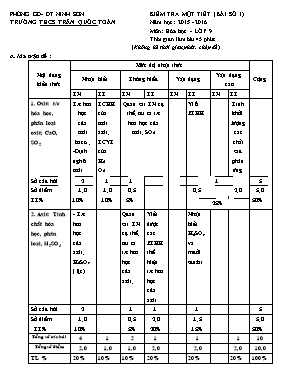
PHỊNG GD- ĐT NINH SƠN KIỂM TRA MỘT TIẾT (BÀI SỐ 1) TRƯỜNG THCS TRẦN QUỐC TOẢN Năm học: 2015 - 2016 Mơn: Hĩa học - LỚP 9 Thời gian làm bài 45 phút (Khơng kể thời gian phát, chép đề) A. Ma trận đề : Nội dung kiến thức Mức độ nhận thức Cộng Nhận biết Thông hiểu Vận dụng Vận dụng cao TN TL TN TL TN TL TN TL 1. Oxit: t/c hóa học, phân loại oxit; CaO, SO2 T/c hóa học của oxit bazơ . -Định nghĩa oxit TCHH của oxit axit, TCVL của H2 O2 Quan sát TN cụ thể, rút ra t/c hóa học của oxit, SO2 Viết PTHH Tính khối lượng các chất sau phản ứng Số câu hỏi 2 1 1 1 5 Số điểm TL% 1,0 10% 1,0 10% 0,5 5% 0,5 2,0 5,0 50% 25% 2. Axit: Tính chất hóa học, phân loại, H2SO4 - T/c hóa học của axit, H2SO4 (đặc) Quan sát TN cụ thể, rút ra t/c hóa học của axit, Viết được các PTHH thể hiện t/c hóa học của axit Nhận biết H2SO4 và muối sunfat Số câu hỏi 2 1 1 1 5 Số điểm TL% 1,0 10% 0,5 5% 2,0 20% 1,5 15% 5,0 50% Tổng số câu hỏi 4 1 2 1 1 1 10 Tổng số điểm 2,0 1,0 1,0 2,0 2,0 2,0 10,0 TL % 20% 10% 10% 20% 20% 20% 100% PHỊNG GD- ĐT NINH SƠN KIỂM TRA MỘT TIẾT (BÀI SỐ 1) TRƯỜNG THCS TRẦN QUỐC TOẢN Năm học: 2015 - 2016 Mơn: Hĩa học - LỚP 9 Thời gian làm bài 45 phút (Khơng kể thời gian phát, chép đề) Họ và tên HS: Lớp: .. Điểm: Lời phê: ĐỀ: (Đề KT cĩ 2 trang) I. Trắc nghiệm khách quan: (3 điểm) Hãy khoanh trịn 1 trong các chữ cái A hoặc B, C, D mà em cho là đúng. Câu 1: Hãy chọn định nghĩa chính xác nhất về oxit trong số các phương án sau: A. Oxit là hợp chất gồm hai nguyên tố, trong đĩ cĩ một nguyên tố là oxi. Oxit là hợp chất gồm hai nguyên tố, trong đĩ cĩ nguyên tố kim loại và oxi. Oxit là hợp chất gồm ba nguyên tố, trong đĩ cĩ một nguyên tố là oxi. Oxit là hợp chất của phi kim và oxi. Câu 2: Oxít tác dụng được với dung dich HCl là: A. CuO; B. SO3; C. CO; D. SO2; Câu 3: Chất làm quì tím ẩm chuyển sang màu đỏ là: A. MgO; B. K2O; C. SO2; D. CaO ; Câu 4: A. Axit H2SO4 đặc chỉ phản ứng với kim loại đứng trước hiđro trong dãy hoạt động hĩa học của kim loại. B. Axit H2SO4 đặc phản ứng với cả kim loại đứng sau hiđro trong dãy hoạt động hĩa học của kim loại và khơng giải phĩng khí hiđro C. Axit H2SO4 đặc phản ứng với tất cả các kim loại. D. Axit H2SO4 (đặc) phản ứng với kim loại khơng giải phĩng khí hiđro Câu 5: Chất tác dụng với dung dịch HCl tạo thành chất khí nhẹ hơn khơng khí là: A. Na2SO3; B. CaCO3; C. MgCO3; D. Mg Câu 6: Cho mẫu quì tím vào dd NaOH. Thêm từ từ dd HCl vào cho đến dư, ta thấy mẫu giấy quì: A. Màu đỏ; B. Màu đỏ chuyển dần sang xanh; C. Màu xanh; D. Màu xanh chuyển dần sang đỏ. * Trả lời bài làm trắc nghiệm vào bảng sau: (3 điểm) Câu 1 2 3 4 5 6 Đáp án Biểu điểm II. Tự luận: (7 điểm) Câu 7: (1,0 điểm). Cĩ những chất khí sau: O2, CO2, H2, N2. Hãy cho biết chất nào cĩ tính chất sau: Tác dụng với nước tạo thành dung dịch axit Cháy được trong khơng khí. Nặng hơn khơng khí. Đổi màu giấy quì tím ẩm thành đỏ. Câu 8: (2.0 điểm). Hồn thành các PTHH sau: a. HCl + Fe ---------> b. HCl + CuO ---------> c. HNO3 + Mg(OH)2 ---------> d. H2SO4 (đặc) + Cu ---------> Câu 9: (1,5 điểm). Cĩ 3 lọ khơng nhãn đựng riêng biệt các dd sau: Na2SO4, HCl, NaCl. Bằng phương pháp hĩa học, hãy nhận biết các chất trên. Viết PTHH xảy ra. Câu 10: (2,5 điểm). Dẫn 1,12 lít khí SO2 (đktc) qua 700 ml dd Ca(OH)2 nồng độ 0,1M, sản phẩm là muối canxi sunfit. a. Viết PTHH. b. Tính khối lượng các chất sau phản ứng. (Biết: Ca = 40, S = 32, O = 16, H = 1) Bài làm phần tự luận PHỊNG GD- ĐT NINH SƠN KIỂM TRA MỘT TIẾT (BÀI SỐ 1) TRƯỜNG THCS TRẦN QUỐC TOẢN Năm học: 2015 - 2016 Mơn: Hĩa học - LỚP 9 Thời gian làm bài 45 phút (Khơng kể thời gian phát, chép đề) ĐÁP ÁN HƯỚNG DẪN CHẤM VÀ BIỂU ĐIỂM I. Trắc nghiệm: 3 điểm. (Mỗi Chọn câu đúng nhất được 0,5 điểm, chọn câu gần đúng được 0,25điểm) Câu 1 2 3 4 5 6 Đáp án A B A C B D D D Biểu điểm 0,5 0,25 0,5 0,5 0,5 0,25 0,5 0,5 II. Tự luận: 7 điểm CÂU ĐÁPÁN BIỂU ĐIỂM Câu 7 a. CO2 b. H2 c. O2 d. CO2 (1,0đ) 0,25 0,25 0,25 0,25 Câu 8 (2,0đ) a. 2HCl + Fe FeCl2 + H2 0,5 b. 2HCl + CuO CuCl2 + H2O 0,5 c. 2HNO3 + Mg(OH)2 Mg(NO3)2 + 2H2O 0,5 d. 2H2SO4 (đặc) + Cu CuSO4 + SO2 + 2H2O 0,5 Câu 9 (1,5đ) - Dùng quì tím nhận ra HCl 0,5 - Dùng dd BaCl2 nhận ra Na2SO4, chất cịn lại là NaCl. 0,5 Na2SO4 + BaCl2 BaSO4 + 2NaCl 0,5 Câu 10 (2,5đ) a. SO2 + Ca(OH)2 CaSO3 + H2O 0,5 b. Số mol SO2: 1,12 : 22,4 = 0,05 mol 0,25 Số mol Ca(OH)2: 0,1 x 0,7 = 0,07 mol 0,25 Theo PTHH: vì nSO2 < nCa(OH)2 Ca(OH)2 dư. 0,25 nSO2 = nCa(OH)2 = nCaSO3 = 0,05 mol. 0,5 Số mol Ca(OH)2 dư: 0,07 - 0,05 = 0,02 mol 0,25 Khối lượng các chất sau phản ứng: mCaSO3 = 0,05 x 120 = 6 (g) 0,25 mCa(OH)2 (dư) = 0,02 x 74 = 1,48 (g) 0,25 Chú ý: - Cân bằng PTHH sai: trừ ½ số điểm; - HS làm cách khác đúng: tính điểm
Tài liệu đính kèm:
 KT HÓA 9 LAN 1.doc
KT HÓA 9 LAN 1.doc





