Kiểm tra 1 tiết Môn: Hóa học 9 Trường THCS Nguyễn Bỉnh Khiêm
Bạn đang xem tài liệu "Kiểm tra 1 tiết Môn: Hóa học 9 Trường THCS Nguyễn Bỉnh Khiêm", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
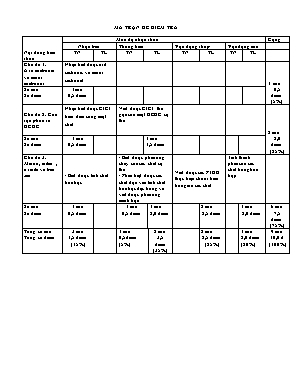
MA TRẬN ĐỀ KIỂM TRA Nội dung kiến thức Mức độ nhận thức Cộng Nhận biết Thông hiểu Vận dụng thấp Vận dụng cao TN TL TN TL TN TL TN TL Chủ đề 1: Axit cacbonic và muối cacbonat Nhận biết được axit cacbonic và muối cacbonat 1 câu 0,5 điểm (5%) Số câu Số điểm 1câu 0,5 điểm Chủ đề 2: Cấu tạo phân tử HCHC Nhận biết được CTCT biểu diễn cùng một chất Viết được CTCT thu gọn của một HCHC cụ thể 2 câu 2,0 điểm (25%) Số câu Số điểm 1 câu 0,5 điểm 1 câu 1,5 điểm Chủ đề 3: Mêtan, etilen , axetile và ben zen - Biết được tính chất hóa học - Biết được phản ứng cháy của các chất cụ thể - Phân biệt được các chất dựa vào tính chất hóa học đặc trưng và viết được phản ứng minh họa Viết được các PTHH thực hiện chuỗi biến hóa giữa các chất Tính thành phần của các chất trong hỗn hợp Số câu Số điểm 1 câu 0,5 điểm 1 câu 0,5 điểm 1 câu 2,0 điểm 2 câu 2,5 điểm 1 câu 2,0 điểm 6 câu 7,5 điểm (75%) Tổng số câu Tổng số điểm 3 câu 1,5 điểm (15%) 1 câu 0,5điểm (5%) 2 câu 3,5 điểm (35%) 2 câu 2,5 điểm (25%) 1 câu 2,0 điểm (20%) 9 câu 10,0 đ (100%) Trường THCS Nguyễn Bỉnh Khiêm Lớp: 9/ Họ và tên: .. Mã đề: Kiểm tra 1 tiết Môn: Hóa học 9 Ngày kiểm tra /03/2016 Điểm Lời phê Đề 1: I/ Trắc nghiệm: (2,0 điểm) Khoanh tròn chữ cái trước câu trả lời đúng Câu 1. (0,5 điểm) Để phân biệt 2 dung dịch: Na2SO4 và Na2CO3 người ta dùng thuốc thử: A. dd NaCl B. dd HCl C. CaCO3 D. dd KCl Câu 2. (0,5 điểm) Dãy những công thức cấu tạo nào sau đây biểu diễn cùng một chất: 1. CH2 – CH2 2. CH2 – CH2 3. CH3– CH2 – CH2 – CH3 4. CH3 – CH2 – CH2 | | | | | CH3 CH3 CH2 – CH2 CH3 A. 1 ; 2 và 4 B. 1 ; 3 và 4 C.2 ; 3 và 4 D. 1; 2 và 3 Câu 3 (0,5 điểm) Hợp chất hữu cơ có số nguyên tử hiđro bằng hai lần số nguyên tử cacbon và làm mất màu dung dịch brom. Hợp chất đó là A. metan. B. etilen. C. axetilen. D. benzen. Câu 4 (0,5 điểm) Chất hữu cơ X khi cháy theo phương trình phản ứng sau: X + 2O2 CO2 + 2H2O thì X có công thức phân tử là A. CH4. B. C2H4 . C. C2H2 . D. C6H6 . II/ Tự luận: ( 8,0 điểm) Câu 1. ( 2,0 điểm)Bằng phương pháp hóa học, làm thế nào phân biệt được các khí : cacbonic, metan, etilen ? Viết các phương trình hoá học của phản ứng (nếu có) để giải thích. Câu 2 ( 2,0 điểm) Thực hiện dãy chuyển hoá sau bằng các phương trình hoá học : CaC2 C2H2 C2H4 C2H4Br2 (4) P.E Câu 3 (1,5 điểm) Viết tất cả các công thức cấu tạo dạng thu gọn cho công thức phân tử C5H12 Câu 4 (2,5 điểm) Cho 2,8 lít hỗn hợp metan và etilen (đktc) lội qua dung dịch brom dư, người ta thu được 4,7 gam đibrometan. 1. Viết phương trình hoá học của phản ứng xảy ra. 2. Tính thành phần phần trăm của hỗn hợp theo thể tích. (Br = 80 ; C = 12 ; H = 1) Bài làm: Trường THCS Nguyễn Bỉnh Khiêm Lớp: 9/ Họ và tên: .. Mã đề: Kiểm tra 1 tiết Môn: Hóa học 9 Ngày kiểm tra /03/2016 Điểm Lời phê Đề 2: I/ Trắc nghiệm: (2,0 điểm) Khoanh tròn chữ cái trước câu trả lời đúng Câu 1. (0,5 điểm) Để phân biệt 2 dung dịch: H2SO4 và HCl người ta dùng thuốc thử: A. dd NaOH B. dd NaCl C. dd BaCl2 D. CaCO3 Câu 2. (0,5 điểm) Dãy những công thức cấu tạo nào sau đây biểu diễn cùng một chất: 1. CH2 – CH2 2. CH2 – CH2 3. CH3– CH2 – CH2 – CH3 4. CH3 – CH2 – CH2 | | | | | CH3 CH3 CH2 – CH2 CH3 A. 2 ; 3 và 4 B. 1 ; 2 và 4 C.1 ; 3 và 4 D. 1; 2 và 3 Câu 3 (0,5 điểm) Hợp chất hữu cơ có số nguyên tử hiđro bằng số nguyên tử cacbon và làm mất màu dung dịch brom. Hợp chất đó là A. axetilen. B. metan. C. benzen. D. etilen. Câu 4 (0,5 điểm) Chất hữu cơ X khi cháy theo phương trình phản ứng sau: X + 3O2 2CO2 + 2H2O thì X có công thức phân tử là A. C2H2 . B. C6H6 . C. CH4. D. C2H4 . II/ Tự luận: (8,0 điểm) Câu 1. (2,0 điểm) Bằng phương pháp hóa học, làm thế nào phân biệt được các khí: cacbonic, metan, axetilen? Viết các phương trình hoá học của phản ứng (nếu có) để giải thích. Câu 2 (2,0 điểm) Thực hiện dãy chuyển hoá sau bằng các phương trình hoá học: CH4 C2H2 C2H4 (3) (4) C2H6 P.E Câu 3 (1,5 điểm) Viết tất cả công thức cấu tạo thu gọn( dạng mạch thẳng và mạch nhánh) cho công thức phân tử C4H8 Câu 4 (2,5 điểm) Dẫn toàn bộ 2,24 lít hỗn hợp khí ở điều kiện tiêu chuẩn gồm CH4 và C2H4 đi qua bình dung dịch brôm dư , thấy có 8 gam khối lượng brôm tham gia phản ứng. 1. Viết phương trình hoá học của phản ứng xảy ra. 2. Tính thành phần phần trăm của hỗn hợp theo thể tích (Br = 80 ; C = 12 ; H = 1) Bài làm: ĐÁP ÁN VÀ BIỂU ĐIỂM ĐỀ SỐ 1 Phần I: Trắc nghiệm ( 2,0 điểm) BIỂU ĐIỂM Câu 1 Câu 2 Câu 3 Câu 4 B B B A 0,5 x 4 = 2,0 điểm PHẦN II: Tự luận ( 8,0điểm) Câu 1 - Dẫn ban khí lần lượt qua ba cốc nước vôi trong + Khí làm đục nước vôi trong là CO2 + PT: Ca(OH)2 + CO2 CaCO3 + H2O - Dẫn hai khí còn lại qua dung dịch brom + Khí làm mất màu dung dịch brom là etilen, còn lại là metan + PT: CH2 = CH2 + Br- Br CH2Br - CH2Br 2,0 điểm Câu 2 (1) CaC2 + 2H2O C2H2 + Ca(OH)2 (2) C2H2 + H2 C2H4 (3) C2H4 + Br2 C2H4Br2 (4) n CH2 = CH2 (-CH2-CH2-)n (P.E) 0,5 đ 0,5 đ 0,5 đ 0,5 đ Câu 3 + CH3 - CH2 - CH2 - CH2 - CH3 ; CH3 – CH - CH2 - CH3; CH3 CH3 CH3 – C –CH3 CH3 0,5 x 3 = 1,5 điểm Câu 4 1/ PTHH C2H4 + Br2 C2H4Br2 2/ Số mol của C2H4Br2: n = = 0,025 mol Theo PTHH: n= n= 0,025 mol Thể tích của C2H4 ( đktc): V= 0,025 x 22,4 = 0,56 lit Phần trăm của các khí theo thể tích: % V= x 100% = 20% % V= 100% - 20% = 80% ( Học sinh giải cách khác đúng vẫn đạt điểm tối đa) 0,5 đ 0,25 đ 0,25 đ 0,5 đ 0,5 đ 0,5 đ Tổng 10,0 điểm ĐÁP ÁN VÀ BIỂU ĐIỂM ĐỀ SỐ 2 Phần I: Trắc nghiệm ( 2,0 điểm) BIỂU ĐIỂM Câu 1 Câu 2 Câu 3 Câu 4 C C A D 0,5 x 4 = 2,0 điểm PHẦN II: Tự luận ( 8,0điểm) Câu 1 - Dẫn ban khí lần lượt qua ba cốc nước vôi trong + Khí làm đục nước vôi trong là CO2 + PT: Ca(OH)2 + CO2 CaCO3 + H2O - Dẫn hai khí còn lại qua dung dịch brom + Khí làm mất màu dung dịch brom là axetilen, còn lại là metan + PT: CH CH + Br- Br CHBr2 – CHBr2 2,0 điểm Câu 2 (1) 2CH4 C2H2 + 3H2 (2) C2H2 + H2 C2H4 (3) C2H2 + 2H2 C2H6 (4) n CH2 = CH2 (-CH2-CH2-)n (P.E) 0,5 đ 0,5 đ 0,5 đ 0,5 đ Câu 3 CH3 - CH = CH - CH3 ; CH3 – C= CH2; CH3 – CH2 – CH = CH2 CH3 0,5 x 3 = 1,5 điểm Câu 4 1/ PTHH C2H4 + Br2 C2H4Br2 2/ Số mol của Br2: n = = 0,05 mol Theo PTHH: n= n= 0,05 mol Thể tích của C2H4 ( đktc): V= 0,05 x 22,4 = 1,12 lit Phần trăm của các khí theo thể tích: % V= x 100% = 50% % V= 100% - 50% = 50% ( Học sinh giải cách khác đúng vẫn đạt điểm tối đa) 0,5 đ 0,25 đ 0,25 đ 0,5 đ 0,5 đ 0,5 đ Tổng 10,0 điểm
Tài liệu đính kèm:
 KIEM_TRA_HOA_9_LAN_3.doc
KIEM_TRA_HOA_9_LAN_3.doc





