Khung ma trận, bản đặc tả và đề kiểm tra định kỳ môn Hóa học Lớp 8 - Trường THCS Nam Hồng - Năm học 2022-2023 (Có đáp án và thang điểm)
Bạn đang xem tài liệu "Khung ma trận, bản đặc tả và đề kiểm tra định kỳ môn Hóa học Lớp 8 - Trường THCS Nam Hồng - Năm học 2022-2023 (Có đáp án và thang điểm)", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
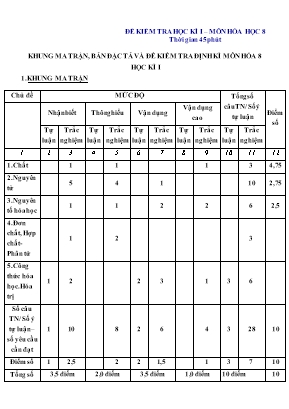
ĐỀ KIỂM TRA HỌC KÌ I – MÔN HÓA HỌC 8 Thời gian 45 phút KHUNG MA TRẬN, BẢN ĐẶC TẢ VÀ ĐỀ KIỂM TRA ĐỊNH KÌ MÔN HÓA 8 HỌC KÌ I KHUNG MA TRẬN Chủ đề MỨC ĐỘ Tổng số câuTN/ Số ý tự luận Điểm số Nhận biết Thông hiểu Vận dụng Vận dụng cao Tự luận Trắc nghiệm Tự luận Trắc nghiệm Tự luận Trắc nghiệm Tự luận Trắc nghiệm Tự luận Trắc nghiệm 1 2 3 4 5 6 7 8 9 10 11 12 1. Chất 1 1 1 3 4,75 Nguyên tử 5 4 1 10 2,75 Nguyên tố hóa học 1 1 2 2 6 2,5 Đơn chất, Hợp chất- Phân tử 1 2 3 Công thức hóa học. Hóa trị 1 2 2 3 1 3 6 Số câu TN/ Số ý tự luận – số yêu cầu cần đạt 1 10 8 2 6 4 3 28 10 Điểm số 1 2,5 2 2 1,5 1 3 7 10 Tổng số điểm 3,5 điểm 2,0 điểm 3,5 điểm 1,0 điểm 10 điểm 10 điểm BẢN ĐẶC TẢ Nội dung Mức độ Yêu cầu cần đạt Số ý TL/số câu hỏi TN Câu hỏi TL (Số ý) TN (Số câu) TL (Số ý) TN (Số câu) Chất Nhận biết - Trình bày được khái niệm chất, chất nguyên chất, hỗn hợp và một số tính chất của chất. 1 1 Thông hiểu Phân biệt được chất nguyên chất và hỗn hợp dựa vào tính chất vật lý. Phân biệt được chất và vật thể, chất tinh khiết và hỗn hợp. 1 2 Vận dụng So sánh được tính chất vật lý của một số chất gần gũi trong cuộc sống. Vận dụng cao - Tách riêng được chất ra khỏi hỗn hợp (dựa vào tính chất vật lý). 1 3 Nguyên tử Nhận biết - Biết được trong nguyên tử số p bằng số e và điện tích của 1p bằng điện tích của 1e về giá trị tuyệt đối nhưng trái dấu, nên nguyên tử trung hòa về điện. - Biết được khối lượng nguyên tử và nguyên tử khối. 5 4,5,6,20,21 Thông hiểu - Xác định được số đơn vị điện tích hạt nhân, số p, số e trong mỗi lớp dựa vào sơ đồ cấu tạo nguyên tử . 4 7,8,18,19 Vận dụng Tìm được số đơn vị điện tích hạt nhân, số p, số e, số n của dạng bài tập đơn giản. 1 22 Vận dụng cao Bài tập tính toán liên quan đến số đơn vị điện tích hạt nhân, số e, số p, số n và khối lượng của nguyên tử. 3. Nguyên tố hóa học Nhận biết Biết được nguyên tử có cùng số p trong hạt nhân thuộc cùng một nguyên tố hóa học. Biết được khái niệm nguyên tử khối và đơn vị. 1 17 Thông Hiểu - Đọc được tên nguyên tố khi biết được ký hiệu và ngược lại. 1 9 Vận dụng - Tìm được nguyên tử khối của một số nguyên tố cụ thể. - Bài tập tính toán đơn giản 2 23,11 Vận dụng cao - Bài tập tính toán liên quan đến nguyên tử khối. - So sánh được sự nặng/nhẹ của các nguyên tử với nhau. 2 10,12 4.Đơn chất và Hợp chất- Phân tử Nhận biết Biết được chất nào là đơn chất, hợp chất , phân tử và phân tử khối. 1 25 Thông Hiểu Phân biệt được đơn chất hay hợp chất theo thành phần nguyên tố tạo nên nó. 2 26,27 Vận dụng Tính phân tử khối của một số phân tử và hợp chất đơn giản. Vận dụng cao Bài tập tính toán liên quan đến phân tử khối. 5.Công thức hóa học. Hóa trị Nhận biết Biết cách việt công thức hóa học của đơn chất và hợp chất, ý nghĩa của công thức hóa học. - Biết được quy ước: hóa trị của H là I, hóa trị của O là II; hóa trị của một nguyên tố trong hợp chất cụ thể xác định theo hóa trị của H và O. - Phát biểu được quy tắc hóa trị: Trong hợp chất hai nguyên tố AxBy thì: a.x = b.y 1 2 Câu 2 ý a. 14,24 Thông Hiểu - Viết được công thức hóa học của chất cụ thể khi biết được tên nguyên tố và và số nguyên tử của mỗi nguyên tố tạo nên một phân tử và ngược lại. - Xác định được hóa trị của một số chất cơ bản. Vận dụng Tính được hóa trị của nguyên tố hoặc nhóm nguyên tử theo công thức hóa học. 2 3 Câu 1, câu 2 ý b 15,13,16 Vận dụng cao Lập được công thức hóa học của hợp chất khi biết hóa trị của nguyên tố, nhốm nguyên tử. Bài toán liên quan đến hóa trị. 1 1 Câu 3 28 ĐỀ KIỂM TRA PHÒNG GD-ĐT HUYỆN ĐÔNG ANH TRƯỜNG THCS NAM HỒNG ĐỀ KIỂM TRA GIỮA KÌ I Năm học: 2022 –2023 Môn: Hóa Học lớp 8 – Tiết : 16 Thời gian: 45 phút (Không kể thời gian giao đề) ĐỀ 1 Đề gồm: Trắc nghiệm: 28 câu (7 điểm), Tự luận: 3 câu (3 điểm) I. Trắc nghiệm: Khoanh tròn chữ cái đứng trước đáp án đúng Câu 1. Nước sông hồ thuộc loại: A. Đơn chất B. Hợp chất C. Chất tinh khiết D. Hỗn hợp Câu 2. Trong số các chất sau, chất nào là chất tinh khiết ? A. Nước tự nhiên B. Nước biển C. Nước cất D. Nước mưa Câu 3. Để tách rượu ra khỏi hỗn hợp rượu lẫn nước, dùng cách nào sau đây? Lọc B. Dùng phễu chiết C. Chưng cất phân đoạn D. Đốt Câu 4. Trong một nguyên tử luôn luôn có: A. Số p bằng số e B. Số p lớn hơn số e C. Số p nhỏ hơn số e D. A, B,C đều Sai Câu 5. Những nguyên tử cùng loại có cùng số hạt nào sau đây? Electron. B. Proton, C. Proton, nơtron, electron. D. Proton, nơtron. Câu 6. Vỏ nguyên tử được tạo thành từ hạt : A. n B. e C. p D. Cả A,B,C. Câu 7. Một nguyên tử được tạo thành từ 17 proton vậy số electron tạo nên nguyên tử là : 17 B. 18 C . 19 D. 20 Câu 8. Vì sao nói khối lượng của hạt nhân cũng là khối lượng của nguyên tử? A. Vì khối lượng hạt nhân bằng khối lượng nguyên tử B. Vì điện tích hạt nhân bằng điện tích ở vỏ C. Vì khối lượng electron không đáng kể D. Vì khối lượng Nơtron không đáng kể Câu 9. Nguyên tử khối là: Khối lượng của một nguyên tử tính bằng đơn vị kilogam Khối lượng của một nguyên tử tính bằng đơn vị gam Khối lượng của một nguyên tử tính bằng đơn vị cacbon Khối lượng của một nguyên tử tính bằng đơn vị lít Câu 10. Nguyên tử X nặng 5,312.10-23g, đó là nguyên tử của nguyên tố hóa học nào sau đây? O : 16 đvC B. Fe: 56 đvC C. S: 32 đvC D. P: 31 đvC Câu 11. Phân tử khối của caxicacbonat (CaCO3) là ..........đvC A. 68 B. 96 C. 97 D. 100 Câu 12. Biết nguyên tử C có khối lượng bằng 1.9926.10-23g, khối lượng của nguyên tử Al là: A. 0,885546.10-23g B. 4,482675.10-23g C. 3,9846.10-23g D. 0.166025.10-23g Câu 13. Công thức phân tử của một chất gồm 2 nguyên tử X, 1 Nguyên tử X nặng hơn phân tử hidro 7 lần. X là nguyên tố nào sau đây: A. C B. Na. C. N D. Ni Câu 14. Trong công thức hóa học NH3 hóa trị của N là : A. IV B. III C. II D. I Câu 15. Phân tử khối của CH4, Mg(OH)2, KCl lần lượt là: A. 16 đvC, 74,5 đvC, 58 đvC B. 74,5 đvC, 58 đvC, 16 đvC C. 17 đvC, 58 đvC, 74,5 đvC D. 16 đvC, 58 đvC, 74,5 đvC Câu 16. Biết kẽm có hóa trị II, trong công thức Zn3(PO4)2 nhóm PO4 có hóa trị là: A. III B. I C. II D. IV Câu 17. Nguyên tố hóa học là tập hợp những nguyên tử cùng loại có cùng : A. số p trong hạt nhân. B. số n trong hạt nhân. C. tổng số p và n trong hạt nhân. D. tổng số e và p trong hạt nhân. Câu 18. Các hạt cấu tạo nên hạt nhân của hầu hết nguyên tử là: A. electron, proton và nơtron. C. proton và nơtron. B. electron và nơtron. D. electron và proton. Câu 19. Trong nguyên tử, hạt mang điện là: A. Electron. C. Proton và nơtron. B. Electron và nơtron. D. Proton và electron. Câu 20. Các hạt cấu tạo nên hầu hết các nguyên tử là: A. electron, proton và nơtron. C. proton và nơtron. B. electron và nơtron. D. electron và proton. Câu 21. Trong nguyên tử, loại hạt nào có khối lượng không đáng kể so với các hạt còn lại? A. Proton. B. Nơtron. C. Electron và nơtron. D. Electron. Câu 22. Nguyên tử Ca so với nguyên tử O nặng hơn hay nhẹ hơn? A. Nặng hơn 0,4 lần. C. Nhẹ hơn 0,4 lần. B. Nhẹ hơn 2,5 lần. D. Nặng hơn 2,5 lần. Câu 23. Sự so sánh phân tử khí oxi (O2) và phân tử muối ăn (NaCl) nào dưới đây là đúng? A. NaCl nặng hơn O2 bằng 0,55 lần. C. O2 nhẹ hơn NaCl bằng 0,55 lần. B. O2 nặng hơn NaCl bằng 0,55 lần. D. NaCl nhẹ hơn O2 bằng 1,83 lần. Câu 24. Cách biểu diễn 4H2 có nghĩa là A. 4 nguyên tử hiđro. C. 4 phân tử hiđro B. 8 nguyên tử hiđro. D. 8 phân tử hiđro. Câu 25. Dãy chất nào sau đây đều là kim loại? A. Nhôm, đồng, lưu huỳnh, bạc. C. Oxi, nitơ, cacbon, canxi. B. Vàng, magie, nhôm, clo. D. Sắt, chì, kẽm, thiếc. Câu 26. Dãy nguyên tố phi kim là: A. Cl, O, N, Na, Ca. C. S, O, Cl, N, C. B. S, O, Cl, N, Na. D. C, Cu, O, N, Cl. Câu 27. Trong số các chất sau: Cl2, ZnCl2, Al2O3, Ca, NaNO3, KOH số đơn chất và hợp chất lần lượt là: A. 3 đơn chất và 3 hợp chất. C. 2 đơn chất và 4 hợp chất. B. 5 đơn chất và 1 hợp chất. D. 1 đơn chất và 5 hợp chất. Câu 28. Một oxit có công thức là Fe2Ox có phân tử khối là 160. Hóa trị của Fe là: A. I B. II C. III D. IV II. Tự luận Câu 1 (1 điểm): Hãy dùng chữ số và kí hiệu hóa học diễn đạt các ý sau: a, Bốn nguyên tử lưu huỳnh b, Sáu nguyên tử cac bon Câu 2 ( 1 điểm): a, Phát biểu quy tắc hóa trị. b, Cho biết hóa trị của Na và C theo quy ước trong công thức hóa học sau: Na 2O và CO2. Câu 3 (1 điểm): Lập công thức hóa học của các hợp chất sau. a, Ba(II) và O b, Fe(III) và (OH)(I) (Cho nguyên tử khối của các nguyên tố H = 1, O = 16, C = 12, N = 14, Na =23, Mg = 24, Al = 27, S = 32, Cl = 35,5, Cu =64, Fe = 56, Ba =137, Ag =108). ----------Hết---------- PHÒNG GD-ĐT HUYỆN ĐÔNG ANH TRƯỜNG THCS NAM HỒNG ĐỀ KIỂM TRA GIỮA KÌ I Năm học: 2022 –2023 Môn: Hóa Học lớp 8 Thời gian: 45 phút (Không kể thời gian giao đề) ĐỀ 2 Đề gồm: Trắc nghiệm: 28 câu (7 điểm), Tự luận: 3 câu (3 điểm) I. Trắc nghiệm: Khoanh tròn chữ cái đứng trước đáp án đúng Câu 1. Phân tử khối của caxicacbonat (CaCO3) là ..........đvC A. 68 B. 96 C. 97 D. 100 Câu 2. Biết nguyên tử C có khối lượng bằng 1.9926.10-23g, khối lượng của nguyên tử Al là: A. 0,885546.10-23g B. 4,482675.10-23g C. 3,9846.10-23g D. 0.166025.10-23g Câu 3. Những nguyên tử cùng loại có cùng số hạt nào sau đây? Electron. B. Proton, C. Proton, nơtron, electron. D. Proton, nơtron. Câu 4. Biết kẽm có hóa trị II, trong công thức Zn3(PO4)2 nhóm PO4 có hóa trị là: A. III B. I C. II D. IV Câu 5. Vì sao nói khối lượng của hạt nhân cũng là khối lượng của nguyên tử? A. Vì khối lượng hạt nhân bằng khối lượng nguyên tử B. Vì điện tích hạt nhân bằng điện tích ở vỏ C. Vì khối lượng electron không đáng kể D. Vì khối lượng Nơtron không đáng kể Câu 6. Để tách rượu ra khỏi hỗn hợp rượu lẫn nước, dùng cách nào sau đây? Lọc B. Dùng phễu chiết C. Chưng cất phân đoạn D. Đốt Câu 7. Phân tử khối của CH4, Mg(OH)2, KCl lần lượt là: A. 16 đvC, 74,5 đvC, 58 đvC B. 74,5 đvC, 58 đvC, 16 đvC C. 17 đvC, 58 đvC, 74,5 đvC D. 16 đvC, 58 đvC, 74,5 đvC Câu 8. Trong số các chất sau, chất nào là chất tinh khiết ? A. Nước tự nhiên B. Nước biển C. Nước cất D. Nước mưa Câu 9. Nguyên tử X nặng 5,312.10-23g, đó là nguyên tử của nguyên tố hóa học nào sau đây? O : 16 đvC B. Fe: 56 đvC C. S: 32 đvC D. P: 31 đvC Câu 10. Nước sông hồ thuộc loại: A. Đơn chất B. Hợp chất C. Chất tinh khiết D. Hỗn hợp Câu 11. Trong công thức hóa học NH3 hóa trị của N là : A. IV B. III C. II D. I Câu 12. Nguyên tử khối là: Khối lượng của một nguyên tử tính bằng đơn vị kilogam Khối lượng của một nguyên tử tính bằng đơn vị gam Khối lượng của một nguyên tử tính bằng đơn vị cacbon Khối lượng của một nguyên tử tính bằng đơn vị lít Câu 13. Một nguyên tử được tạo thành từ 17 proton vậy số electron tạo nên nguyên tử là : 17 B. 18 C . 19 D. 20 Câu 14. Công thức phân tử của một chất gồm 2 nguyên tử X, 1 Nguyên tử X nặng hơn phân tử hidro 7 lần. X là nguyên tố nào sau đây: A. C B. Na. C. N D. Ni Câu 15. Trong một nguyên tử luôn luôn có: A. Số p bằng số e B. Số p lớn hơn số e C. Số p nhỏ hơn số e D. A, B,C đều Sai Câu 16. Vỏ nguyên tử được tạo thành từ hạt : A. n B. e C. p D. Cả A,B,C. Câu 17. Các hạt cấu tạo nên hạt nhân của hầu hết nguyên tử là: A. electron, proton và nơtron. C. proton và nơtron. B. electron và nơtron. D. electron và proton. Câu 18. Các hạt cấu tạo nên hầu hết các nguyên tử là: A. electron, proton và nơtron. C. proton và nơtron. B. electron và nơtron. D. electron và proton. Câu 19. Trong nguyên tử, hạt mang điện là: A. Electron. C. Proton và nơtron. B. Electron và nơtron. D. Proton và electron. Câu 20. Nguyên tố hóa học là tập hợp những nguyên tử cùng loại có cùng : A. số p trong hạt nhân. B. số n trong hạt nhân. C. tổng số p và n trong hạt nhân. D. tổng số e và p trong hạt nhân. Câu 21. Trong số các chất sau: Cl2, ZnCl2, Al2O3, Ca, NaNO3, KOH số đơn chất và hợp chất lần lượt là: A. 3 đơn chất và 3 hợp chất. C. 2 đơn chất và 4 hợp chất. B. 5 đơn chất và 1 hợp chất. D. 1 đơn chất và 5 hợp chất. Câu 22. Một oxit có công thức là Fe2Ox có phân tử khối là 160. Hóa trị của Fe là: A. I B. II C. III D. IV Câu 23. Trong nguyên tử, loại hạt nào có khối lượng không đáng kể so với các hạt còn lại? A. Proton. B. Nơtron. C. Electron và nơtron. D. Electron. Câu 24. Cách biểu diễn 4H2 có nghĩa là A. 4 nguyên tử hiđro. C. 4 phân tử hiđro B. 8 nguyên tử hiđro. D. 8 phân tử hiđro. Câu 25. Dãy nguyên tố phi kim là: A. Cl, O, N, Na, Ca. C. S, O, Cl, N, C. B. S, O, Cl, N, Na. D. C, Cu, O, N, Cl. Câu 26. Nguyên tử Ca so với nguyên tử O nặng hơn hay nhẹ hơn? A. Nặng hơn 0,4 lần. C. Nhẹ hơn 0,4 lần. B. Nhẹ hơn 2,5 lần. D. Nặng hơn 2,5 lần. Câu 27. Sự so sánh phân tử khí oxi (O2) và phân tử muối ăn (NaCl) nào dưới đây là đúng? A. NaCl nặng hơn O2 bằng 0,55 lần. B. O2 nhẹ hơn NaCl bằng 0,55 lần. C. O2 nặng hơn NaCl bằng 0,55 lần. D. NaCl nhẹ hơn O2 bằng 1,83 lần. Câu 28. Dãy chất nào sau đây đều là kim loại? A. Nhôm, đồng, lưu huỳnh, bạc. C. Oxi, nitơ, cacbon, canxi. B. Vàng, magie, nhôm, clo. D. Sắt, chì, kẽm, thiếc. II. Tự luận Câu 1 (1 điểm): Hãy dùng chữ số và kí hiệu hóa học diễn đạt các ý sau: a, Sáu nguyên tử lưu huỳnh b, Bốn nguyên tử cac bon Câu 2 (1 điểm): a, Phát biểu quy tắc hóa trị. b, Cho biết hóa trị của Ca và S theo quy ước trong công thức hóa học sau: Ca O và SO2. Câu 3 (1 điểm): Lập công thức hóa học của các hợp chất sau. a, Al(III) và O b, Mg (II) và SO4 (II) (Cho nguyên tử khối của các nguyên tố H = 1, O = 16, C = 12, N = 14, Na =23, Mg = 24, Al = 27, S = 32, Cl = 35,5, Cu =64, Fe = 56, Ba =137, Ag =108). ----------Hết---------- PHÒNG GD-ĐT HUYỆN ĐÔNG ANH TRƯỜNG THCS NAM HỒNG Đề số: 01 HƯỚNG DÂN CHẤM ĐỀ KIỂM TRA GIỮA KÌ I Năm học: 2022 – 2023 Môn: Hóa Học lớp 8 I. Trắc nghiệm: (7 điểm) mỗi ý đúng được 0,25 điểm Câu 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 Đáp án đúng C C C A B B A C C C D B C B D A Câu 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 Đáp án đúng A A D A D D C C D C C C II. Tự luận: (3 điểm) Câu Ý Nội dung Điểm 1 a b 4S 6C 0,5đ 0,5đ 2 a b Quy tắc hóa trị: Trong công thức hóa học, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia. - Hóa trị của Na là I - Hóa trị của C là IV 0,5đ 0,25đ 0,25đ 3 a b BaO Fe(OH)3 0,5đ 0,5đ (Học sinh làm theo cách khác, nếu đúng, lập luận chặt chẽ vẫn cho điểm tối đa) PHÒNG GD-ĐT HUYỆN ĐÔNG ANH TRƯỜNG THCS NAM HỒNG Đề số: 2 HƯỚNG DÂN CHẤM ĐỀ KIỂM TRA GIỮA KÌ I Năm học: 2022 – 2023 Môn: Hóa Học lớp 8 I. Trắc nghiệm: (7 điểm) mỗi ý đúng được 0,25 điểm Câu 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 Đáp án đúng D B B A C C D C C D B C A C A B Câu 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 Đáp án đúng C A D A C C D C C D B D II. Tự luận: (3 điểm) Câu Ý Nội dung Điểm 1 a b 6S 4C 0,5đ 0,5đ 2 a b Quy tắc hóa trị: Trong công thức hóa học, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia. - Hóa trị của Ca là II - Hóa trị của S là IV 0,5đ 0,25đ 0,25đ 4 a b Al2O3 MgSO4 0,5đ 0,5đ (Học sinh làm theo cách khác, nếu đúng, lập luận chặt chẽ vẫn cho điểm tối đa) 4 . HƯỚNG DẪN CHẤM ĐỀ 1 Trắc nghiệm 1.A 2.C 3.A 4.B 5.D 6.B 7.C 8.D 9.D 10.A 11.D 12.C 13.C 14.B 15.D 16.A 17.B 18.C 19.A 20.C 21.A 22.B 23.A 24.A 25.C 26.D 27.D 28.B 29.B 30.B 31.A 32.C Tự luận Câu 1: nNa2SO4 = 0,2 mol; nCuSO4= 0,1 mol; nBa(OH)2= 0,36 mol PTHH Na2SO4 + Ba(OH)2 -> 2NaOH + BaSO4 CuSO4 + Ba(OH)2 -> Cu(OH)2 + BaSO4 Cu(OH)2 -> CuO + H2O m = mCuO + mBaSO4 = 0,1.80+ 0,3.233 = 77,9 g 0,5 0,5 Câu 2: MA= 54, tính nSO2=nCO2=0,1 mol PTHH Na2CO3 + 2HCl -> 2NaCl + CO2 + H2O K2SO3 + 2HCl -> 2KCl + SO2 + H2O m dd HCl = 100 gam -> m dd sau pư = 0,1.106+0,1.158 + 100 – 0,2.2.27 = 115,6 (g) C%NaCl= 0,2.58,5: 115,6.100% = 10,12% C%KCl = 0,2.74,5: 115,6.100% = 12,89% 0,25 0,25 0,5 ĐỀ 2 Trắc nghiệm 1.A 2.C 3.A 4.B 5.D 6.B 7.C 8.D 9.D 10.A 11.D 12.C 13.C 14.B 15.D 16.A 17.B 18.C 19.A 20.C 21.A 22.B 23.A 24.D 25.C 26.D 27.A 28.B 29.B 30.B 31.A 32.C Tự luận Câu 1: nNa2SO4 = 0,15 mol; nCuSO4= 0,16 mol; nBa(OH)2= 0,33 mol PTHH Na2SO4 + Ba(OH)2 -> 2NaOH + BaSO4 CuSO4 + Ba(OH)2 -> Cu(OH)2 + BaSO4 Cu(OH)2 -> CuO + H2O m = mCuO + mBaSO4 = 0,16.80+ 0,31.233 = 85,03 g 0,5 0,5 Câu 2: MA= 54, tính nSO2=nCO2=0,1 mol PTHH Na2CO3 + 2HCl -> 2NaCl + CO2 + H2O K2SO3 + 2HCl -> 2KCl + SO2 + H2O m dd HCl = 200 gam -> m dd sau pư = 0,1.106+0,1.158 + 200 – 0,2.2.27 = 215,6 (g) C%NaCl= 0,2.58,5: 215,6.100% = 5,43% C%KCl = 0,2.74,5: 215,6.100% = 6,91% 0,25 0,25 0,5
Tài liệu đính kèm:
 khung_ma_tran_ban_dac_ta_va_de_kiem_tra_dinh_ky_mon_hoa_hoc.doc
khung_ma_tran_ban_dac_ta_va_de_kiem_tra_dinh_ky_mon_hoa_hoc.doc





