Đề kiểm tra học kì II năm học: 2015 - 2016 môn: Hóa học 8 thời gian: 45 phút (không kể thời gian giao đề)
Bạn đang xem tài liệu "Đề kiểm tra học kì II năm học: 2015 - 2016 môn: Hóa học 8 thời gian: 45 phút (không kể thời gian giao đề)", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
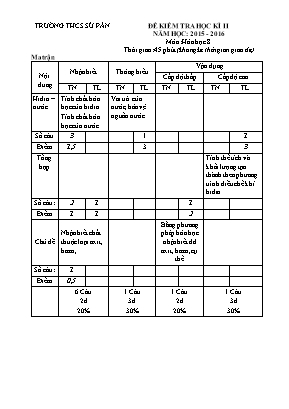
TRƯỜNG THCS SỬ PÁN ĐỀ KIỂM TRA HỌC KÌ II NĂM HỌC: 2015 - 2016 Môn: Hóa học 8 Thời gian: 45 phút (không kể thời gian giao đề) Ma trận Nội dung Nhận biết Thông hiểu Vận dụng Cấp độ thấp Cấp độ cao TN TL TN TL TN TL TN TL Hiđro – nước Tính chất hóa học của hiđro. Tính chất hóa học của nước Vai trò của nước, bảo vệ nguồn nước. Số câu 3 1 1 Điểm 1,5 3 3 Tổng hợp Tính thể tích và khối lượng tạo thành theo phương trình điều chế khí hiđro Số câu: 2 1 1 Điểm 1 1 2 Chủ đề Nhận biết chất thuộc loại axit, bazo, Bằng phương pháp hóa học nhận biết dd axit, bazo, cụ thể Số câu: 1 Điểm 0,5 6 Câu 2đ 20% 1 Câu 3đ 30% 1 Câu 2đ 20% 1 Câu 3đ 30% ĐỀ KIỂM TRA HỌC KÌ II Môn hóa học 8 ĐỀ 1. Chủ đề: Nhận biết các chất (2,5đ) Đọc thông tin sau và làm các bài tập Để nhận biết các chất bằng PPHH, người ta dựa vào sự khác nhau về tính chất của các chất. VD: dd axít làm quỳ tím chuyển thành màu đỏ, dd bazơ làm quỳ tím chuyển thành màu xanh. 1. Khoanh tròn vào chữ cái trước câu trả lời đúng a. Chất làm quỳ tím chuyển màu thành đỏ là A. NaOH B. HCl C. H2O D. KOH a. Chất làm quỳ tím chuyển màu thành xanh là A. NaOH B. HCl C. H2O D. H2SO4 2. Hãy nêu phương pháp nhận biết 3 dung dịch đựng trong 3 lọ mất nhãn sau: Ba(OH)2, HCl, H2O I/ Trắc nghiệm khách quan (1,5đ ) * Khoanh tròn vào đáp án đứng trước câu trả lời đúng Câu 1: Để thu khí hiđro trong phòng thí nghiệm bằng cách đẩy nước ngư ời ta dựa vào tính chất nào của Hiđro: A. Nhẹ hơn không khí B. Không tác dụng với nư ớc C. Không tác dụng với KK D. Nhẹ hơn KK và ít tan trong n ước Câu 2: Cho các chất sau chất nào không tác dụng được với nước: A. Al B. CaO C. K D.SO3 Câu 3: Loại chất làm quì tím chuyển màu xanh là: A. oxit B. axit C. bazơ D. muối II/ Tự luận (6đ ) Câu 4: (3đ) Nước có vai trò gì trong TN và đời sống con người? Để bảo vệ nguồn nước, theo em chúng ta cần phải làm gì? Câu 5: (3đ) Cho 3,25 gam Zn tác dụng với dung dịch HCl d ư. a. Viết phư ơng trình phản ứng hoá học xảy ra. b. Tính thể tích khí (đktc) thu đư ợc sau phản ứng. c. Tính khối lư ợng muối thu đ ược sau phản ứng. (Cho biết Zn = 65; H = 1; Cl = 35,5 ; O = 16) C/ Đáp án, thang điểm: Chủ đề: 2,5đ 1. Mỗi đáp án đúng đạt 0,25đ 1 a b Đáp án B A 2. Lấy ba mẩu giấy quỳ tím cho vào ba lọ, lọ nào làm quỳ tím chuyển thành màu đỏ lọ đó là HCl. Lọ nào làm quỳ tím chuyển thành màu xanh, lọ đó đựng Ba(OH)2 . Lọ còn lại là nước. I/ Trắc nghiệm khách quan: 1,5đ Mỗi câu đúng đạt 0,5đ Câu 1 2 3 Đáp án D A C II/ Tự luận: 6đ Câu Nội dung Điểm 4 HS nêu được vai trò của nước HS nêu được biện pháp bảo vệ nguồn nước 1,5 1,5 5 nZn = = 0,05 mol a. Ph ương trình phản ứng Zn + 2HCl ZnCl2 + H2 b. Tính thể tích khí (đktc) thu đ ược sau phản ứng. Theo PTHH số mol của Zn bằng số mol của H2 = 0,05 mol Thể tích khí H2 thu đ ược là: V = 22,4.0,05 = 1,12 lít c. Tính khối lư ợng muối thu đ ược sau phản ứng Theo PTHH thì số mol ZnCl2 bằng số mol Zn = 0, 05 mol Khối lư ợng của ZnCl2 thu đ ược là: n = 0,05.136 = 6,8 g 0,5 0,5 1 1 ĐỀ 2. Chủ đề: Nhận biết các chất (2,5đ) Đọc thông tin sau và làm các bài tập Để nhận biết các chất bằng PPHH, người ta dựa vào sự khác nhau về tính chất của các chất. VD: dd axít làm quỳ tím chuyển thành màu đỏ, dd bazơ làm quỳ tím chuyển thành màu xanh. 1. Khoanh tròn vào chữ cái trước câu trả lời đúng a. Chất làm quỳ tím chuyển màu thành đỏ là A. KOH B. Ca(OH)2 C. H2O D. H2SO4 a. Chất làm quỳ tím chuyển màu thành xanh là A. Al B. NaOH C. H2O D. H2SO4 2. Hãy nêu phương pháp nhận biết 3 dung dịch đựng trong 3 lọ mất nhãn sau: KOH, H2SO4, H2O I/ Trắc nghiệm khách quan (1,5đ ) * Khoanh tròn vào đáp án đứng trước câu trả lời đúng Câu 1: Để thu khí hiđro trong phòng thí nghiệm bằng cách đẩy nước ngư ời ta dựa vào tính chất nào của Hiđro: A. Nhẹ hơn không khí B. Không tác dụng với nư ớc C. Không tác dụng với KK D. Nhẹ hơn KK và ít tan trong n ước Câu 2: Cho các chất sau chất nào không tác dụng được với nước: A. Al B. CaO C. K D.SO3 Câu 3: Loại chất làm quì tím chuyển màu xanh là: A. oxit B. axit C. bazơ D. muối II/ Tự luận (6đ ) Câu 4: (3đ) Nước có vai trò gì trong TN và đời sống con người? Để bảo vệ nguồn nước, theo em chúng ta cần phải làm gì? Câu 5: (3đ) Cho 6,5 gam Zn tác dụng với dung dịch HCl d ư. a. Viết phư ơng trình phản ứng hoá học xảy ra. b. Tính thể tích khí (đktc) thu đư ợc sau phản ứng. c. Tính khối lư ợng muối thu đ ược sau phản ứng. (Cho biết Zn = 65; H = 1; Cl = 35,5 ; O = 16) C/ Đáp án, thang điểm: Chủ đề: 2,5đ 1. Mỗi đáp án đúng đạt 0,25đ 1 a b Đáp án D B 2. Lấy ba mẩu giấy quỳ tím cho vào ba lọ, lọ nào làm quỳ tím chuyển thành màu đỏ lọ đó là H2SO4. Lọ nào làm quỳ tím chuyển thành màu xanh, lọ đó đựng KOH . Lọ còn lại là nước. I/ Trắc nghiệm khách quan: 1,5đ Mỗi câu đúng đạt 0,5đ Câu 1 2 3 Đáp án D A C II/ Tự luận: 6đ Câu Nội dung Điểm 4 HS nêu được vai trò của nước HS nêu được biện pháp bảo vệ nguồn nước 1,5 1,5 5 nZn = = 0,1 mol a. Ph ương trình phản ứng Zn + 2HCl ZnCl2 + H2 b. Tính thể tích khí (đktc) thu đ ược sau phản ứng. Theo PTHH số mol của Zn bằng số mol của H2 = 0,1 mol Thể tích khí H2 thu đ ược là: V = 22,4.0,1 = 2,24 lít c. Tính khối lư ợng muối thu đ ược sau phản ứng Theo PTHH thì số mol ZnCl2 bằng số mol Zn = 0, 1 mol Khối lư ợng của ZnCl2 thu đ ược là: n = 0,1.136 = 13,6 g 0,5 0,5 1 1 4/ Củng cố - Giáo viên nhận xét giờ kiểm tra 5/ Dặn dò, hướng dẫn về nhà - Tiếp tục ôn tập các kiến thức đã học và đọc tr
Tài liệu đính kèm:
 hoa_8.doc
hoa_8.doc





