Đề kiểm tra giữa học kỳ môn Khoa học tự nhiên 7 (Chân trời sáng tạo) - Năm học 2023-2024 (Có đáp án)
Câu 1. Cho các bước phương pháp tìm hiểu tự nhiên: 1-Hình thành giả thiết. 2-Quan sát và dặt câu hỏi. 3- Thực hiện kế hoạch . 4- Kết luận. 5- Lập kế hoạch kiểm tra giả thiết. Trình tự sắp xếp đúng là:
1,2,3,4,5 B. 2,1,5,3,4
C. 2,3,5,1,4 D. 5,1,2,4,3.
Câu 2. “ Em hãy sắp xếp các động vật sau thành các nhóm: hươu, tôm, gà, ngựa, trai ”. Để thực hiện được yêu cầu trên em cần có kĩ năng:
Phân loại B. liên kết C. quan sát D. dự báo.
Câu 3. Khi học KHTN, để mô tả một hiện tượng xảy ra, em cần có kĩ năng:
Phân loại B. liên kết C. quan sát D. dự báo.
Câu 4. Để đo nhiệt độ của cốc nước ấm ở nhiệt độ phòng em cần dùng dụng cụ:
Dao động kí B. ẩm kế C. nhiệt kế D. thước đo.
Câu 5. Nguyên tử cấu tạo gồm:
Hạt nhân B. hạt nhân và electron
C. lớp vỏ và proton D. lớp vỏ và hạt nhân.
Câu 6. Hạt chuyển động xung quanh hạt nhân là:
Electron B. proton C. neutron D. cả 3 ý
Câu 7. Trong nguyên tử luôn có:
n = p B. p = e C. e = n D. e = n + p
Câu 8. KHHH của nguyên tố Calcium là:
Ca B. C C. Cal D. Cl
Câu 9. KHHH của nguyên tố Iron là:
I B. Ir C. Fe D. F.
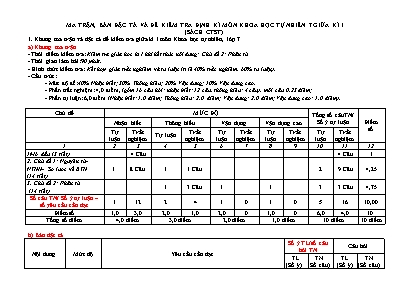
MA TRẬN, BẢN ĐẶC TẢ VÀ ĐỀ KIỂM TRA ĐỊNH KÌ MÔN KHOA HỌC TỰ NHIÊN 7 GIỮA KÌ I (SÁCH CTST) 1. Khung ma trận và đặc tả đề kiểm tra giữa kì I môn Khoa học tự nhiên, lớp 7 a) Khung ma trận - Thời điểm kiểm tra: Kiểm tra giữa học kì I khi kết thúc nội dung: Chủ đề 2: Phân tử - Thời gian làm bài:90 phút. - Hình thức kiểm tra: Kết hợp giữa trắc nghiệm và tự luận (tỉ lệ 40% trắc nghiệm, 60% tự luận). - Cấu trúc: - Mức độ đề:40% Nhận biết; 30% Thông hiểu; 20% Vận dụng; 10% Vận dụng cao. - Phần trắc nghiệm: 4,0 điểm, (gồm 16 câu hỏi: nhận biết: 12 câu, thông hiểu: 4 câu), mỗi câu 0,25 điểm; - Phần tự luận: 6,0 điểm (Nhận biết: 1,0 điểm; Thông hiểu: 2,0 điểm; Vận dụng: 2,0 điểm; Vận dụng cao: 1,0 điểm). Chủ đề MỨC ĐỘ Tổng số câuTN/ Số ý tự luận Điểm số Nhận biết Thông hiểu Vận dụng Vận dụng cao Tự luận Trắc nghiệm Tự luận Trắc nghiệm Tự luận Trắc nghiệm Tự luận Trắc nghiệm Tự luận Trắc nghiệm 1 2 3 4 5 6 7 8 9 10 11 12 1Mở đầu (5 tiết) 4 Câu 4 Câu 1 2. Chủ đề 1: Nguyên tử- NTHH- Sơ lược về BTH (14 tiết) 1 8 Câu 1 1 Câu 2 9 Câu 4,25 3. Chủ đề 2: Phân tử (14 tiết) 1 3 Câu 1 1 3 3 Câu 4,75 Số câu TN/ Số ý tự luận – số yêu cầu cần đạt 1 12 2 4 1 0 1 0 5 16 10,00 Điểm số 1,0 3,0 2,0 1,0 2,0 0 1,0 0 6,0 4,0 10 Tổng số điểm 4,0 điểm 3,0 điểm 2,0 điểm 1,0 điểm 10 điểm 10 điểm b) Bản đặc tả Nội dung Mức độ Yêu cầu cần đạt Số ý TL/số câu hỏi TN Câu hỏi TL (Số ý) TN (Số câu) TL (Số ý) TN (Số câu) 1. Mở đầu (5 tiết) 4 Nhận biết - Xác định được các bước phương pháp tìm hiểu KHTN 1 C1 - Xác định được kĩ năng cần khi học KHTN - Biết chọn dụng cụ đo hợp lí 3 C2-3 C4 2. Nguyên tử- NTHH- Sơ lược về BTH ( 14 tiết ) 2 9 – Nguyên tử Nhận biết Nắm được cấu tạo của nguyên tử 3 C5-7 – Nguyên tố hóa học Nhận biết – Nhận biết được KHHH của nguyên tố 2 C8-9 Thông hiểu – Phát hiện được KHHH sai và biết sửa lại 1 C17 Sơ lược về bảng tuần hoàn Nhận biết – Ghi nhớ các khái niệm nhóm, chu kì. 2 C10-11 Nhận biết được nhóm các nguyên tố kim loại và phi kim 2 C12-13 Thông hiểu – Từ vị trí đọc được tên, KHHH, KLNT và ngược lại 1 C18 3. Phân tử (14 tiết) - Phân tử- Đơn chất- Hợp chất - Giới thiệu về liên kết hóa học. - Hóa trị và CTHH. Thông hiểu Từ CTHH phân biệt được đơn chất và hợp chất 1 C19 – Từ cấu tạo nhận ra CTHH của chất 1 C14 – Sự hình thành các ion, loại liên kết 2 C15-16 Vận dụng – Từ CTHH xác định được hóa trị của nguyên tố hoặc nhóm nguyên tử. 1 C20 Vận dụng cao Lập được CTHH của hợp chất khi biết hóa trị các nguyên tố. 1 C21 c) Đề kiểm tra ĐỀ KIỂM TRA GIỮA HỌC KỲ I NĂM HỌC 2023-2024 MÔN KHOA HỌC TỰ NHIÊN LỚP 7 Thời gian làm bài 90 phút A. TRẮC NGHIỆM: (4,0 điểm). Chọn phương án trả lời đúng cho các câu sau: Câu 1. Cho các bước phương pháp tìm hiểu tự nhiên: 1-Hình thành giả thiết. 2-Quan sát và dặt câu hỏi. 3- Thực hiện kế hoạch . 4- Kết luận. 5- Lập kế hoạch kiểm tra giả thiết. Trình tự sắp xếp đúng là: 1,2,3,4,5 B. 2,1,5,3,4 C. 2,3,5,1,4 D. 5,1,2,4,3. Câu 2. “ Em hãy sắp xếp các động vật sau thành các nhóm: hươu, tôm, gà, ngựa, trai”. Để thực hiện được yêu cầu trên em cần có kĩ năng: Phân loại B. liên kết C. quan sát D. dự báo. Câu 3. Khi học KHTN, để mô tả một hiện tượng xảy ra, em cần có kĩ năng: Phân loại B. liên kết C. quan sát D. dự báo. Câu 4. Để đo nhiệt độ của cốc nước ấm ở nhiệt độ phòng em cần dùng dụng cụ: Dao động kí B. ẩm kế C. nhiệt kế D. thước đo. Câu 5. Nguyên tử cấu tạo gồm: Hạt nhân B. hạt nhân và electron C. lớp vỏ và proton D. lớp vỏ và hạt nhân. Câu 6. Hạt chuyển động xung quanh hạt nhân là: Electron B. proton C. neutron D. cả 3 ý Câu 7. Trong nguyên tử luôn có: n = p B. p = e C. e = n D. e = n + p Câu 8. KHHH của nguyên tố Calcium là: Ca B. C C. Cal D. Cl Câu 9. KHHH của nguyên tố Iron là: I B. Ir C. Fe D. F. Câu 10. Chu kì là những nguyên tố có cùng..trong nguyên tử được sắp xếp vào hàng ngang trong bảng tuần hoàn. Từ trong dấu..là: Số electron B. số proton C. số lớp electron D số hạt nhân Câu 11. Nhóm gồm các nguyên tố kim loại là: Na, K, Au, Fe. B. O, S, P, Cl C. Ne, Ag, He, Rn D. Mg, S, O, Fe. Câu 12. Nhóm gồm các nguyên tố phi kim là: Na, K, Au, Fe. B. O, S, P, Cl C. Ne, Ag, He, Rn D. Mg, S, O, Fe. Câu 13. Nhóm gồm: 1- Các NTHH theo cột. 2- có số lớp e bằng nhau. 3- có tính chất hóa học tương tự nhau. 4. Có số e lớp ngoài cùng bằng nhau. Các phát biểu đúng là: 1, 3, 4 B. 1, 2, 3 C. 1, 3, 4 D cả 4 Câu 14. Nguyên tử kim loại Na nhường 01 electron lớp ngoài cùng trở thành: Ion B. nguyên tử dương C. ion âm D. ion dương. Câu 15. Mỗi nguyên tử Oxygen góp chung 2 e để hình thành phân tử Oxygen gồm 2 nguyên tử. Liên kết trong phân tử Oxygen là: Góp chung e B. ion C. cộng hóa trị D. cả B và C. Câu 16. Phân tử Methane gồm 01 nguyên tử C liên kết với 04 nguyên tử H. CTHH của Methane là: H4C B. CH4 C. H4C D. CH4 TỰ LUẬN: (6đ) Câu 17. (1đ). Các KHHH nào sau đây viết sai? Nếu sai sửa lại cho đúng và đọc tên nguyên tố? He, MG, Na, FE, BA, Au. Câu 18. (1đ). Hoàn thành thông tin trong các ô còn trống của bảng: Tên nguyên tố KHHH Số hiệu nguyên tử Số electron trong nguyên tử Khối lượng nguyên tử, 12 Na Iron 15 Câu 19.(1đ) Dựa vào CTHH hãy phân biệt các chất sau: O2, SO2, Ca, NaCl , CaCO3, Mg, Fe, H 2O và H2 thành 2 nhóm đơn chất và hợp chất? Câu 20.(2đ) Em hãy xác định hóa trị của nguyên tố hoặc nhóm nguyên tử trong các hợp chất: Hợp chất NH3 Fe2O3 H2S SO3 CH4 CO H3PO4 H2SO4 Nguyên tố/nhóm nguyên tử (2) N Fe S S C C PO4 SO4 Hóa trị của (2) Câu 21. (1đ). Xác định CTHH của hợp chất aluminium oxide có cấu tạo từ: Al- III và O ? d. Đáp án. A. Trắc nghiệm: mỗi ý đúng được 0,25đ. 1B, 2A, 3D, 4C, 5D, 6A, 7B, 8A, 9C, 10C, 11A, 12B, 13A, 14D, 15C, 16D TỰ LUẬN: (6đ) Câu 17. Xác định đúng KHHH đúng và sai được 0,5đ, đọc đúng tên các nguyên tố được 0,5đ. KHHH đúng: - He: helium. - Na: Sodium. – Au: Gold. KHHH sai: MG, FE, BA. Sửa lại các KHHH sai: Mg: Magnesium. – Fe: Iron. – Ba: Barium. Câu 18. Hoàn thành đúng mỗi nguyên tố được 0,25đ. Tên nguyên tố KHHH Số hiệu nguyên tử Số electron trong nguyên tử Khối lượng nguyên tử, Carbon C 6 6 12 Sodium Na 11 11 23 Iron Fe 26 26 56 Photphorus P 15 15 31 Câu 19. Phân biệt đúng mỗi nhóm được 0,5đ. Đơn chất: O2, Ca, Fe, H2, Mg. Hợp chất: SO2, NaCl, CaCO3, H2O. Câu 19. Xác định đúng hóa trị của mỗi nguyên tố hay nhóm nguyên tử được 0,25đ. Hợp chất NH3 Fe2O3 H2S SO3 CH4 CO H3PO4 H2SO4 Nguyên tố/nhóm nguyên tử (2) N Fe S S C C PO4 SO4 Hóa trị của (2) III III II VI IV II III II Câu 21. H làm đúng mỗi bước được 0,25đ. CTHH chung: AlxIIIOIIy Theo QTHT, ta có: x.III = y.II Chuyển thành tỉ lệ: x : y = II : III = 2 : 3 Vậy x = 2, y = 3. CTHH của hợp chất: Al2O3.
Tài liệu đính kèm:
 de_kiem_tra_giua_hoc_ky_mon_khoa_hoc_tu_nhien_7_chan_troi_sa.doc
de_kiem_tra_giua_hoc_ky_mon_khoa_hoc_tu_nhien_7_chan_troi_sa.doc






