Đề kiểm tra giữa học kỳ I môn Khoa học tự nhiên Lớp 7 (Cánh diều) - Năm học 2022-2023 - Trường THCS Bản Lầu (Có đáp án)
I. PHẦN TRẮC NGHIỆM (5,0 điểm)
Hãy khoanh tròn vào chữ cái đứng trước câu trả lời đúng trong các câu sau.
Câu 1: Bước làm nào sau đây không thuộc phương pháp tìm hiểu tự nhiên?
Đề xuất vấn đề cần tìm hiểu
Đưa ra dự đoán khoa học để giải quyết vấn đề
Lập kế hoạch sinh hoạt cá nhân
Viết báo cáo. Thảo luận và trình bày báo cáo khi được yêu cầu
Câu 2: Cho một số kĩ năng sau:
Kĩ năng chiến đấu đặc biệt
Kĩ năng dự đoán
Kĩ năng quan sát
Kĩ năng đo đạc
Số kĩ năng thường sử dụng trong học tập môn KHTN là
1 B. 2 C. 3 D. 4
Câu 3: Trong các loại hạt cấu tạo nên nguyên tử, hạt mang điện tích âm là
A. electron. B. electron và neutron.
C. proton. D. proton và neutron.
Câu 4: Khối lượng nguyên tử được đo theo đơn vị quốc tế là:
amu B. đvC C. U D. gam
Câu 5: Cho sơ đồ nguyên tử nitrogen như sau.
Số hạt mang điện trong nguyên tử nitrogen là
A. 7 B. 14
C. 21 D. không xác định được
Câu 6: Nguyên tố hóa học là tập hợp nguyên tử cùng loại có
A. cùng số neutron trong hạt nhân.
B. cùng số proton trong hạt nhân.
C. cùng số electron trong hạt nhân.
D. cùng số proton và số neutron trong hạt nhân.
Câu 7: Đến nay con người đã tìm ra bao nhiêu nguyên tố hóa học
A. 90 B. 100 C. 118 D. 108
Câu 8: Nguyên tố Sodium có kí hiệu hóa học là
A. NA
B. Na
C. na
D. nA
Câu 9: Hình dưới đây mô tả cấu tạo nguyên tử oxygen.
Cho biết số hiệu nguyên tử (số proton) của nguyên tố oxygen là
A. 6
B. 7
C. 8
D. 9
Câu 10: Cho biết sơ đồ cấu tạo nguyên tử của nguyên tố như hình dưới.
Nguyên tố trên là
A. Be B. C C. O D. Na
Câu 11: Bảng tuần hoàn các nguyên tố hoá học được cấu tạo từ
A. Ô nguyên tố, chu kì, nhóm B. Chu kì, nhóm
C. Ô nguyên tố D. Chu kì
Câu 12: Các kim loại kiềm trong nhóm IA đều có số electron lớp ngoài cùng là
A. 1e
B. 2e
C. 3e
D. 7e
Câu 13: Phân tử là
A. hạt đại diện cho chất, được tạo bởi một nguyên tố hóa học
B. hạt đại diện cho hợp chất, được tạo bởi nhiều nguyên tố hóa học
C. hạt đại diện cho chất do một hoặc nhiều nguyên tử kết hợp với nhau và thể hiện đầy đủ tính chất của chất
D. hạt nhỏ nhất do các nguyên tố hóa học kết hợp với nhau tạo thành chất
Câu 14: Cặp phân tử nào sau đây là đơn chất ?
A. CO, O2. B. NaCl, O3 C. H2, O2 D. O2, H2S
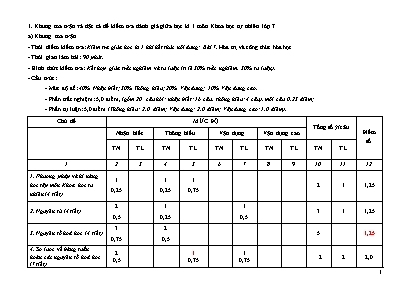
1. Khung ma trận và đặc tả đề kiểm tra đánh giá giữa học kì 1 môn Khoa học tự nhiên lớp 7 a) Khung ma trận - Thời điểm kiểm tra: Kiểm tra giữa học kì 1 khi kết thúc nội dung: Bài 7. Hóa trị và công thức hóa học - Thời gian làm bài: 90 phút. - Hình thức kiểm tra: Kết hợp giữa trắc nghiệm và tự luận (tỉ lệ 50% trắc nghiệm, 50% tự luận). - Cấu trúc: - Mức độ đề: 40% Nhận biết; 30% Thông hiểu; 20% Vận dụng; 10% Vận dụng cao. - Phần trắc nghiệm: 5,0 điểm, (gồm 20 câu hỏi: nhận biết: 16 câu, thông hiểu: 4 câu), mỗi câu 0,25 điểm; - Phần tự luận: 5,0 điểm (Thông hiểu: 2,0 điểm; Vận dụng: 2,0 điểm; Vận dụng cao: 1,0 điểm). Chủ đề MỨC ĐỘ Tổng số ý/câu Điểm số Nhận biết Thông hiểu Vận dụng Vận dụng cao TN TL TN TL TN TL TN TL TN TL 1 2 3 4 5 6 7 8 9 10 11 12 1. Phương pháp và kĩ năng học tập môn Khoa học tự nhiên (4 tiết) 1 0,25 1 0,25 1 0,75 2 1 1,25 2. Nguyên tử (4 tiết) 2 0,5 1 0,25 1 0,5 3 1 1,25 3. Nguyên tố hoá học (4 tiết) 3 0,75 2 0,5 5 1,25 4. Sơ lược về bảng tuần hoàn các nguyên tố hoá học (7 tiết) 2 0,5 1 0,75 1 0,75 2 2 2,0 5. Phân tử- Đơn chất – Hợp chất (5 tiết) 3 0,75 1 0,75 3 1 1,5 6. Giới thiệu về liên kết hoá học (4 tiết) 3 0,75 1 0,5 3 1 1,25 7. Hoá trị và công thức hoá học (5 tiết) 2 0,5 1 1,0 2 1 1,5 Tổng số câu/ý 16 4 3 3 1 20 7 Điểm số 4 1 2 2 1 5 5 10 Tổng số điểm 4,0 3,0 2,0 1,0 10 10 b) Bản đặc tả Nội dung Mức độ Yêu cầu cần đạt Số ý TL/số câu hỏi TN Câu hỏi TL (Số ý) TN (Số câu) TL (Số ý) TN (Số câu) 1. Phương pháp và kĩ năng học tập môn Khoa học tự nhiên (5 tiết) 2 Một số phương pháp trong học tập môn Khoa học tự nhiên (Phương pháp tìm hiểu tự nhiên; kĩ năng tiến trình: quan sát, phân loại, liên kết, đo, dự báo) Nhận biết Biết được các bước số phương pháp tìm hiểu tự nhiên 1 C1 Biết cách sử dụng được một số dụng cụ đo trong môn Khoa học tự nhiên 7 Thông hiểu Ghi nhớ được một số kỹ năng thường sử dụng học tập môn KHTN 1 C2 Lựa chọn được một số dụng cụ đo trong trường hợp cụ thể (trong nội dung môn Khoa học tự nhiên 7) và xác định được các kĩ năng: quan sát, phân loại, liên kết, đo, dự báo 1 C21 Vận dụng Vận dụng phương pháp tìm hiểu tự nhiên và các kĩ năng tiến trình (quan sát, phân loại, liên kết, đo, dự báo) để tìm hiểu các hiện tượng tự nhiên trong học tập môn Khoa học tự nhiên Làm được báo cáo, thuyết trình. Vận dung cao Vận dung các phương pháp học tập môn khoa học tự nhiên đề xuất phương pháp bảo vệ môi trường; 2. Nguyên tử (6 tiết) - Mô hình nguyên tử của Rutherford – Bohr (mô hình sắp xếp electron trong các lớp vỏ nguyên tử). - Khối lượng của một nguyên tử theo đơn vị quốc tế amu (đơn vị khối lượng nguyên tử). Nhận biết Biết thành phần cấu tạo nguyên tử 1 C3 Biết được mô hình nguyên tử của Rutherford – Bohr (mô hình sắp xếp electron trong các lớp vỏ nguyên tử). Biết được khối lượng của một nguyên tử theo đơn vị quốc tế amu (đơn vị khối lượng nguyên tử). 1 C4 Thông hiểu Trình bày được mô hình nguyên tử của Rutherford – Bohr (mô hình sắp xếp electron trong các lớp vỏ nguyên tử). Nêu được khối lượng của một nguyên tử theo đơn vị quốc tế amu (đơn vị khối lượng nguyên tử). Hiểu cấu tạo nguyên tử; khối lượng của các nguyên tử; điện tích của các thành phần cấu tạo nên nguyên tử. 1 C5 Giải thích được tại sao nguyên tử trung hòa về điện. Giải thích được vì sao khối lượng hạt nhân là khối lượng nguyên tử Vận dụng Từ mô hình nguyên tử, xác định số lượng các thành phần cấu tạo nên nguyên tử. 1 C22 Từ số lượng các thành phần cấu tạo nên nguyên tử . Vẽ sơ đồ và mô tả cấu tạo nguyên tử theo mô hình. Vận dung cao Giải các bài tập liên quan đến các loại hạt cấu tạo nên nguyên tử 3. Nguyên tố hoá học (3 tiết) - Phát biểu được khái niệm về nguyên tố hoá học và kí hiệu nguyên tố hoá học. - Viết được công thức hoá học và đọc được tên của 20 nguyên tố đầu tiên. Nhận biết Biết được khái niệm về nguyên tố hoá học và kí hiệu nguyên tố hoá học. 1 C6 Biết số lượng nguyên tố hoá học con người đã tìm ra 1 C7 Biết được công thức hoá học và đọc được tên của 20 nguyên tố đầu tiên. 1 C8 Thông hiểu Hiểu được khái niệm về nguyên tố hoá học và kí hiệu nguyên tố hoá học Từ mô hình nguyên tử xác định số lượng các loại hạt trong nguyên tử của nguyên tố. 1 C9 Từ mô hình nguyên tử xác định số hiệu nguyên tử của nguyên tố 1 C10 Từ tên nguyên tố hoá học, viết được kí hiệu của nguyên tố hoá học và ngược lại Vận dụng Xác định được khối lượng các hạt và khối lượng nguyên tử theo đơn vị amu. Vận dụng cao Viết một đoạn văn ngắn khoảng 100 từ về đề tài “Mô tả vai trò của các nguyên tố hoá học trong cuộc sống con người”. Tìm hiểu thành phần của muối ăn và nêu vai trò của muối ăn với con người - Vận dụng hiểu biết về NTHH vào thực tế cuộc sống (xác định nguyên tố dinh dưỡng cần cho cây, NTHH có trong nhãn mác của thuốc,) 4. Sơ lược về bảng tuần hoàn các nguyên tố hoá học (7 tiết) -Nêu được các nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hoá học. - Mô tả được cấu tạo bảng tuần hoàn gồm: ô, nhóm, chu kì. - Sử dụng được bảng tuần hoàn để chỉ ra các nhóm nguyên tố/nguyên tố kim loại, các nhóm nguyên tố/nguyên tố phi kim, nhóm nguyên tố khí hiếm trong bảng tuần hoàn. Nhận biết Biết được các nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hoá học và cấu tạo bảng tuần hoàn gồm: ô, nhóm, chu kì. 1 C11 Biết số electron lớp ngoài cùng của các nguyên tố trong các nhóm chính 1 C12 Thông hiểu Sử dụng được bảng tuần hoàn để chỉ ra các nhóm nguyên tố/nguyên tố kim loại, các nhóm nguyên tố/nguyên tố phi kim, nhóm nguyên tố khí hiếm trong bảng tuần hoàn. Từ số hiệu nguyên tử xác định số thứ tự, tên và KHHH của nguyên tố trong bảng tuần hoàn 1 C23a Vận dụng Dựa vào Số hiệu nguyên tử xác định vị trí (ô nguyên tố, chu kỳ, nhóm) của nguyên tố trong bảng tuần hoàn. Từ số hiệu nguyên tử xác định số lượng hạt e, p của nguyên tử và ngược lại. Vận dụng xác định được vị trí của một số NTHH có nhiều ứng dụng trong đời sống. - Giải thích được một số ứng dụng của một số NTHH trong bảng tuần hoàn 1 C23b 5. Phân tử- Đơn chất – Hợp chất (4 tiết) Nêu được khái niệm phân tử, đơn chất, hợp chất. Đưa ra được một số ví dụ về đơn chất và hợp chất. Tính được khối lượng phân tử theo đơn vị amu. Nhận biết Nhận biết được khái niệm phân tử, đơn chất, hợp chất. 1 C13 Biết được công thức hoá học của đơn chất phân tử, đơn chất, hợp chất. 2 C14, C15 Thông hiểu Phân biệt đơn chất và hợp chất Xác định được các hợp chất trong dãy các chất. Giải thích được một số chất trong tự nhiên là đơn chất hay hợp chất Vận dụng Tính được khối lượng phân tử theo đơn vị amu. Giải thích được một số ứng dụng của đơn chất, hợp chất. 1 C24 6. Giới thiệu về liên kết hoá học (4 tiết) Nêu được mô hình sắp xếp electron trong vỏ nguyên tử của một số nguyên tố khí hiếm; sự hình thành liên kết cộng hoá trị theo nguyên tắc dùng chung electron để tạo ra lớp vỏ electron của nguyên tố khí hiếm (Áp dụng được cho các phân tử đơn giản như H2, Cl2, NH3, H2O, CO2, N2,.). ion có lớp vỏ electron của nguyên tố khí hiếm (Áp dụng cho phân tử đơn giản như NaCl, MgO,). – Chỉ ra được sự khác nhau về một số tính chất của chất ion và chất cộng hoá trị. Nhận biết Biết được các loại liên kết hoá học 1 C16 Biết được một số hợp chất được tạo thành từ loại liên kết nào 1 C17 Biết số lượng cặp electron dùng chung để hình trong liên kết cộng hoá trị trong các phân tử chất. 1 C18 Thông hiểu Vẽ được mô hình tạo thành các ion âm và ion dương 1 C25 Vẽ được mô hình sắp xếp electron trong vỏ nguyên tử của một số nguyên tố khí hiếm; sự hình thành liên kết cộng hoá trị theo nguyên tắc dùng chung electron để tạo ra lớp vỏ electron của nguyên tố khí hiếm (Áp dụng được cho các phân tử đơn giản như H2, Cl2, NH3, H2O, CO2, N2,.). Vẽ được mô hình tạo thành liên kết ion theo nguyên tắc cho và nhận electron để tạo ra ion có lớp vỏ electron của nguyên tố khí hiếm (Áp dụng cho phân tử đơn giản như NaCl, MgO,). Chỉ ra được sự khác nhau về một số tính chất của chất ion và chất cộng hoá trị. Vận dụng - Mô tả và vẽ được sơ đồ quá trình tạo thành liên kết trong các phân tử - Giải thích được ứng dụng của liên kết hoá học trong cuộc sống 7. Hoá trị và công thức hoá học (3 tiết) -Khái niệm về hoá trị (cho chất cộng hoá trị). Cách viết công thức hoá học. -Viết công thức hoá học của một số chất và hợp chất đơn giản thông dụng. - Mối liên hệ giữa hoá trị của nguyên tố với công thức hoá học. -Thành phần trăm (%) nguyên tố trong hợp chất Nhận biết Biết được khái niệm hoá trị (cho chất cộng hoá trị). 1 C19 Phát biểu được quy tắc hóa trị Trình bày được khái niệm về hoá trị (cho chất cộng hoá trị). Cách viết công thức hoá học của đơn chất và hợp chất Biết được ý nghĩa của CTHH 1 C20 Thông hiểu Xác định được công thức hóa học của hợp chất khi biết hóa trị của các nguyên tố tạo nên hợp chất. Hiểu được mối liên hệ giữa hoá trị của nguyên tố với công thức hoá học. Vận dụng Tính được phần trăm (%) nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất. Vận dụng cao Lập được công thức hóa học dựa vào hóa trị của nguyên tố Xác định được công thức hoá học của hợp chất dựa vào phần trăm (%) nguyên tố và khối lượng phân tử. 1 C26 2. Đề kiểm tra TRƯỜNG THCS XÃ BẢN LẦU Họ và tên: .................................. Lớp 7..... ĐỀ 1 KIỂM TRA GIỮA HỌC KÌ I Môn: Khoa học tự nhiên 7 Năm học 2022 - 2023 (Thời gian: 90 phút không kể thời gian giao đề) (Đề gồm 26 câu, 03 trang) I. PHẦN TRẮC NGHIỆM (5,0 điểm) Hãy khoanh tròn vào chữ cái đứng trước câu trả lời đúng trong các câu sau. Câu 1: Bước làm nào sau đây không thuộc phương pháp tìm hiểu tự nhiên? Đề xuất vấn đề cần tìm hiểu Đưa ra dự đoán khoa học để giải quyết vấn đề Lập kế hoạch sinh hoạt cá nhân Viết báo cáo. Thảo luận và trình bày báo cáo khi được yêu cầu Câu 2: Cho một số kĩ năng sau: Kĩ năng chiến đấu đặc biệt Kĩ năng dự đoán Kĩ năng quan sát Kĩ năng đo đạc Số kĩ năng thường sử dụng trong học tập môn KHTN là 1 B. 2 C. 3 D. 4 Câu 3: Trong các loại hạt cấu tạo nên nguyên tử, hạt mang điện tích âm là A. electron. B. electron và neutron. C. proton. D. proton và neutron. Câu 4: Khối lượng nguyên tử được đo theo đơn vị quốc tế là: amu B. đvC C. U D. gam Câu 5: Cho sơ đồ nguyên tử nitrogen như sau. Số hạt mang điện trong nguyên tử nitrogen là A. 7 B. 14 C. 21 D. không xác định được Câu 6: Nguyên tố hóa học là tập hợp nguyên tử cùng loại có A. cùng số neutron trong hạt nhân. B. cùng số proton trong hạt nhân. C. cùng số electron trong hạt nhân. D. cùng số proton và số neutron trong hạt nhân. Câu 7: Đến nay con người đã tìm ra bao nhiêu nguyên tố hóa học A. 90 B. 100 C. 118 D. 108 Câu 8: Nguyên tố Sodium có kí hiệu hóa học là A. NA B. Na C. na D. nA Câu 9: Hình dưới đây mô tả cấu tạo nguyên tử oxygen. Cho biết số hiệu nguyên tử (số proton) của nguyên tố oxygen là A. 6 B. 7 C. 8 D. 9 Câu 10: Cho biết sơ đồ cấu tạo nguyên tử của nguyên tố như hình dưới. Nguyên tố trên là A. Be B. C C. O D. Na Câu 11: Bảng tuần hoàn các nguyên tố hoá học được cấu tạo từ A. Ô nguyên tố, chu kì, nhóm B. Chu kì, nhóm C. Ô nguyên tố D. Chu kì Câu 12: Các kim loại kiềm trong nhóm IA đều có số electron lớp ngoài cùng là A. 1e B. 2e C. 3e D. 7e Câu 13: Phân tử là A. hạt đại diện cho chất, được tạo bởi một nguyên tố hóa học B. hạt đại diện cho hợp chất, được tạo bởi nhiều nguyên tố hóa học C. hạt đại diện cho chất do một hoặc nhiều nguyên tử kết hợp với nhau và thể hiện đầy đủ tính chất của chất D. hạt nhỏ nhất do các nguyên tố hóa học kết hợp với nhau tạo thành chất Câu 14: Cặp phân tử nào sau đây là đơn chất ? A. CO, O2. B. NaCl, O3 C. H2, O2 D. O2, H2S Câu 15: Phân tử nào dưới đây là hợp chất? A. C. B. NaCl. C. H2. D. O2. Câu 16: Liên kết ion là Liên kết giữa ion dương và ion âm Liên kết giữa các nguyên tử kim loại với nhau Liên kết giữa các nguyên tử phi kim với nhau Liên kết giữa nguyên tử kim loại với nguyên tử khí hiếm Câu 17: Hợp chất nào sau đây được tạo thành nhờ liên kết cộng hóa trị NH3 B. NaCl C. CuO D. K2S Câu 18: Trong phân tử O2, hai nguyên tử O đã liên kết với nhau bằng A. 1 cặp electron dùng chung B. 2 cặp electron dùng chung C. 3 cặp electron dùng chung D. 4 cặp electron dùng chung Câu 19: Con số biểu thị khả năng liên kết của nguyên tử nguyên tố này với nguyên tử nguyên tố khác là A. Số hiệu nguyên tử B. Hoá trị C. Khối lượng nguyên tử D. Số liên kết của các nguyên tử Câu 20: Phân tử của hợp chất carbon dioxide có công thức hóa học là CO2. Điều nào đúng khi nói về công thức hóa học trên? chứa một nguyên tử carbon và hai nguyên tử oxygen chứa một phân tử carbon và hai phân tử oxygen chứa một nguyên tử carbon và một nguyên tử oxygen chứa một nguyên tử carbon và một phân tử oxygen II. PHẦN TỰ LUẬN (5,0 điểm) Câu 21 (0,75 điểm) Cho một cốc nước ấm để trong điều kiện nhiệt độ phòng. a. Em hãy lựa chọn các dụng cụ, thiết bị phù hợp có trong phòng thí nghiệm để xác định nhiệt độ và thể tích của nước trong cốc. b. Em đã sử dụng các kĩ năng nào để giải quyết các vấn đề trên? Câu 22 (0,5 điểm) Quan sát hình mô phỏng cấu tạo nguyên tử dưới đây và hãy xác định số lượng các loại hạt p, e của nguyên tử Chlorine (Cl)? (Sơ đồ cấu tạo nguyên tử Cl) Câu 23 (1,5 điểm) Nguyên tố X có số hiệu nguyên tử là 15. Dựa vào bảng tuần hoàn các nguyên tố hóa học: a. Hãy xác định số thứ tự, tên và kí hiệu hóa học của nguyên tố X. b. Một kim loại ở thể lỏng trong điều kiện thường được ứng dụng để chế tạo nhiệt kế. Đó là kim loại nào? Cho biết vị trí (nhóm, chu kì ) của nguyên tố kim loại đó? Câu 24 (0,75 điểm) Trong mật ong có nhiều fructose. Phân tử fructose gồm 6 nguyên tử C, 12 nguyên tử H và 6 nguyên tử O. Hãy viết công thức hoá học của fructose và tính khối lượng phân tử fructose? Câu 25 (0,5 điểm) Vẽ sơ đồ tạo thành ion Magnesium từ nguyên tử Magnesium. Biết trong nguyên tử có 12 proton. Câu 26 (1,0 điểm) Một oxide có công thức XOn, trong đó X chiếm 30,43% về khối lượng. Biết khối lượng phân tử của oxide bằng 46 amu. Xác định công thức hoá học của oxide trên. ĐÁP ÁN – HƯỚNG DẪN CHẤM Đề 1 I. PHẦN TRẮC NGHIỆM Câu 1 2 3 4 5 6 7 8 9 10 Đáp án C C A A A B C B C B Câu 11 12 13 14 15 16 17 18 19 20 Đáp án A A C C B A A B B A II. PHẦN TỰ LUẬN Câu ý Nội dung Điểm 21 a - Để đo nhiệt độ nước trong cốc em sử dụng nhiệt kế - Để đo thể tích nước em sử dụng ống đong hoặc cốc có chia độ. 0,25 0,25 b Em đã thực hiện kĩ năng đo để giải quyết vấn đề trên 0,25 22 số p = số e = 17 hạt 0, 5 23 a X ở ô số 15, KHHH là P (Phosphorus) 0,75 b Nguyên tố kim loại là Mercury (Hg) + Nhóm IIB + Chu kì 6 0,25 0,25 0,25 24 Fructose là hợp chất. Phân tử khối Fructose = 12 x 6 + 12 + 16 x 6 = 180 amu 0,25 0,25 25 HS chỉ cần vẽ đúng, không cần vẽ đẹp vẫn ghi điểm tối đa 0,5 26 Khối lượng của X = 30,43 x 46/100 = 14 amu => X là N Khối lượng của O = 46 – 14 = 32 amu Số nguyên tử O = 32: 16 = 2 Vậy công thức cần tìm là NO2 (HS giải cách khác đúng vẫn được điểm tối đa) 0,25 0,25 0,25 0,25 TRƯỜNG THCS XÃ BẢN LẦU Họ và tên: .................................. Lớp 7..... ĐỀ 2 KIỂM TRA GIỮA HỌC KÌ I Môn: Khoa học tự nhiên 7 Năm học 2022 - 2023 (Thời gian: 90 phút không kể thời gian giao đề) (Đề gồm 26 câu, 03 trang) I. PHẦN TRẮC NGHIỆM (5,0 điểm) Hãy khoanh tròn vào chữ cái đứng trước câu trả lời đúng trong các câu sau. Câu 1: Phương pháp tìm hiểu tự nhiên được thực hiện qua mấy bước? A. 3 B. 4. C. 5 D. 6 Câu 2: Đâu không phải là kĩ năng cần vận dụng vào phương pháp tìm hiểu tự nhiên? A. Kĩ năng chiến đấu đặc biệt B. Kĩ năng dự đoán C. Kĩ năng quan sát D. Kĩ năng đo đạc Câu 3: Trong các loại hạt cấu tạo nên nguyên tử, hạt mang điện tích dương là: A. electron. B. electron và neutron. C. proton. D. proton và neutron. Câu 4: Khối lượng nguyên tử được đo theo đơn vị quốc tế là A. amu B. đvC C. U D. gam Câu 5: Cho sơ đồ nguyên tử Chlorine như sau. Số hạt mang điện trong nguyên tử Chlorine là A. 7. B. 14. C. 17. D. không xác định được. Câu 6: Loại hạt nào sau đây là số đặc trưng cho nguyên tố hóa học ? A. neutron B. electron C. proton D. proton và số neutron Câu 7: Số nguyên tố hóa học được tìm thấy trong tự nhiên là A. 118 B. 180 C. 108 D. 98 Câu 8: Nguyên tố Magnesium có kí hiệu hóa học là A. MG B. mg C. Mg D. mG Câu 9: Hình dưới đây mô tả cấu tạo nguyên tử oxygen. Cho biết số hiệu nguyên tử (số proton) của nguyên tố oxygen là A. 6. B. 7. C. 8. D. 9. Câu 10: Cho biết sơ đồ cấu tạo nguyên tử của nguyên tố như hình dưới. Nguyên tố trên là A. Be B. C C. O D. Na Câu 11: Bảng tuần hoàn các nguyên tố hoá học được sắp xếp theo A. thứ tự chữ cái trong từ điển B. thứ tự tăng dần điện tích hạt nhân C. thứ tự tăng dần số hạt electron lớp ngoài cùng D. thứ tự tăng dần số hạt neutron Câu 12: Các kim loại kiềm trong nhóm VIIA đều có số electron lớp ngoài cùng là A. 1e. B. 2e. C. 3e. D. 7e. Câu 13: Hạt đại diện cho chất do một hoặc nhiều nguyên tử kết hợp với nhau và thể hiện đầy đủ tính chất của chất được gọi là A. nguyên tố hóa học. B. nguyên tử C. phân tử D. hạt nhân Câu 14: Cặp phân tử nào sau đây là hợp chất? A. Cl2, O2. B. NaCl, CaCO3 C. H2, O2 D. O3, H2 Câu 15: Phân tử nào dưới đây là đơn chất? A. Cl2. B. NaCl. C. H2.S D. CO2. Câu 16: Liên kết cộng hóa trị là A. liên kết giữa ion dương và ion âm B. liên kết giữa các nguyên tử kim loại với nguyên tử phi kim C. liên kết giữa được hình thành bởi sự dùng chung electron giữa hai nguyên tử D. liên kết giữa nguyên tử kim loại với nguyên tử khí hiếm Câu 17: Hợp chất nào sau đây được tạo thành nhờ liên kết ion A. NH3 B. NaCl C. CO D. H2S Câu 18: Trong phân tử H2, hai nguyên tử H đã liên kết với nhau bằng A. 1 cặp electron dùng chung. B. 2 cặp electron dùng chung. C. 3 cặp electron dùng chung. D. 4 cặp electron dùng chung. Câu 19: Hóa trị là con số biểu thị khả năng liên kết A. của 2 nguyên tử cùng loại B. của nguyên tử nguyên tố đó với nguyên tử khác trong phân tử C. của 2 nguyên tử khác loại D. của 2 nguyên tố khác nhau Câu 20: Phân tử của hợp chất Calcium chloride có công thức hóa học là CaCl2. Điều nào sau đây đúng khi nói về công thức hóa học trên? A. chứa một nguyên tử calcium và hai nguyên tử chlorine B. chứa một nguyên tử calcium và hai phân tử chlorine C. chứa một phân tử calcium và hai nguyên tử chlorine D. chứa một nguyên tử calcium và một phân tử chlorine II. PHẦN TỰ LUẬN (5,0 điểm) Câu 21 (0,75 điểm) Cho một cốc nước ấm để trong điều kiện nhiệt độ phòng. a. Em hãy lựa chọn các dụng cụ, thiết bị phù hợp có trong phòng thí nghiệm để xác định nhiệt độ và khối lượng của nước trong cốc. b. Em đã sử dụng các kĩ năng nào để giải quyết các vấn đề trên? Câu 22 (0,5 điểm) Quan sát hình mô phỏng cấu tạo nguyên tử dưới đây và hãy xác định số lượng các loại hạt p, e của nguyên tử Nitrogen (N)? (Sơ đồ cấu tạo nguyên tử N) Câu 23 (1,5 điểm) Nguyên tố X có số hiệu nguyên tử là 19. Dựa vào bảng tuần hoàn các nguyên tố hóa học: a. Hãy xác định số thứ tự, tên và kí hiệu hóa học của nguyên tố X. b. Cho biết nguyên tố phi kim có trong thành phần của muối ăn? Chúng thuộc chu kì và nhóm nào trong bảng tuần hoàn? Câu 24 (0,75 điểm) Trong mật ong có nhiều fructose. Phân tử fructose gồm 6 nguyên tử C, 12 nguyên tử H và 6 nguyên tử O. Hãy viết công thức hoá học của fructose và tính khối lượng phân tử fructose? Câu 25 (0,5 điểm) Vẽ sơ đồ tạo thành ion Aluminium từ nguyên tử Aluminium. Biết trong nguyên tử có 13 proton. Câu 26 (1,0 điểm) Một oxide có công thức XOn, trong đó X chiếm 80% về khối lượng. Biết khối lượng phân tử của oxide bằng 80 amu. Xác định công thức hoá học của oxide trên. ĐÁP ÁN – HƯỚNG DẪN CHẤM Đề 2 I. PHẦN TRẮC NGHIỆM Câu 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 Đáp án C A C A C C D C C B B D C B A C B A B A II. PHẦN TỰ LUẬN Câu ý Nội dung Điểm 21 a - Để đo nhiệt độ nước trong cốc em sử dụng nhiệt kế - Để đo khối lượng nước em sử dụng cân 0,25 0,25 b Em đã thực hiện kĩ năng đo để giải quyết vấn đề trên 0,25 22 số p = số e = 7 hạt 0, 5 23 a X ở ô số 19 KHHH là K Tên nguyên tố là Potassium 0,25 0,25 0,25 b Nguyên tố kim loại là Fluorine (F) + Nhóm IA + Chu kì 2 0,25 0,25 0,25 24 Fructose là hợp chất. Phân tử khối Fructose = 12 x 6 + 12 + 16 x 6 = 180 amu 0,25 0,25 25 HS chỉ cần vẽ đúng, không cần vẽ đẹp vẫn ghi điểm tối đa 0,5 26 Khối lượng của X = 80 x 80/100 = 64 amu => X là Cu Khối lượng của O = 80 – 64 = 16 amu Số nguyên tử O = 16: 16 = 1 Vậy công thức cần tìm là CuO (HS giải cách khác đúng vẫn được điểm tối đa) 0,25 0,25 0,25 0,25 DUYỆT CỦA BGH DUYỆT CỦA TCM GV RA ĐỀ Lê Thị Bích Hải Nông Thị Sin
Tài liệu đính kèm:
 de_kiem_tra_giua_hoc_ky_i_mon_khoa_hoc_tu_nhien_lop_7_canh_d.docx
de_kiem_tra_giua_hoc_ky_i_mon_khoa_hoc_tu_nhien_lop_7_canh_d.docx






