Đề kiểm tra giữa học kì I môn Khoa học tự nhiên Lớp 7 (Cánh diều) - Trường THCS Nam Tiến (Có đáp án)
Câu 1:Phương pháp tìm hiểu tự nhiên gồm mấy bước?
A. 3. B. 4. C. 5. D. 6.
Câu 2: Đâu không phải là kĩ năng cần vận dụng vào phương pháp tìm hiểu tự nhiên?
A. Kĩ năng chiến đấu đặc biệt;
B. Kĩ năng quan sát;
C. Kĩ năng dự báo;
D. Kĩ năng đo đạc.
Câu 3:Trên cơ sở các số liệu và phân tích số liệu, con người có thể đưa ra các dự
báo hay dự đoán tính chất của sự vật, hiện tượng, nguyên nhân của hiện
tượng . Đó là kĩ năng nào?
A. Kĩ năng quan sát, phân loại.
B. Kĩ năng liên kết tri thức.
C. Kĩ năng dự báo.
D. Kĩ năng đo.
Câu 4: Để đo tốc độ chuyển động ta cần sử dụng các dụng cụ gì?
A. Dụng cụ đo độ dài
B. Dụng cụ đo thời gian
C.Dụng cụ đo khối lượng
D. Cả A và B
Câu 5: Phát biểu nào sau đây không mô tả đúng vỏ nguyên tử theo mô hình nguyêntử của Rơ-dơ-pho - Bo?
A. Electron chuyến động xung quanh hạt nhân theo từng lớp khác nhau tạo
thành các lớp electron.
B. Lớp electron trong cùng gần hạt nhân nhất có tối đa 2 electron, các lớp
electron khác có chứa tối đa 8 electron hoặc nhiều hơn.
C. Lớp electron trong cùng gần hạt nhân nhất có tối đa 8 electron, các lớp
electron khác có chứa tối đa nhiều hơn 8 electron.
D. Các electron sắp xếp vào các lớp theo thứ tự từ trong ra ngoài cho đến hết.
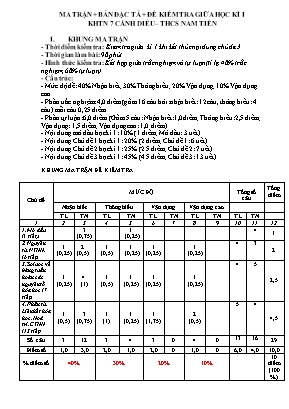
MA TRẬN + BẢN ĐẶC TẢ + ĐỀ KIỂM TRA GIỮA HỌC KÌ I KHTN 7 CÁNH DIỀU – THCS NAM TIẾN KHUNG MA TRẬN - Thời điểm kiểm tra: Kiểm tra giữa kì 1 khi kết thúc nội dung chủ đề 3 - Thời gian làm bài: 90 phút - Hình thức kiểm tra: Kết hợp giữa trắc nghiệm và tự luận (tỉ lệ 40% trắc nghiệm, 60% tự luận) - Cấu trúc: - Mức độ đề: 40% Nhận biết; 30% Thông hiểu; 20% Vận dụng; 10% Vận dụng cao - Phần trắc nghiệm: 4,0 điểm (gồm 16 câu hỏi: nhận biết: 12 câu, thông hiểu: 4 câu) mỗi câu 0,25 điểm - Phần tự luận: 6,0 điểm (Gồm 5 câu: Nhận biết:1,0 điểm; Thông hiểu: 2,5 điểm; Vận dụng: 1,5 điểm; Vận dụng cao: 1,0 điểm) - Nội dung mở đầu học kì 1: 10% (1 điểm; Mở đầu: 3 tiết) - Nội dung Chủ đề 1 học kì 1: 20% (2 điểm; Chủ đề 1: 6 tiết) - Nội dung Chủ đề 2 học kì 1: 25% (2.5 điểm; Chủ đề 2: 7 tiết) - Nội dung Chủ đề 3 học kì 1: 45% (4.5 điểm; Chủ đề 3: 13 tiết) KHUNG MA TRẬN ĐỀ KIỂM TRA Chủ đề MỨC ĐỘ Tổng số câu Tổng điểm Nhận biết Thông hiểu Vận dụng Vận dụng cao TL TN TL TN TL TN TL TN TL TN 1 2 3 4 5 6 7 8 9 10 11 12 1. Mở đầu (3 tiết). 3 (0,75) 1 (0,25) 4 1 2. Nguyên tử. NTHH. (6 tiết). 1 (0,25) 2 (0,5) 1 (0,5) 1 (0,25) 1 (0,25) 1 (0,25) 4 3 2 3.Sơ lược về bảng tuần hoàn các nguyên tố hóa học (7 tiết). 1 (0,25) 4 (1) 1 (0,5) 1 (0,25) 1 (0,25) 1 (0,25) 4 5 2,5 4. Phân tử. Liên kết hóa học. Hoá trị, CTHH (13 tiết) 1 (0,5) 3 (0,75) 1 (1) 1 (0,25) 1 (1,75) 2 (0,5) 5 4 4,5 Số câu 3 12 3 4 3 0 4 0 13 16 29 Điểm số 1,0 3,0 2,0 1,0 2,0 0 1,0 0 6,0 4,0 10,0 % điểm số 40% 30% 20% 10% 10 điểm (100%) II. BẢN ĐẶC TẢ Nội dung Mức độ Yêu cầu cần đạt Số câu hỏi Câu hỏi TL TN TL TN 1. Mở đầu (3 tiết). 4 Nhận biết Trình bày được một số phương pháp và kĩ năng trong học tập môn Khoa học tự nhiên + Phương pháp tìm hiểu tự nhiên. 1 C1 + Sử dụng được một số dụng cụ đo (trong nội dung môn Khoa học tự nhiên). 2 C2, C3 Thông hiểu - Thực hiện được các kĩ năng tiến trình: quan sát, phân loại, liên kết, đo, dự báo. 1 C4 2. Nguyên tử. NTHH.(6 tiết). 4 3 Nhận biết – Trình bày được mô hình nguyên tử của Rutherford – Bohr (mô hình sắp xếp electron trong các lớp vỏ nguyên tử). 1 C5 – Phát biểu được khái niệm về nguyên tố hoá học và kí hiệu nguyên tố hoá học. 1 1 C17a C6 Thông hiểu Viết được công thức hoá học và đọc được tên của 20 nguyên tố đầu tiên. 1 C7 -Xác định được số đơn vị điện tích hạt nhân , số p, số e dựa vào sơ đồ cấu tạo. 1 C17b Vận dụng - Từ cấu tạo nguyên tử xác định được nguyên tố hóa học 1 C17b Vận dụng cao -Vẽ được mô hình nguyên tử 1 C17b 3.Sơ lược về bảng tuần hoàn các nguyên tố hóa học (7 tiết). 4 5 Nhận biết – Nêu được các nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hoá học. 2 C8, C9 – Mô tả được cấu tạo bảng tuần hoàn gồm: ô, nhóm, chu kì. 1 2 C18 C10, C11 Thông hiểu Sử dụng được bảng tuần hoàn để chỉ ra các nhóm nguyên tố/nguyên tố kim loại, các nhóm nguyên tố/nguyên tố phi kim, nhóm nguyên tố khí hiếm trong bảng tuần hoàn. 1 1 C18 C12 Vận dụng Xác định tên và KHHH của nguyên tố khi đã biết nhóm, chu kỳ của nguyên tố đó 1 C18 Vận dụng cao Xác định nhóm, chu kì của nguyên tố hoá học khi biết cấu tạo của nguyên tố hoá học 1 C18 4. Phân tử. Đơn chất, hợp chất. Liên kết hóa học. Hoá trị, CTHH (13 tiết) 4 4 Nhận biết - Nêu được khái niệm phân tử, đơn chất, hợp chất. 2 C13,C14 – Nêu được mối liên hệ giữa hoá trị của nguyên tố với công thức hoá học. 1 C15 – Trình bày được khái niệm về hoá trị (cho chất cộng hoá trị). Các viết công thức hoá học. 1 C19a Thông hiểu – Chỉ ra được sự khác nhau về một số tính chất của chất ion và chất cộng hoá trị. 1 C16 – Viết được công thức hoá học của một số chất và hợp chất đơn giản thông dụng. 1 C19b,c Vận dụng – Xác định được công thức hoá học của hợp chất dựa vào phần trăm (%) nguyên tố và khối lượng phân tử. 1 C20a Vận dụng cao -Lập được công thức hoá học của hợp chất dựa vào phần trăm (%) nguyên tố và khối lượng phân tử. 1 C20b ĐỀ BÀI A. PHẦN TRẮC NGHIỆM (4,0 điểm) Câu 1:Phương pháp tìm hiểu tự nhiên gồm mấy bước? A. 3. B. 4. C. 5. D. 6. Câu 2: Đâu không phải là kĩ năng cần vận dụng vào phương pháp tìm hiểu tự nhiên? A. Kĩ năng chiến đấu đặc biệt; B. Kĩ năng quan sát; C. Kĩ năng dự báo; D. Kĩ năng đo đạc. Câu 3:Trên cơ sở các số liệu và phân tích số liệu, con người có thể đưa ra các dự báo hay dự đoán tính chất của sự vật, hiện tượng, nguyên nhân của hiện tượng . Đó là kĩ năng nào? A. Kĩ năng quan sát, phân loại. B. Kĩ năng liên kết tri thức. C. Kĩ năng dự báo. D. Kĩ năng đo. Câu 4: Để đo tốc độ chuyển động ta cần sử dụng các dụng cụ gì? A. Dụng cụ đo độ dài B. Dụng cụ đo thời gian C.Dụng cụ đo khối lượng D. Cả A và B Câu 5: Phát biểu nào sau đây không mô tả đúng vỏ nguyên tử theo mô hình nguyêntử của Rơ-dơ-pho - Bo? A. Electron chuyến động xung quanh hạt nhân theo từng lớp khác nhau tạo thành các lớp electron. B. Lớp electron trong cùng gần hạt nhân nhất có tối đa 2 electron, các lớp electron khác có chứa tối đa 8 electron hoặc nhiều hơn. C. Lớp electron trong cùng gần hạt nhân nhất có tối đa 8 electron, các lớp electron khác có chứa tối đa nhiều hơn 8 electron. D. Các electron sắp xếp vào các lớp theo thứ tự từ trong ra ngoài cho đến hết. Câu 6. Cách viết: 8 N chỉ ý gì? A. 8 nguyên tử Sodium. B. 8 nguyên tố Nitrogen. C. 8 phân tử Nitrogen. D. 8 nguyên tử Nitrogen. Câu 7. Kí hiệu hóa học của kim loại Copper là: A. cU B. cu C. CU D. Cu. Câu 8. Các nguyên tố hóa học trong bảng tuần hoàn được sắp xếp theo chiều tăng dần của A. nguyên tử khối. B. phân tử khối. C. điện tích hạt nhân. D. số lớp electron trong nguyên tử. Câu 9. Số hiệu nguyên tử của một nguyên tố là A.số proton trong nguyên tử. B.số neutron trong nguyên tử. C.số electron trong hạt nhân. D.số proton và neutron trong hạt nhân. Câu 10. Hiện nay, có bao nhiêu chu kì trong bảng tuần hoàn các nguyên tố hoá học? A.5 B.7 C.8 D.9 Câu 11. Vị trí kim loại kiềm trong bảng tuần hoàn các nguyên tố hoá họcthường A. Ở đầu nhóm B. ở cuối nhóm C. ở đầu chu kì D. ở cuối chu kì Câu 12. Tên gọi của các cột trong bảng tuần hoàn các nguyên tố hoá học là gì? A. Chu kì B. Nhóm C. Loại D. Họ Câu 13: Trong số các chất dưới đây, thuộc loại đơn chất có: A. Oxygen B. Nước C. Muối ăn D. Đá vôi Câu 14: Hợp chất là chất được tạo nên từ: A. Hai hay nhiều nguyên tử B. Hai hay nhiều nguyên tố C. Hai hay nhiều chất D. Hai hay nhiều phân tử Câu 15. Hóa trị của iron trong hợp chất Fe2O3 là I B. II C. III D. IV Câu 16. Phát biểu nào sau đây đúng? A. Để tạo ion âm thì nguyên tử của nguyên tố phi kim sẽ nhường các electron ở lớp ngoài cùng. B. Để tạo ion âm thì nguyên tử của nguyên tố phi kim sẽ nhận thêm electron để có đủ electron ở lớp electron ngoài cùng. C. Để tạo ion âm thì nguyên tử của nguyên tố kim loại sẽ nhận thêm electron để có đủ 8 electron ở lớp electron ngoài cùng. D. Để tạo ion âm thì nguyên tử của nguyên tố hoá học sẽ nhường các electron ở lớp ngoài cùng. B. PHẦN TỰ LUẬN (6,0 điểm) Câu 17 (1,25 điểm):Cho biết nguyên tố hóa học có số đơn vị điện tích hạt nhân là 8. Hãy cho biết: a) Đó là nguyên tố hoá học nào, kí hiệu hoá học của nguyên tố đó? b) Vẽ mô hình nguyên tử đó? Cho biết điện tích hạt nhân, số proton và số electron, số lớp electron trong nguyên tử, số electron lớp ngoài cùng? Câu 18 (1,25 điểm): Sử dụng bảng tuần hoàn hãy xác định vị trí ( số thứ tự, chu kì, nhóm, kí hiệu hoá học, đó là Kim loại, Phi kim hay khí hiếm) của các nguyên tố Aluminium, Calcium, Sodium, Copper, Oxygen. Câu 19 (2 điểm): Hãy tính hoá trị của copper và iron trong các hợp chất sau: Cu(OH)2, Fe(NO3)3. (Biết hoá trị của nhóm OH là I và của nhóm NO3 là I). Hãy viết công thức hoá học và gọi tên của hợp chất được tạo thành từ sự kết hợp các đơn chất sau: - Iron và Chlorine, biết trong hợp chất này Iron hoá trị III và Chlorine hoá trị I. - Sodium và Oxygen, biết Sodium hoá trị I và Oxygen hoá trị II. - Hydrogen và Fluorine, biết Hydrogen hoá trị I và Fluorine hoá trị I. - Potassium và Chlorine, biết Potassium hoá trị I và Chlorine hoá trị I. Tính khối lượng các phân tử Cu(OH)2, Fe(NO3)3 theo đơn vị amu Câu 20 ( 1,5 điểm): a) (0,75 điểm) Xác định phần % theo khối lượng các nguyên tố có trong hợp chất KNO3 b) (0,75 điểm) R là hợp chất của S và O, khối lượng phân tử của R là 64amu. Biết phần trăm khối lượng của oxygen trong R là 50%. Hãy xác định CTHH của R Cho biết: (H=1, O=16, S=32, K=39, N=14, Cu=64, Fe = 56) ĐÁP ÁN KIỂM TRA ĐÁNH GIÁ GIỮA KÌ 1 KHTN7 I. TRẮC NGHIỆM ( 4 điểm) Câu 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 ĐA C A C B C D D C A B C B A A C B II.TỰ LUẬN (6 điểm) Câu Đáp án Điểm Câu 17 (1,25 điểm) -Đó là nguyên tố Oxygen. Kí hiệu là O Điện tích hạt nhân: +8 Số p: 8, số e =8 Số lớp e: 2 Số e lớp ngoài cùng: 6 0,25 Hình 0,5 0,25 0,25 Câu 18 (1,25 điểm) Aluminium thuộc số thứ tự 13. Chu kì 3 nhóm IIIA, Al, Kim loại Calcium thuộc số thứ tự 20, chu kì 4 nhóm IIA, Ca, Kim loại Sodium thuộc số thứ tự 11, chu kì 3 nhóm IA, Na, Kim loại Copper thuộc số thứ tự 29, chu kì 4 nhóm IB, Cu, Kim loại Oxygen thuộc số thứ tự 8, chu kì 2 nhóm VIA, O, Phi kim 0,25 0,25 0,25 0,25 0,25 Câu 19 (2 điểm) Hoá trị Cu: II, hoá trị Fe: III FeCl3 Na2O HF KCl mCu(OH)2 = 98 mFe(NO3)3= 242 0.5 0,25 0,25 0,25 0,25 0,25 0,25 Câu 20 ( 1,5 điểm) a)+ Khối lượng mol của hợp chất: MKNO3 = 39 + 14 + ( 163 ) = 101 gam. + Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất. Trong 1mol KNO3 có: 1mol của K, 1mol N, 3 mol của O. + Thành phần phần trăm của các nguyên tố có trong hợp chất. % K = 39100/101 = 38,6 %. % N = 14100/101 = 13,8%. % O = 100% - ( 38,6 + 13,8 ) = 47,6 %. 0,25 0,25 0,25 b) + Thành phần phần trăm của các nguyên tố có trong hợp chất. mS = 64*50/100 = 32 (gam). mO=64*50/100 = 32 ( gam ). nS = 64/64 = 1 (mol). nO = 32/16 = 2 (mol) CTHH: hợp chất SO2 0,25 0,25 0,25 Nam Tiến, ngày tháng năm 2022 Tổ chuyên môn BGH duyệt Lê Thị Anh Đào Trần Thị Minh Thu
Tài liệu đính kèm:
 de_kiem_tra_giua_hoc_ki_i_mon_khoa_hoc_tu_nhien_lop_7_canh_d.docx
de_kiem_tra_giua_hoc_ki_i_mon_khoa_hoc_tu_nhien_lop_7_canh_d.docx






