Đề khảo sát chất lượng học kì i – Môn: Hóa học khối 8 Trường Thcs Nguyễn Thái Học
Bạn đang xem tài liệu "Đề khảo sát chất lượng học kì i – Môn: Hóa học khối 8 Trường Thcs Nguyễn Thái Học", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
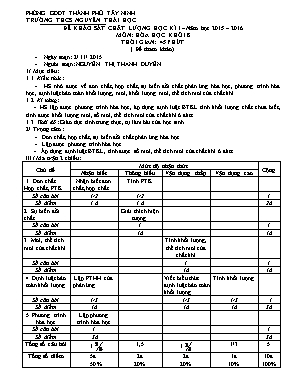
PHÒNG GDĐT THÀNH PHỐ TÂY NINH TRƯỜNG THCS NGUYỄN THÁI HỌC ĐỀ KHẢO SÁT CHẤT LƯỢNG HỌC KÌ I – Năm học 2015 – 2016 MÔN: HÓA HỌC KHỐI 8 THỜI GIAN: 45 PHÚT ( Đề tham khảo) Ngày soạn: 2/ 11/ 2015 Người soạn: NGUYỄN THỊ THANH DUYÊN 1/ Mục tiêu: 1.1. Kiến thức: HS nhớ được về đơn chất, hợp chất, sự biến đổi chất phản ứng hóa học, phương trình hóa học, định luật bảo toàn khối lượng, mol, khối lượng mol, thể tích mol của chất khí. 1.2. Kĩ năng: - HS lập được phương trình hóa học, áp dụng định luật BTKL tính khối lượng chất chưa biết, tính được khối lượng mol, số mol, thể tích mol của chất khí ở đktc. 1.3. Thái độ: Giáo dục tính trung thực, tự làm bài của học sinh. 2/ Trọng tâm: - Đơn chất, hợp chất, sự biến đổi chất phản ứng hóa học - Lập được phương trình hóa học. - Áp dụng định luật BTKL, tính được số mol, thể tích mol của chất khí ở đktc. III/ Ma trận 2 chiều: Chủ đề Mức độ nhận thức Cộng Nhận biết Thông hiểu Vận dụng thấp Vận dụng cao 1. Đơn chất Hợp chất, PTK Nhận biết đơn chất, hợp chất Tính PTK Số câu hỏi 1/2 1/2 1 Số điểm 1 đ 1 đ 2đ 2. Sự biến đổi chất Giải thích hiện tượng Số câu hỏi 1 1 Số điểm 1đ 1đ 3. Mol, thể tích mol của chất khí Tính khối lượng, thể tích mol của chất khí Số câu hỏi 1 1 Số điểm 1đ 1đ 4. Định luật bảo toàn khối lượng Lập PTHH của phản ứng Viết biểu thức định luật bảo toàn khối lượng Tính khối lượng Số câu hỏi 1/3 1/3 1/3 1 Số điểm 1đ 1đ 1đ 3đ 5. Phương trình hóa học Lập phương trình hóa học Số câu hỏi 1 1 Số điểm 3đ 3đ Tổng số câu hỏi 1 1,5 1 1/3 5 Tổng số điểm 5đ 50% 2đ 20% 2đ 20% 1đ 10% 10đ 100% IV/ Đề Kiểm tra HKI: A/ Câu hỏi: Câu 1: (2đ) a/ Hãy chỉ CTHH của đơn chất, hợp chất trong các CTHH sau: Cl2, NaOH, SO2, O3. b/ Tính phân tử khối của hợp chất Fe2(SO4)3 Câu 2: (1đ) Ở gia đình em, thức ăn dùng không hết trong ngày, hôm sau thấy có sự thay đổi màu, mùi, vị. Em hãy cho biết đó là hiện tượng gì? Vì sao? Câu 3: (1đ) Tính: Khối lượng của 0,4 mol CuO? Thể tích khí (đktc) của 0,3mol SO2? Câu 4: (3đ) Hãy hoàn thành các phương trình hóa học sau và cho biết tỉ lệ số nguyên tử, phân tử các chất trong phản ứng: a- P2O5 + H2O H3PO4 b- HgO Hg + O2 c- Al2O3 + H2SO4 Al2(SO4)3 + H2O Câu 5: (3đ) Cho 5,6 g sắt vào 16g dung dịch đồng II sunfat (CuSO4) thấy xuất hiện một lớp đồng màu đỏ và 15,2 g muối sắt II sunfat (FeSO4) tạo thành. a/ Hãy lập PTHH của phản ứng. b/ Viết biểu thức liên hệ về khối lượng giữa các chất trong phản ứng? c/ Tính khối lượng đồng sinh ra? B/ Đáp án: Câu Đáp án Biểu điểm Câu 1: a/ Đơn chất là Cl2, O3 Hợp chất là NaOH, SO2 b/ Phân tử khối của hợp chất Fe2(SO4)3 PTK= 56.2 + (32 + 16 . 4) . 3 = 400 (đvC) 0, 5đ 0, 5đ 0, 5đ 0, 5đ Câu 2: Hiện tượng hóa học vì thức ăn bị oxi hóa thành chất khác. 1đ Câu 3: Khối lượng của 0,4 mol CuO: mCuO = 0,4 . 80 = 32 (g) Thể tích khí (đktc) của 0,3mol SO2: V= 0,3. 22,4= 6,72 (lít) 0, 5đ 0, 5đ Câu 4: a- P2O5 + 3H2O 2H3PO4 1 pt : 3 pt : 2 pt b- 2HgO 2Hg + O2 2 pt : 2 ngt : 1 pt c- Al2O3 + 3H2SO4 Al2(SO4)3+ 3H2O 1 pt : 3 pt : 1 pt : 3 pt 0, 5đ 0, 5đ 0, 5đ 0, 5đ 0, 5đ 0, 5đ Câu 5: a- Fe + CuSO4 FeSO4 + Cu b- mFe + mCuSO = mFeSO + mCu c- 5,6 + 16 = 15,2 + mCu => mCu = 5,6 + 16 – 15,2 = 6,4 g 1đ 1đ 1đ Duyệt của tổ CM Giáo viên bộ môn Nguyễn Thị Thanh Nguyễn Thị Thanh Duyên
Tài liệu đính kèm:
 De_thi_tham_khao_mon_Hoa_lop_8.doc
De_thi_tham_khao_mon_Hoa_lop_8.doc





