Đề cương ôn tập cuối học kì II môn Hóa học Lớp 9 - Năm học 2022-2023
Bạn đang xem tài liệu "Đề cương ôn tập cuối học kì II môn Hóa học Lớp 9 - Năm học 2022-2023", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
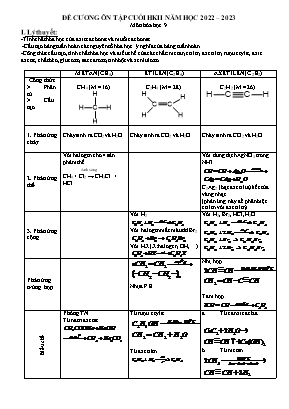
ĐỀ CƯƠNG ÔN TẬP CUỐI HKII NĂM HỌC 2022 – 2023 Môn hóa học 9 I. Lý thuyết: -Tính chất hóa học của axit cacbonic và muối cacbonat -Cấu tạo bảng tuần hoàn các nguyên tố hóa học. ý nghĩa của bảng tuần hoàn. -Công thức cấu tạo, tính chất hóa học và điều chế của các chất: metan, etilen, axetilen, rượu etylic, axit axetic, chất béo, glucozơ, saccarozơ, tinh bột và xenlulozơ. METAN (CH4) ETILEN (C2H4) AXETILEN (C2H2) Công thức Phân tử Cấu tạo CH4 (M = 16) C2H4 (M = 28) C2H2 (M = 26) 1. Phản ứng cháy Cháy sinh ra CO2 và H2O Cháy sinh ra CO2 và H2O Cháy sinh ra CO2 và H2O 2. Phản ứng thế Với halogen cho 4 sản phảm thế Ánh sáng CH4 + Cl2 ® CH3Cl + HCl Với dung dịch AgNO3 trong NH3 C2Ag2 (bạc axetilua) kết tủa vàng nhạt. (phản ứng này để phân biệt etilen với axetilen) 3. Phản ứng cộng Với H2 Với halogen mất màu dd Br2 Với HX (X:halogen, OH,) Với H2, Br2, HCl, H2O Phản ứng trùng hợp Nhựa P.E Nhị hợp Tam hợp Điều chế Phòng TN Từ natri axetat Từ rượu etylic Từ axetilen Từ canxicacbua Từ metan RƯỢU ETYLIC (C2H5OH) AXIT AXETIC (CH3COOH) CHẤT BÉO (LIPIT) (RCOO)3C3H5 GLUCOZO C6H12O6 SACCAROZO C12H22O11 Công thức Phân tử Cấu tạo C2H6O CH3-CH2-OH C2H4O2 R gốc hidrocacbon Tổng quát (RCOO)3C3H5 C6H12O6 C12H22O11 Lý tính Chất lỏng không màu, mùi đặc trung, dễ chịu, vị nồng Sôi ở 78,30C Nhẹ hơn nước (d=0,8) và tan trong nước bất kì tỷ lệ nào Chất lỏng không màu, mùi cay xốc Sôi ở 1180C, dưới p thường Tan vô hạn trong nước Nhẹ hơn nước Không tan trong nước tan nhiều trong dung môi hữu cơ Chất rắn không màu khi nguyên chất Vị ngọt Dễ tan trong nước Chất rắn không màu khi nguyên chất Vị ngọt Tan nhiều trong nước nóng Hóa tính Tác dụng với Na Phản ứng cháy Phản ứng với axit axetic Axit axetic là 1 axit hữu cơ, tính axit yếu Làm tím hóa đỏ Tác dụng với KL Tác dụng với oxit KL Tác dụng với muối Tác dung với bazo 6. Phản ứng với rượu etylic Phản ứng thủy phân chất béo tạo thành glixerol và axit beo Phàn ứng xà phòng hóa Phản ứng oxi hóa glucozo (tráng gương) Glucozo bị oxi hóa thành axit gluconic Lên men Thủy phân saccarozo thu được glucozo và fructozo Fructoz cấu tạo khác glucozo, vị ngọt hơn glucozo Có thể thủy phân saccarozo nhờ tác dụng của enzim ờ nhiệt độ thường Điều chế Sản xuất Công nghiệp Lấy từ mỡ động vật, thực vật Từ tinh bột Ép lấy từ mía Ứng dụng Rượu bia Dược phẩm Cao su tổng hợp Axit axetic Pha vecni, nước hoa Tơ nhân tạo Dược phẩm Phẩm nhuộm Thuốc diệt côn trùng Pha giấm ăn Chất dẻo Làm chất dinh dưỡng cho người và gia súc Điều chế xà phòng, glixerol Pha huyết thanh Tráng gương, ruột phích Sản xuất vitamin C Điều chế rượu etylic, axit lactic Thức ăn cho người Nguyên liệu cho công nghiệp thực phẩm Nguyên liệu pha chế thuốc II. Bài tập trắc nghiệm: Câu 1: Sau khi làm thí nghiệm, khí dư Clo được loại bỏ bằng cách sục khí Clo vào: Dung dịch HCl Dung dịch NaOH Dung dịch NaCl Nước Câu 2: Nhóm các chất đều gồm các hỗn hợp hữu cơ là: K2CO3 ; CH3COOH ; C2H6 ; C2H6O C6H6 ; Ca(HCO3)2 ; C2H5Cl ; CH3OH CH3Cl ; C2H6O ; C3H8 ; CH3COONa C2H4 ; CH4 ; C3H7Br ; CO2 Câu 3: Điều khẳng định nào sau đây không đúng? Chất hữu cơ nào cũng chứa cacbon Chất hữu cơ nào cũng chứa oxi Mỗi chất chỉ có một công thức cấu tạo Công thức cấu tạo cho biết thành phần nguyên tử và trất tự liên kết các nguyên tử trong phân tử Câu 4: Đốt cháy hoàn toàn một hợp chất hữu cơ A thu được khí cacbonic và nước. Điều khẳng định nào sau đây là đúng? Hợp chất A có chứa ít nhất hai nguyên tố C và H Hợp chất A chỉ chứa hai nguyên tố C và H Hợp chất A là hiđro cacbon Hợp chất A là dẫn xuất của hiđro cacbon Câu 5: Trong số các phương trình hóa học sau phương trình nào được viết đúng? CH4 + Cl2+ C6H6 + HCl CH4+ Cl2+ CH3 + HCl CH4+ Cl2+ CH3Cl + HCl CH4+ Cl2+ CH3Cl + H2 Câu 6: Điểm khác biệt cơ bản trong cấu tạo phân tử của etilen so với metan là về: Hoá trị của nguyên tố cacbon Liên kết giữa hai nguyên tử cacbon Hóa trị của hiđro Liên kết đôi của etilen so với liên kết đơn của metan Câu 7: Etilen có thể tham gia phản ứng nào sau đây? Phản ứng cộng brom và hiđro Phản ứng trùng hợp tạo ra polietilen Phản ứng cháy tạo ra khí CO2 và H2O Cả A, B, C Câu 8: Phương pháp hóa học nào sau đây dùng để loại bỏ etilen lẫn trong khí metan? Đốt cháy hỗn hợp trong không khí Dẫn hỗn hợp khí đi qua dung dịch brom dư Dẫn hỗn hợp khí qua dung dịch muối ăn Dẫn hỗn hợp khí qua nước Câu 9: Điều khẳng định nào sau đây không đúng? Liên kết đôi kém bền hơn liên kết đơn. Liên kết đôi bền gấp đôi liên kết đơn. Trong liên kết đôi có một liên kết kém bền hơn liên kết đơn. Etilen làm mất màu dung dịch brom ờ nhiết độ phòng Câu 10: Chất nào trong các chất dưới đây làm mất màu dung dịch brom? CH3 – CH3 CH2 = CH2 CH3 – Cl CH3 – CHO Câu 11: Một hỗn hợp khí gồm CH4 và CO2. Dùng dãy hóa chất nào để thu đựơc từng khí riêng biệt? Dung dịch Ca(OH)2 , dung dịch HCl Dung dịch Ca(OH)2 dư, khí Clo (khi không chiếu sáng) Dung dịch Ca(OH)2 , khí Clo (khi chiếu sáng) Dung dịch Ca(OH)2 dư, dung dịch HCl Câu 12: Trong số các chất sau, chất nào không làm mất màu dung dịch brom. CH2 = CH2 HC CH CH2 = CH – CH3 CH3-CH3 Câu 13: Cho 3,36 lít hỗn hợp A gồm hai khí metan và etilen (đktc). Tỉ khối của A so với hiđro bằng 10. Thể tích của metan và etilen trong hỗn hợp A lần lượt là: 2,24 lít và 1,12 lít 1,12 lít và 2,24 lít 1,68 lít và 1,68 lít 2,00 lít và 1,00 lít Câu 14: Thành phần của dầu mỏ: Dầu mỏ là một đơn chất Dầu mỏ là mốt hợp chất phức tạp Dầu mỏ là một hợp chất tự nhiên của nhiều hiđro cacbon Câu 15: Đốt cháy hoàn toàn 5,6 lít khí metan (đktc). Thể tích khí oxi cần dùng để đốt cháy hết lượng metan đó là: 5,6 lít 11,2 lít 22,4 lít 33,6 lít Câu 16: Cho 1,12 lít etilen (đktc) tác dụng với dung dịch brom. Khối lượng của sản phẩm tạo thành là: 18,8 gam 9,4 gam 5,4 gam 10,8 gam Câu 17: Cồn 900 có nghĩa là: Dung dịch đựơc tạo thành khi hòa tan 90 ml rượu etylic nguyên chất vào 100 ml nước. Dung dịch đựơc tạo thành khi hòa tan 90 ml rượu etylic với 10 gam nước. Trong 100ml dung dịch có 90 ml rược etylic nguyên chất. Câu 18: Thể tích khí oxi cần để đốt cháy 23 gam rượu etylic là: 33,6 lít 11,2 lít 5,6 lít 22,4 lít Câu 19: Chọn thí nghiệm nào sau dây để phân biệt axit axetic với axit clohiđric: Làm đỏ quì tím Phản ứng với đá vôi cho chất khí bay ra Phản ứng với kim loại natri cho chất khí bay ra Phản ứng với rượu etylic khi có H2SO4 đặc nóng Câu 20: Na không tác dụng với chất nào trong các chất sau đây? C6H6 C2H5OH H2O CH3COOH Câu 21: Mg có thể tác dụng với chất nào trong các chất sau đây? C6H6 C2H5OH H2O CH3COOH Câu 22: Dung dịch NaOH có thể tác dụng với chất nào trong các chất sau đây? C6H6 C2H5OH H2O CH3COOH Câu 23: Pha loãng 10 ml rượu 900 bằng nứơc nguyên chất thành 20 ml thì độ rượu của dung dịch rượu là: 500 400 450 550 Câu 24: Phân tử hợp chất hữu cơ A có 2 nguyên tố. Tỉ khối của A so với hiđro là 22. A là chất nào trong số các chất sau: C2H6O C3H8 C3H6 C4H6 Câu 25: Điều khẳng định nào sau đây không đúng? Dầu mỏ tan nhiều trong nứơc Dầu mỏ không tan trong nứơc Dầu mỏ nổi trên mặt nước Dầu mỏ là hỗn hợp nhiều hiđro cacbon Câu 26: Điều khẳng định nào sau đây là đúng? Thành phần chính của khí thiên nhiên là etilen Thành phần chính của khí thiên nhiên là metan và etilen Thành phần chính của khí thiên nhiên là metan Thành phần chính của khí thiên nhiên là axetilen và etilen Câu 27: Rượu etylic phản ứng được với natri vì: Trong phân tử có nguyên tử oxi Trong phân tử có nguyên tử hiđro và nguyên tử oxi Trong phân tử có nguyên tử cacbon, hiđro, oxi Trong phân tử có nhóm – OH Câu 28: Chọn câu đúng nhất Dầu ăn là este Dầu ăn là este của glixenrol Dầu ăn là một este của glixenrol và axit béo. Dầu ăn là hỗn hợp nhiều este của glixenrol và các axit béo. Câu 29: Khi cho chất béo tác dụng với kiềm sẽ thu được glixenrol và: Một muối của axít béo Hai muối của axít béo Ba muối của axít béo Một hỗn hợp muối của axit béo. Câu 30: Chất hữu cơ A là chất rắn màu trắng ở điều kiện thường tan nhiều trong nước. Khi đốt cháy A chỉ thu được CO2 và H2O. A là chất nào trong các chất sau: Etilen Rượu etylic Chất béo Glucozơ III. Bài tập tự luận. DẠNG 1. Viết PTHH theo chuỗi phản ứng (Ghi rõ điều kiện xảy ra phản ứng) Câu 1: Viết phương trình phản ứng hoàn thành dãy chuyển hóa sau, ghi rõ điều kiện phản ứng (nếu có): a. Glucozơ à Rượu Etylic à Axit axetic à Etyl axetat à Axit axetic à Canxi axetat b. CaC2 CH≡CH C2H4 C2H5OH CH3COOH CH3COOC2H5 c) CO CO2NaHCO3Na2CO3NaClNaOH Câu 2. Viết các phương trình hóa học thực hiện sự chuyển đổi hóa học sau: a) Saccarozơ ® Glucozơ ® Rượu etylic ® Axit axetic ® Etyl axtat ® Canxi axetat. b) C2H4 ® C2H6 ® C2H5Cl ® C2H5OH ® CH3COOH ®CH3COONa ® CH4 c) CH4 ® C2H2 ® C2H4 ® C2H5OH ® CH3COOH ® CH3COONa d. C2H4 ® C2H5OH CH3COOH CH3COOC2H5 CH3COONa (2) (1) (3) Natri axetat. (5) (4) e. Glucozơ Rượu Etylic Axit axetic Etyl axetat Axit axetic (3) (2) (1) (5) (4) f. C2H4 C2H5OH CH3COOH (CH3COO)2 Zn C2H5ONa CH3COOC2H5 g. Đá vôi vôi sống đất đèn axetylen etylen P.E Câu 3. Hãy viết các phương trình hóa học trong sơ đồ chuyển đổi hóa học sau : C6H12O6 A + B A + O2 B + D A + O2 C + D A + C CH3COOC2H5 + D Câu 4. Hoàn thành PTHH. Ghi rõ đk phản ứng nếu có. a) CH3COOH + .... → (CH3COO)2Cu + ..... d) (RCOO)3C3H5 + ..... → RCOONa + .... b) C2H5OH + ...... → C2H5ONa + ...... c) C6H12O6 + ...... → Ag + ..... e) H2SO4 + .... → CH3COOH + .... Câu 5. Hoàn thành các phương trình hóa học sau. Ghi rõ điều kiện phản ứng nếu có. a) C2H6 + .... → HCl + ..... b) CH2 = CH2 + Br2 → ..... c) CH º CH + 2Br2 → .. DẠNG 2. Nêu hiện tượng và viết PTHH hoá xảy ra cho mỗi thí nghiệm sau: Câu 1: 1/ Đổ một ít nước vào cốc đựng đất đèn 2/ Cho mẫu natri vào cốc đựng rượu etylic 3/ Nhúng 1 cây đinh sắt vào cốc đựng giấm ăn 4/ Nhỏ một ít giấm vào cục đá vôi 5/ Dẫn khí clo vào ống nghiệm đựng giấy quì tím 6/ Đốt 1 đoạn dây đồng trong lọ đựng khí clo Câu 2. Nêu hiện tượng , giải thích, viết phương trình phản ứng của các thí nghiệm sau : Dẫn khí Axetilen vào dung dịch brom Cho một mẫu đá vôi CaCO3 vào dung dịch axit axetic Cho Na vào rượu etylic Thả mẫu kim loại K vào cốc đựng rượu etylic . Cho vài giọt dd bạc nitrat vào ống nghiệm đựng dd amonic , lắc nhẹ . thêm tiếp dd glucozơ vào ,sau đó đặt ống nghiệm vào trong cốc nước nóng . Câu 3. Trong các chất sau đây: a. C2H5OH ; b. CH3COOH ; c. CH3COOC2H5 Chất nào tác dụng được với Na, NaOH, Mg, CaO? Viết các phương trình hoá học cho phản ứng xảy ra. DẠNG 3. Phân biệt, nhận biết, tách chất: 1/ Nhận biết chất: khí CO2, C2H4, CH4 khí C2H2, SO2, CO khí Cl2, CO2, CH4, HCl các chất lỏng: etylaxetat, rượu etylic, axit axetic các dd :glucozơ, sacarozơ, axit axetic các chất lỏng: etylaxetat, axit axetic, dd glucozơ, rượu etylic các dd: rượu etylic, saccarozơ, glucozơ, axit axetic 2/ Tách chất: a/ Tinh chế CH4 có lẫn khí C2H4, C2H2 b/ Tinh chế CH4 có lẫn CO2, C2H4 DẠNG 4. Lập CTPT chất hữu cơ 1/ Đốt cháy hoàn toàn 1 lít chất hữu cơ A cần 3 lít oxi, thu được 2 lít CO2 và 2 lít hơi nước. Xác định CTPT và CTCT của A, biết các khí đo ở cùng điều kiện nhiệt độ và áp suất. 2/ Lập CTPT của các chất hữu cơ sau: a/ Thành phần 54,5%C ; 9,1%H; 36,4%O và M=88 b/ Thành phần 85,8%H và 14,2% H và chất này có tỉ khối so với khí H2 là 28. 3/ Đốt cháy hoàn toàn 3g chất hữu cơ A thu được 6,6g CO2 và 3,6g H2O, có tỉ khối hơi đối với oxi bằng 1,875. Lập CTPT của A và viết CTCT của A, biết rằng A có thể phản ứng với Na. DẠNG 5. Dạng bài toán hỗn hợp: 1/ Đốt cháy hoàn hoàn hỗn hợp gồm etilen và axetilen rồi dẫn roàn bộ sản phẩm cháy qua bình 1 đựng H2SO4 đặc, bình 2 đựng nước vôi trong dư. Kết thúc thí nghiệm thấy khối lượng 1 tăng 3,6g và bình 2 tăng 13,2g. Tính % khối lượng các khí trong hỗn hợp. 2. Hỗn hợp X gồm axit axetic và rượu etylic. Cho m gam hỗn hơp X tác dụng hết với Natri thấy thoát ra 5,6 lít khí ở đktc. Mặt khác cho m gam X tác dụng vừa đủ với dung dịch NaOH 1,5 M thì hết 200ml. a) Hãy xác định m. b) Tính thành phần % khối lượng mỗi chất trong hỗn hợp. DẠNG 6. Bài toán có liên quan độ rượu 1/ Cho 90ml rượu etylic 900 (d=0,8g/cm3) tác dụng với Na dư. Tính k.l muối và bazơ sinh ra? Tính VH2? 2. Rượu 450 có nghĩa là gì ? Cho kim loại Na vào rượu 450, có những phản ứng nào xãy ra ? Viết các phương trình phản ứng . DẠNG 7. Bài toán có liên đến hiệu suất 1/ Đun nóng hh gồm 3,68g rượu etylic và 3g axit axetic trong điều kiện có H2SO4 đặc làm xúc tác. Tính k.l các chất thu được sau pư biết. Hiệu suất pư este hóa là 60%? 2/ Tính k.l dd axit axetic thu được khi lên men 5 lít rượu 400. Biết drượu = 0,8g/ml và hiệu suất pư là 92%? DẠNG 8. Bài tập có liên quan đến nồng độ dung dịch 1/ Cho 250ml dd axit axetic tác dụng hoàn toàn với kim loại Mg. Cô cạn dd sau pư thu được 14,2g muối khan. a. Tính nồng độ mol của dd axit axetic và thể tích khí H2 sinh ra? b. Để trung hòa 250 ml dd axit axetic nói trên cần bao nhiêu ml dd NaOH 0,5M? 2/ Cho 10,6g Na2CO3 vào dd CH3COOH 5%. Phản ứng xảy ra hoàn toàn. Lượng khí thoát ra dẫn vào bình đựng nước vôi trong dư. Tính khối lượng dd axit axetic đã dùng. Tính khối lượng kết tủa thu được. Tính nồng độ phần trăm dung dịch muối thu được. 3/ Tính khối lượng Na2CO3 cần dùng để phản ứng hết với 50g dd axit axetic 30%.
Tài liệu đính kèm:
 de_cuong_on_tap_cuoi_hoc_ki_ii_mon_hoa_hoc_lop_9_nam_hoc_202.doc
de_cuong_on_tap_cuoi_hoc_ki_ii_mon_hoa_hoc_lop_9_nam_hoc_202.doc





