Bài kiểm tra số 3 môn: Hoá học – lớp 8
Bạn đang xem tài liệu "Bài kiểm tra số 3 môn: Hoá học – lớp 8", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
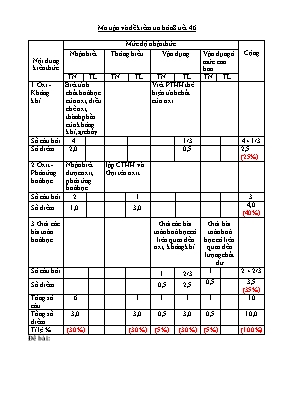
Ma trận và đề kiểm tra hóa 8 tiết 46 Nội dung kiến thức Mức độ nhận thức Cộng Nhận biết Thông hiểu Vận dụng Vận dụng ở mức cao hơn TN TL TN TL TN TL TN TL 1. Oxi - Không khí. Biết tính chất hoá học của oxi, điều chế oxi, thành phần của không khí,sự cháy. Viết PTHH thể hiện tính chất của oxi. Số câu hỏi 4 1/3 4+ 1/3 Số điểm 2,0 0,5 2,5 (25%) 2. Oxit - Phản ứng hoá học. Nhận biết được oxit; phản ứng hoá học. lập CTHH và Gọi tên oxit. Số câu hỏi 2 1 3 Số điểm 1,0 3,0 4,0 (40%) 3. Giải các bài toán hoá học. Giải các bài toán hoá học có liên quan đến oxi, không khí. Giải bài toán hoá học có liên quan đến lượng chất dư Số câu hỏi 1 2/3 1 2 + 2/3 Số điểm 0,5 2,5 0,5 3,5 (35%) Tổng số câu 6 1 1 1 1 10 Tổng số điểm 3,0 3,0 0,5 3,0 0,5 10,0 Tỉ lệ % (30%) (30%) (5%) (30%) (5%) (100%) Đề bài: TRƯỜNG THCS XUÂN CẨM BÀI KIỂM TRA SỐ 3 Môn: HOÁ HỌC – Lớp 8 Thời gian làm bài: 45 phút Họ và tên học sinh: .................................................... Lớp: 8.. Điểm Lời phê của giáo viên Phần I. Trắc nghiệm (4,0 điểm) Hãy khoanh tròn vào câu trả lời đúng nhất. Câu 1. Người ta thu khí oxi bằng phương pháp đẩy nước là do khí oxi có tính chất sau: A. Nặng hơn không khí B. Tan nhiều trong nước C. Ít tan trong nước D. Khó hóa lỏng Câu 2. Điều khẳng định nào sau đây là đúng, không khí là: A. Một hợp chất B. Một hỗn hợp C. Một đơn chất D. Một chất. Câu 3. Phản ứng hoá học có xảy ra sự oxi hoá là: A. 4NH3 + 5O2 4NO + 6H2O B. Na2O + H2O 2NaOH C. CaCO3 CaO + CO2 D. Na2SO4 + BaCl2 BaSO4 + 2NaCl Câu 4. Nhóm công thức nào sau đây biểu diễn toàn oxit A. CuO, CaCO3, SO3 C. FeO; KCl, P2O5 B. N2O5 ; Al2O3 ; SiO2 D. CO2 ; H 2SO4 ; MgO Câu 5. Những chất được dùng để điều chế oxi trong phòng thí nghiệm là: A. KClO3 và KMnO4 . B. KMnO4 và H2O. C. KClO3 và CaCO3 . D. KMnO4 và không khí. Câu 6. Phản ứng nào dưới đây là phản ứng hóa hợp. A. CuO + H2 Cu + H2O B. CO2 + Ca(OH)2 CaCO3 + H2O. C. 2KMnO4 K2MnO4 + MnO2 + O2 D. CaO + H2O Ca(OH)2 . Câu 7. Khi phân hủy 122,5g Kaliclorat KClO3 (có xúc tác) thể tích khí oxi thu được là A. 48,0 (l) B. 24,5 (l) C. 67,2 (l) D. 33,6 (l) Câu 8. Cho 13,5g kim loại nhôm tác dụng với 8,96 lít khí oxi ở đktc. Khối lượng của nhôm oxit sau khi phản ứng kết thúc là: A. 49,25 g ; B. 79,0 g ; C. 25,5 g ; D. 39.5 g Phần II. Tự luận (6,0 điểm) Câu 1 (3,0 điểm). Điền công thức hoá học và tên gọi vào ô trống trong bảng sau: Nguyên tố K(I) S(VI) C(IV) Fe(II) P(V) Al(III) CTHH của oxit Tên gọi Câu 2 (3,0 điểm). Đốt cháy hoàn toàn 1,24 gam photpho trong khí oxi tạo thành điphotpho pentaoxit. Viết phương trình hoá học của phản ứng xảy ra. Tính khối lượng điphotpho pentaoxit được tạo thành. Tính thể tích khí oxi (ở đktc) đã tham gia phản ứng. (Cho biết: P = 31; O = 16) BÀI LÀM Đáp án - Biểu điểm. Trắc nghiệm (4,0 điểm) Mçi câu ®óng: 0,5 ®iÓm Câu 1 2 3 4 5 6 7 8 Đáp án C B A B A D D C II. Tự luận (6điểm). Câu 1(3,0 ®iÓm). Mçi trêng hîp ®óng: 0,5 ®iÓm Nguyên tố K S(VI) C(IV) Fe(II) P(V) Al CTHH của oxit K2O SO3 CO2 FeO P2O5 Al2O3 Tên gọi Kali oxit Lưu huỳnh đi oxit Cacbon đi oxit Sắt(II)oxit Đi photpho penta oxit Nhôm oxit Câu 2: (3,0 ®iÓm). Ph¬ng tr×nh hãa häc: 4P + 5O2 2P2O5 0,5®iÓm b) 0,5®iÓm Theo PTHH: 1,0 ®iÓm c) 1,0 ®iÓm
Tài liệu đính kèm:
 Kiem_tra_tiet_46_Hoa_hoc_8.doc
Kiem_tra_tiet_46_Hoa_hoc_8.doc





