2 Đề kiểm tra học kì I Hóa học 8 - Năm học 2022-2023 - Trường PTDTBT TH&THCS Bản Liền (Có đáp án + Ma trận)
Bạn đang xem tài liệu "2 Đề kiểm tra học kì I Hóa học 8 - Năm học 2022-2023 - Trường PTDTBT TH&THCS Bản Liền (Có đáp án + Ma trận)", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
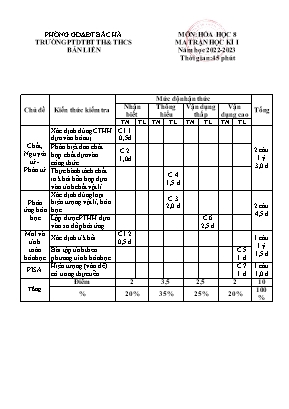
PHÒNG GD&ĐT BẮC HÀ MÔN: HÓA HỌC 8 TRƯỜNG PTDTBT TH& THCS MA TRẬN HỌC KÌ I BẢN LIỀN Năm học 2022-2023 Thời gian: 45 phút Mức độ nhận thức Chủ đề Kiến thức kiểm tra Nhận Thông Vận dụng Vận Tổng biết hiểu thấp dụng cao TN TL TN TL TN TL TN TL Xác định đúng CTHH C1.1 dựa vào hóa trị 0,5đ Chất, Phân biệt đơn chất 2 câu Nguyên C 2 hợp chất dựa vào 1 ý tử - 1,0đ công thức 3,0 đ Phân tử Thực hành tách chất C 4 ra khỏi hỗn hợp dựa 1,5 đ vào tính chất vật lí Xác định đúng loại C 3 Phản hiện tượng vật lí, hóa 2,0 đ 2 câu ứng hóa học 4,5 đ học Lập được PTHH dựa C 6 vào sơ đồ phản ứng 2,5 đ Mol và C1.2 Xác định tỉ khối 1 câu tính 0,5 đ 1 ý toán Bài tập tính theo C 5 1,5 đ hóa học phương trình hóa học 1 đ Hiện tượng (vấn đề) C 7 1 câu PISA có trong thực tiễn 1 đ 1,0 đ Điểm 2 3,5 2,5 2 10 Tổng 100 % 20% 35% 25% 20% % PHÒNG GD&ĐT BẮC HÀ KIỂM TRA HỌC KÌ I TRƯỜNG PTDTBT TH & THCS MÔN: HÓA HỌC 8 BẢN LIỀN Năm học 2022-2023 Thời gian: 45 phút(không kể thời gian giao đề) Đề I I.Trắc nghiệm(2đ) Câu 1. (1,0đ) Khoanh tròn vào chữ cái đứng trước đáp án trả lời đúng. Câu 1.1 Những chất nào dưới đây là đơn chất: A. H2O B. Cu C. HCl D. O2 E. Cu(OH)2 Câu 1.2 Hãy xác định công thức hoá học đúng của 2 hợp chất sau: Cu xOy và CuxCly (Biết Cu có hóa trị II, O hóa trị II và Cl hóa trị I) A. CuO B. Cu2O C. CuO2 D. CuCl E. CuCl2 F. Cu2Cl Câu 2. (1,0đ) Hãy lựa chọn “Đúng” hoặc “ Sai” và ghi vào cột đáp án tương ứng với những hiện tượng sau: Hiện tượng Đáp án 1.Đốt đường bị phân hủy thành than và nước là hiện tượng hóa học. . .. . .. 2. Cho cốc nước vào trong tủ lạnh nước bị đông thành đá là hiện tượng vật lí. 3. Thổi hơi thở vào cốc nước đựng dung dịch nước vôi trong thấy nước vôi trong vẩn đục là hiện tượng vật lí. 4. Đun sôi nước thấy nước bị bay hơi là hiện tượng hóa học. II. Tự luận(8đ) Câu 3. (1,0đ) Hãy trình bày phương pháp để tách riêng biệt các chất ở 2 hỗn hợp sau: a. Muối ăn và cát đã hòa tan vào trong nước. b. Bột sắt và bột nhôm trộn lẫn với nhau. Câu 4. (1,0đ) Lập phương trình hóa học sau: a. Hg + O2 -----› HgO b. BaCl2 + H2SO4 -----› BaSO4 + HCl Câu 5. (1,0đ) a. Hãy so sánh xem khí O2 nặng hay nhẹ hơn khí H2 bao nhiêu lần? b. Hãy so sánh xem khí SO2 nặng hay nhẹ hơn không khí bao nhiêu lần? (Biết O=16; H=1; S=32) Câu 6. (3,0 điểm) Cho 2,4 (g) kim loại Magie (Mg) vào dung dịch axit clohiđric (HCl). Phản ứng kết thúc thu được muối Magie clorua (MgCl2) và có khí hiđro (H2) thoát ra. a. Viết phương trình hóa học xảy ra? b. Tính khối lượng MgCl2? c. Tính thể tích khí H2 (ở đktc)? Câu 7. (2,0đ)SỰ BIẾN ĐỔI CHẤT Để diệt chuột trong một nhà kho người ta thường dùng phương pháp đốt lưu huỳnh, đóng kín cửa nhà kho lại. Chuột hít phải khói sẽ bị co giật, tê liệt cơ quan hô hấp dẫn ngạt mà chết. Hãy viết phương trình phản ứng đốt cháy lưu huỳnh. Hãy cho biết chất nào đã làm chết chuột? ( Biết Mg= 24, Cl=35,5) PHÒNG GD&ĐT BẮC HÀ ĐÁP ÁN + HƯỚNG DẪN CHẤM TRƯỜNG PTDTBT TH & THCS MÔN: HÓA HỌC 8 BẢN LIỀN Năm học 2022-2023 ĐỀ I Câu Đáp án Điểm I. Trắc nghiệm (2,0đ) 1.1 B và D (Mỗi ý đúng đạt 0,25đ) 0,5 đ 1.2 A và E (Mỗi ý đúng đạt 0,25đ) 0,5 đ 1.Đúng 0,25 đ 2 2.Đúng 0,25 đ 3.Sai 0,25 đ 4.Sai 0,25 đ II. Tự luận(8,0đ) 3 a. Đổ hỗn hợp qua một phễu lọc thu được cát trên giấy lọc. 0,5đ Sau đó đun sôi để cô cạn dung dịch thu được muối dưới đáy cốc. b.Dùng nam châm để hút sắt(vì sắt có tính nhiễm từ) còn 0,5đ lại là nhôm. 4 a.2Hg + O2 → 2HgO 0,5đ b.BaCl + H SO → BaSO + 2HCl 2 2 4 4 0,5đ 5 a. dO2/H2 = 32: 2 = 16 Vậy khí O2 nặng hơn khí H2 = 16 lần. 0,5đ b. dSO2/kk = 64:29 =2,2 Vậy khí SO2 nặng hơn không khí 2,2 lần. 0,5đ 6 a.Phương trình hoá học. Mg + 2HCl MgCl2 + H2 0,5đ 0,1(mol) 0,1(mol) 0,1(mol) b. Số mol của Mg là: -ADCT: n=m:M =>nmg= 2,4 : 24 = 0,1 (mol) 0,5đ n n -Ta có: MgCl2 = Mg= 0,1(mol) Khối lượng muối MgCl2 thu đựơc là: 0,5đ m -ADCT: m=n.M => MgCl2= 0,1. 95 = 9,5 (g) 0,5đ n n c. Ta có: H2= Mg = 0,1(mol) Thể tích khí H2 thoát ra (ở đktc) là: 0,5đ V ADCT: V=n.22,4 => H2= 0,1.22,4 = 2,24(l) 0,5đ 7 -Phương trình hoá học đốt cháy lưu huỳnh o S + O2 (t ) SO2 1đ - Khi đốt lưu huỳnh sẽ cháy trong không khí tạo thành khí 1đ SO2 đã làm chuột chết vì SO2 là khí độc. Tổng 10 đ PHÒNG GD&ĐT BẮC HÀ KIỂM TRA HỌC KÌ I TRƯỜNG PTDTBT TH & THCS MÔN: HÓA HỌC 8 BẢN LIỀN Năm học 2022-2023 Thời gian: 45 phút(không kể thời gian giao đề) Đề II I.Trắc nghiệm(2đ) Câu 1. (1,0đ) Khoanh tròn vào chữ cái đứng trước đáp án trả lời đúng. Câu 1.1 Những chất nào dưới đây là hợp chất: A. H2 B. Na C. H2SO4 D. KOH E. O2 Câu 1.2 Hãy xác định công thức đúng của 2 hợp chất sau: KxOy và KxCly (Biết K có hóa trị I, O hóa trị II và Cl hóa trị I) B. KO B. K2O C. KO2 D. KCl E. KCl2 F. K2Cl Câu 2. (1,0đ) Hãy lựa chọn “Đúng” hoặc “ Sai” và ghi vào cột đáp án tương ứng với những hiện tượng sau: Hiện tượng Đáp án 1.Lưu huỳnh tác dụng với sắt tạo thành sắt(II) Sunfua là . .. . .. hiện tượng vật lí. 2. Thủy tinh nóng chảy bị thổi thành bình cầu là hiện tượng hóa học. 3. Hòa tan đường vào nước tạo thành nước đường là hiện tượng vật lí. 4. Cây nến đang cháy bị nóng chảy là hiện tượng hóa học II. Tự luận (8đ) Câu 3. (1,0đ) Hãy trình bày phương pháp để tách riêng biệt các chất ở 2 hỗn hợp sau: a. Muối ăn và cát đã hòa tan vào trong nước. b. Bột sắt và bột nhôm trộn lẫn với nhau. Câu 4. (1,0đ) Lập phương trình hóa học sau: a. Na + O2 -----› Na2O b. SO2 + NaOH -----› Na2SO3 + H2O Câu 5.(1,0đ) a. Hãy so sánh xem khí Cl2 nặng hay nhẹ hơn khí H2 bao nhiêu lần? b. Hãy so sánh xem khí NO2 nặng hay nhẹ hơn không khí bao nhiêu lần? (Biết Cl=35,5 ; H=1 ; N = 14; O=16) Câu 6. (3,0đ) Cho 13(g) kim loại Kẽm (Zn) vào dung dịch axit sunfuric (H 2SO4). Phản ứng kết thúc thu được muối Kẽm sunfat (ZnSO4) có khí hiđro (H2) thoát ra. a. Viết phương trình hóa học xảy ra? b. Tính khối lượng ZnSO4? c. Tính thể tích khí H2 (ở đktc)? ( Biết Zn= 65; S=32; O=16) Câu 7. (2,0đ)SỰ BIẾN ĐỔI CHẤT Để diệt chuột trong một nhà kho người ta thường dùng phương pháp đốt lưu huỳnh, đóng kín cửa nhà kho lại. Chuột hít phải khói sẽ bị co giật, tê liệt cơ quan hô hấp dẫn ngạt mà chết. Hãy viết phản ứng đốt cháy lưu huỳnh.Cho biết chất nào đã làm chết chuột? PHÒNG GD&ĐT BẮC HÀ ĐÁP ÁN + HƯỚNG DẪN CHẤM TRƯỜNG PTDTBT TH & THCS MÔN: HÓA HỌC 8 BẢN LIỀN Năm học 2022-2023 ĐỀ II Câu Đáp án Điểm Phần I: Trắc nghiệm (2,0đ) 1.1 C và D (Mỗi ý đúng đạt 0,25đ) 0,5 đ 1.2 B và D (Mỗi ý đúng đạt 0,25đ) 0,5 đ 1.Sai 0,25 đ 2 2.Sai 0,25 3.Đúng đ 4.Sai 0,25 đ 0,25 đ Phần II. Tự luận(8,0đ) 3 a. Đổ hỗn hợp qua một phễu lọc thu được cát trên giấy 0,5đ lọc. Sau đó đun sôi để cô cạn dung dịch thu được muối dưới đáy cốc. b.Dùng nam châm để hút sắt(vì sắt có tính nhiễm từ) còn 0,5đ lại là nhôm. 4 a. 4Na + O2 → 2Na2O 0,5đ b.SO + 2NaOH → Na SO + H O 2 2 3 2 0,5đ d 5 a. Cl2/H2 = 71: 2 = 35,5 Vậy khí Cl2 nặng hơn khí H2 = 35,5 lần. 0,5đ d b. NO2/kk = 46:29 = 1,59 lần Vậy khí NO2 nặng hơn không khí 1,59 lần. 0,5đ 6 a.Phương trình hoá học. Zn + H2SO4 ZnSO4 + H2 0,5đ 0,2(mol) 0,2(mol) 0,2(mol) b. Số mol của Zn là: 0,5đ ADCT: n=m:M =>nZn= 13: 65 = 0,2 (mol) n n Ta có: ZnSO4 = Zn= 0,2(mol) 0,5đ Khối lượng muối ZnSO4 thu đựơc là: m ADCT: m=n.M => ZnSO4= 0,2. 161 = 32,2 (g) 0,5đ n n c. Ta có: H2= Zn = 0,2(mol) Thể tích khí H2 thoát ra (ở đktc) là: 0,5đ V ADCT: V=n.22,4 => H2= 0,2.22,4 = 4,48(l) 0,5đ 7 -Phương trình hoá học đốt cháy lưu huỳnh o S + O2 (t ) SO2 1đ - Khi đốt lưu huỳnh sẽ cháy trong không khí tạo thành khí 1đ SO2 đã làm chuột chết vì SO2 là khí độc. Tổng 10 đ Người ra đề Duyệt Tổ chuyên môn Duyệt của Ban giám hiệu
Tài liệu đính kèm:
 2_de_kiem_tra_hoc_ki_i_hoa_hoc_8_nam_hoc_2022_2023_truong_pt.docx
2_de_kiem_tra_hoc_ki_i_hoa_hoc_8_nam_hoc_2022_2023_truong_pt.docx






